Clear Sky Science · zh
一种无赖氨酸 REC 标签系统用于近邻生物素化应用
为什么蛋白上的微小标签很重要
在每个细胞内,蛋白质很少独自发挥作用——它们在不断变化的组合中协同工作,驱动健康与疾病的进程。为了研究这些组合,科学家经常在蛋白质上附加小型“名牌”,以便追踪、从混合物中拉出或在显微镜下观察。一种流行的方法称为近邻生物素化,可以绘制细胞内谁靠近谁的图谱,但它带有一个隐性问题:许多这些名牌在关键时刻会被化学修饰,从而有效“消失”。本研究介绍了一种新型标签,称为 REC 标签,旨在在这些苛刻条件下保持可见。
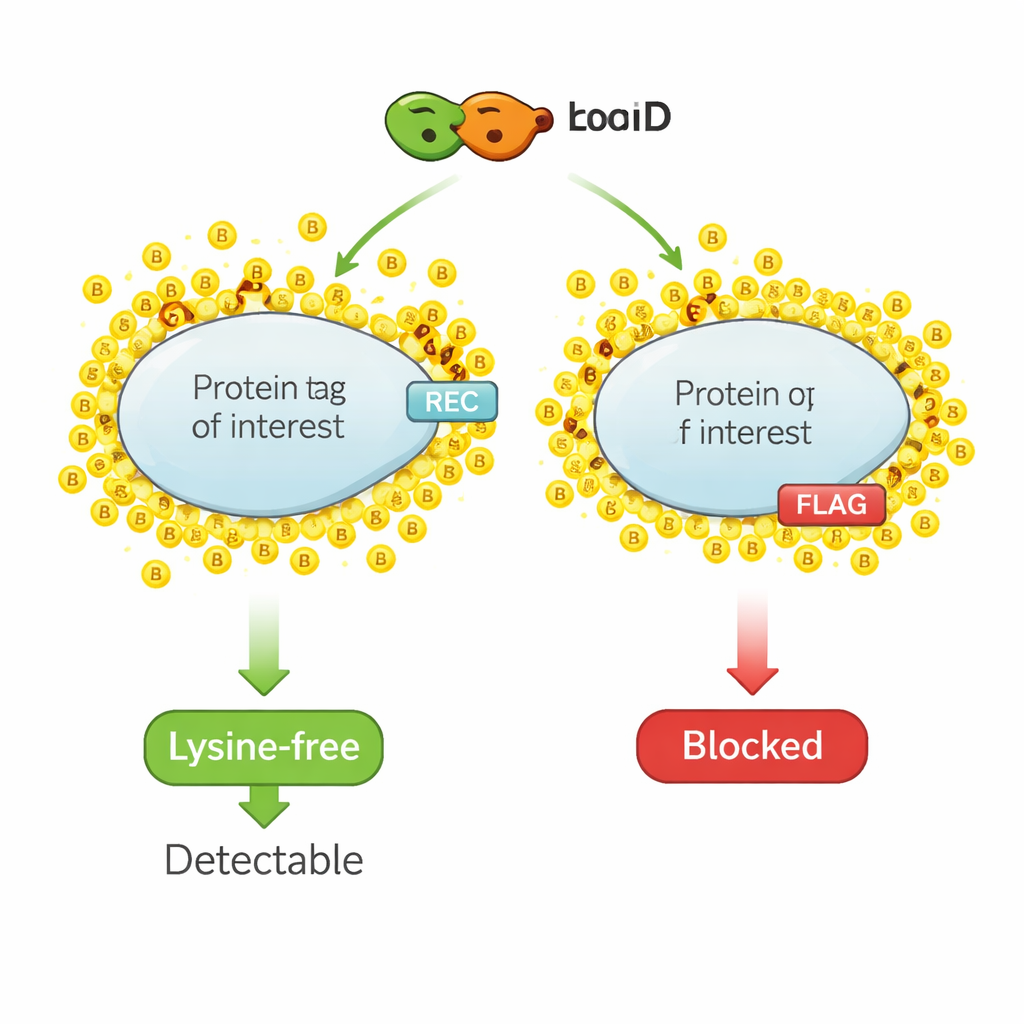
用于标记蛋白邻近者的化学高亮笔
近邻生物素化的工作原理类似于分子高亮笔。一个经过工程改造的酶,例如 TurboID,与目标蛋白融合。当加入生物素——一种小分子维生素时,TurboID 会迅速将生物素分子附着到附近的蛋白质上。研究人员随后将所有被生物素标记的蛋白富集并鉴定,从而获得该蛋白局部邻域的快照。然而,同样的化学反应也会作用于常用于检测的小型表位标签,因为这些标签通常含有赖氨酸——赖氨酸是生物素的主要附着位点。当标签中的赖氨酸被生物素覆盖后,抗体就无法识别该标签,标准检测方法的信号就会下降或消失。
设计一个拒绝被修饰的标签
为了解决这一问题,作者着手设计一种完全不含赖氨酸的新标签。他们从疟原虫蛋白 PfRipr5 的片段出发,该片段与人源蛋白相似性低,从而降低了不良交叉反应的风险。研究者使用基于芯片的兔源筛选方法,针对 PfRipr5 产生了 22 种单克隆抗体,并鉴定出一种编号为 6 的克隆,具有特别强且特异的结合能力。通过系统地修剪和突变 PfRipr5 片段,他们将抗体的识别位点缩小到一个 11 个氨基酸的短序列。该最小序列仅含有一个赖氨酸,他们将其替换为类似的氨基酸——精氨酸。令人惊讶的是,抗体的结合能力并未受影响。这个优化后的无赖氨酸序列被命名为 REC 标签,与之配套的抗体称为 REC 抗体。
让 REC 标签接受考验
接着,团队测试了 REC 标签是否能在常用实验中替代诸如 FLAG 之类的广泛使用标签。当与荧光或信号蛋白融合并在体外合成体系及哺乳动物细胞中表达时,带有 REC 标签的蛋白可以被免疫印迹、高灵敏度的基于光学的板式测定(AlphaScreen)以及细胞免疫染色轻易检测到。检测强度与 FLAG 标签以及另一种无赖氨酸标签系统(AGIA)相当,且在多种人源和猴源细胞系中,REC 抗体显示出非常低的背景噪声。重要的是,该标签无论放在蛋白的 N 端还是 C 端,以及位于不同细胞区室(包括细胞核、线粒体、内质网和细胞膜)时都能工作。
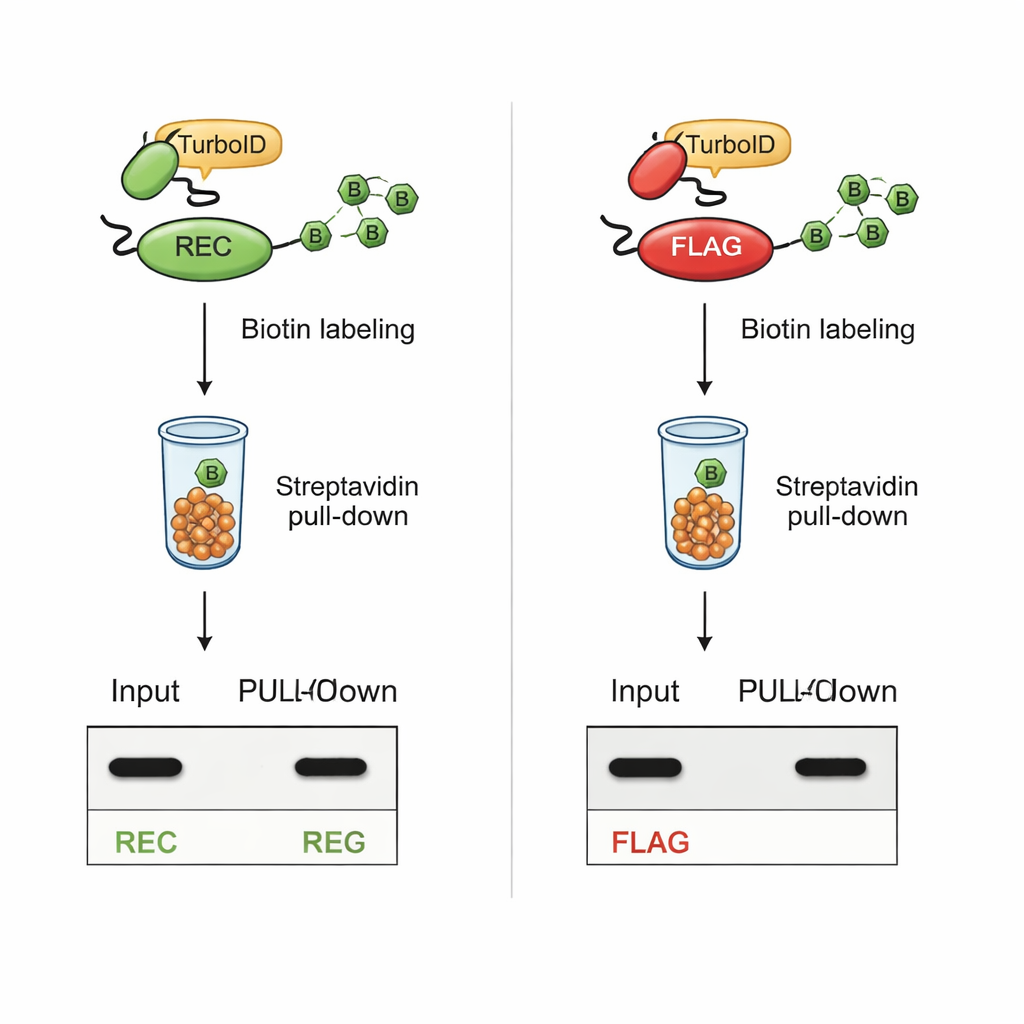
在强烈标记条件下保持可见
关键测试是 REC 在基于 TurboID 的生物素化后是否仍可检测到。在 TurboID 与已知相互作用伙伴融合的细胞中,携带 REC 标签的蛋白在全细胞提取物和富集的生物素标记组分中都保持清晰可见。相比之下,携带经典 FLAG 标签的蛋白一旦 TurboID 活化,其 FLAG 信号就丧失了,尽管这些蛋白本身仍然存在。用合成肽进行的额外实验表明,TurboID 会直接对 FLAG 序列中的赖氨酸进行生物素化,从而物理性地阻碍抗体结合。由于 REC 标签完全不含赖氨酸,它不受 TurboID 影响,仍然易于检测。
这对未来实验意味着什么
对于在活细胞中探索蛋白网络的研究者来说,REC 标签提供了一个实用的新工具:它在日常测定中表现得像熟悉的标签,但在强效近邻标记酶活跃时仍能继续工作。这意味着科学家可以更可靠地确认其带标记的蛋白是否存在并被正确捕获,并且可以研究其他基于赖氨酸的修饰——例如泛素化和乙酰化——而不会被标签本身干扰。简而言之,REC 是一个小小的设计改动却带来重大影响,帮助使复杂的蛋白质绘图实验更清晰、更可靠。
引用: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
关键词: 蛋白质标记, 近邻生物素化, TurboID, 蛋白质相互作用, 抗原表位标签