Clear Sky Science · zh
ELMO1 DNA 甲基化与 Med31 相互作用促进幽门螺杆菌诱导的胃癌上皮‑间质转化和肠上皮化生通过 M2 极化
为何胃内细菌与癌症风险相关
我们多数人在消化道内携带数十亿细菌,其中一种——幽门螺杆菌——可以在胃中悄然生存数十年。对部分人来说,这种感染无害,但对另一些人则可能成为通向胃癌的第一步,胃癌是全球致死率很高的癌症之一。本研究探讨的是,胃细胞中 DNA 上一种微小的化学修饰如何帮助将长期感染转变为癌前损伤,进而形成有利于肿瘤生长的局部环境。
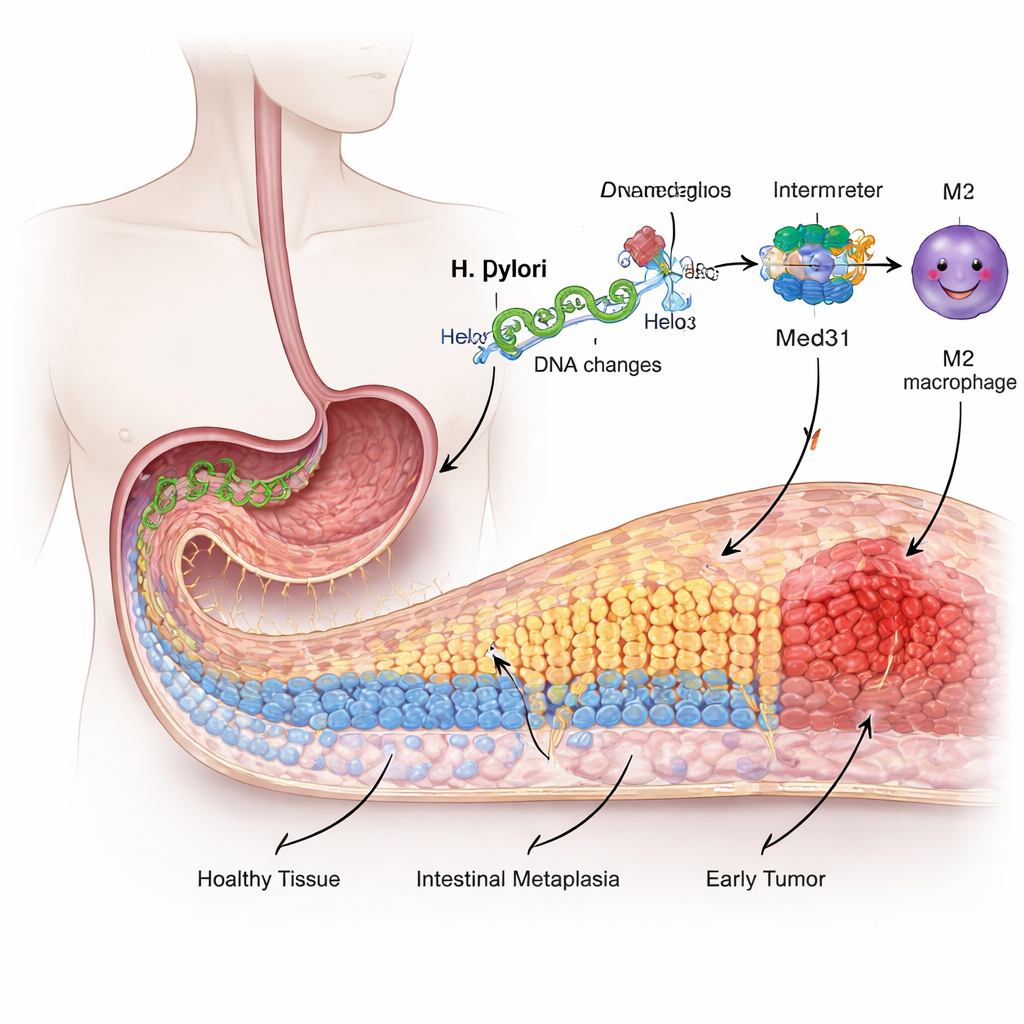
从友好的黏膜到风险改造
胃的内表面由专门化的细胞覆盖,这些细胞适应了强酸环境,而不是像肠道那样负责食物消化。由于长期被幽门螺杆菌引起的刺激和炎症,其中一些胃细胞会开始“重新装扮”自己,呈现出肠道细胞的特征,这一过程称为肠上皮化生。该改变被视为癌前阶段。研究者使用人类胃细胞系模拟感染,发现暴露于幽门螺杆菌会使这些细胞增殖更快、迁移能力增强,并激活肠型标志物,所有这些都是黏膜身份发生改变的信号。
微小化学标签带来的重大后果
我们的 DNA 可以被一种称为甲基的微小化学标签标记,这些标签像基因的开关一样调节基因活性,而不改变遗传编码。研究团队聚焦于一个名为 ELMO1 的基因,它已知参与细胞运动和癌症转移。他们显示,幽门螺杆菌感染增加了 ELMO1 的甲基化,并且有些出人意料地同时提升了该基因在胃细胞中的活性和蛋白水平。当用能去除这些甲基标签的药物处理时,细胞失去了许多由感染驱动的改变:增殖减少、迁移减少,肠上皮化生的信号也减弱。这表明 ELMO1 的甲基化是细菌触发的一个关键开关。
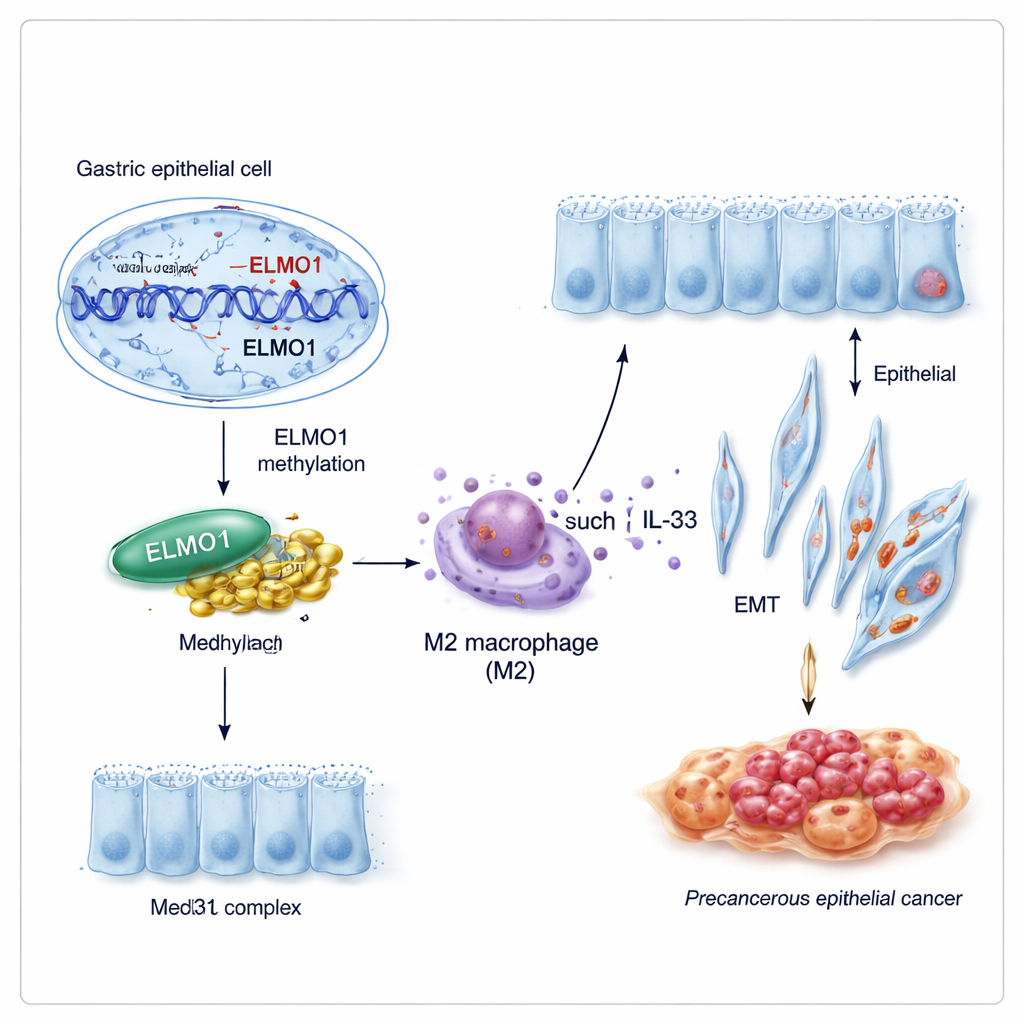
重接线细胞行为的新伙伴关系
基因很少单独起作用。研究者发现,甲基化的 ELMO1 倾向于与另一种蛋白 Med31 建立伙伴关系,Med31 是参与决定细胞启动哪些基因的大型“控制板”的一部分。在促进 DNA 甲基化的条件下,ELMO1 水平上升,Med31 增加,两者发生了物理结合,而 ELMO1 的一个已知旧伙伴 DOCK10 则被置于次要地位。这个新的 ELMO1–Med31 组合似乎改变了胃细胞的基因表达程序,促使它们采纳肠上皮特征并表现得更具侵袭性。
免疫细胞如何被推向助肿瘤一方
癌症并非孤立发生;它在由免疫细胞和支持细胞构成的复杂邻里中生长。研究表明,带有甲基化 ELMO1 的被感染胃细胞释放更多 IL‑33,这是一种信号,促使周围的免疫细胞——巨噬细胞——向有利肿瘤的“M2”状态转变。通过共培养系统,作者发现暴露于这些信号的巨噬细胞明显倾向于 M2 型,而这些 M2 巨噬细胞反过来分泌因子,推进新的胃细胞变得更具迁移性、更具侵袭性,并更像肠上皮细胞。在 M2 巨噬细胞影响下,上皮‑间质转化的标志物显著上升,即原本固定的上皮细胞转变为能够游走和入侵的细胞。
这对预防胃癌意味着什么
综合来看,这项工作描绘了一条事件链:幽门螺杆菌感染改变了 ELMO1 的 DNA 甲基化,这一改变的 ELMO1 与 Med31 结成联盟,被感染的细胞释放信号将周围免疫细胞转化为 M2 助手,而这些助手进一步推动肠上皮化生和更具侵袭性的细胞状态。对非专业读者来说,关键观点是常见的胃内细菌可以通过可逆的 DNA 化学修饰重塑胃黏膜及局部免疫反应。理解这一途径可能为开发可通过血液检测及早发现风险甲基化模式的新方法,或开发在慢性感染进展为胃癌前干预 ELMO1–Med31–M2 轴的药物,打开新的途径。
引用: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
关键词: 胃癌, 幽门螺杆菌, DNA 甲基化, 肠上皮化生, 肿瘤微环境