Clear Sky Science · zh
评估系统性淀粉样变性抗性的生化基础
微小蛋白质变化如何阻止致命堆积
从类风湿性关节炎到结核病,许多慢性炎症性疾病都可能引发一种罕见但常致命的并发症——系统性 AA 淀粉样变性。在这种情况下,一种正常的血液蛋白质以刚性纤维的形式积累,堵塞器官。本研究提出了一个出乎意料的乐观问题:该蛋白的微小天然变体是否能让某些动物在很大程度上对该疾病免疫——如果可以,其机理是什么?
蛋白质堆积的隐秘威胁
AA 淀粉样变性始于血液中的一种炎症报警信号,称为血清淀粉样蛋白 A(SAA)。在严重或长期炎症期间,SAA 水平可能上升到正常值的数千倍。在某些人和动物中,部分该蛋白发生错误折叠并堆积成长长的纤维,即淀粉样纤维,这些纤维遍布脾脏和肾脏等器官。随着时间推移,这些纤维会损害器官功能。然而,并非所有 SAA 水平很高的个体都会发展为淀粉样变性,而且某些小鼠品系即便在实验室中被促发,仍出人意料地具有抵抗性。搞清楚原因可能为预防人类淀粉样堆积提供新策略。
抗性小鼠及其特殊的蛋白变体
在小鼠中,大多数 AA 淀粉样纤维来自一种称为 SAA1.1 的 SAA 变体,该变体与疾病密切相关。然而,一些小鼠品系主要产生略有不同的变体,称为 SAA1.5 和 SAA2.2,这些品系很少发生系统性 AA 淀粉样变性。这些蛋白仅在少数构建单元(氨基酸)上存在差异,但这些变化集中在形成致病纤维内核的一个紧密堆积区域。研究人员提出,这些微小差异并不完全阻止蛋白质聚集,而是阻碍它们采用那种特定的、有害的纤维构象。
在实验室中检验这些蛋白
为检验这一假设,研究团队在细菌中产生了这三种小鼠 SAA 变体,并在试管实验中观察它们的行为。他们使用一种在淀粉样形成时会发光的荧光染料来监测纤维形成,并用电子显微镜验证结构。与疾病相关的 SAA1.1 容易形成长而直的纤维。SAA2.2 也能形成纤维,但这些纤维更粗、更扭曲、结构更为多样,且没有产生相同强度的染料信号。相比之下,SAA1.5 在所测试的条件下未能形成纤维。当科学家向体系中加入从病鼠脾脏提取的真实致病纤维作为“种子”时,SAA1.1 很快在其上生长出与原始结构高度相似的新纤维,类似朊病毒的传播方式。显著的是,SAA1.5 和 SAA2.2 完全无法在这些种子上生长;体外的致病纤维无法将它们招募成致病构象。
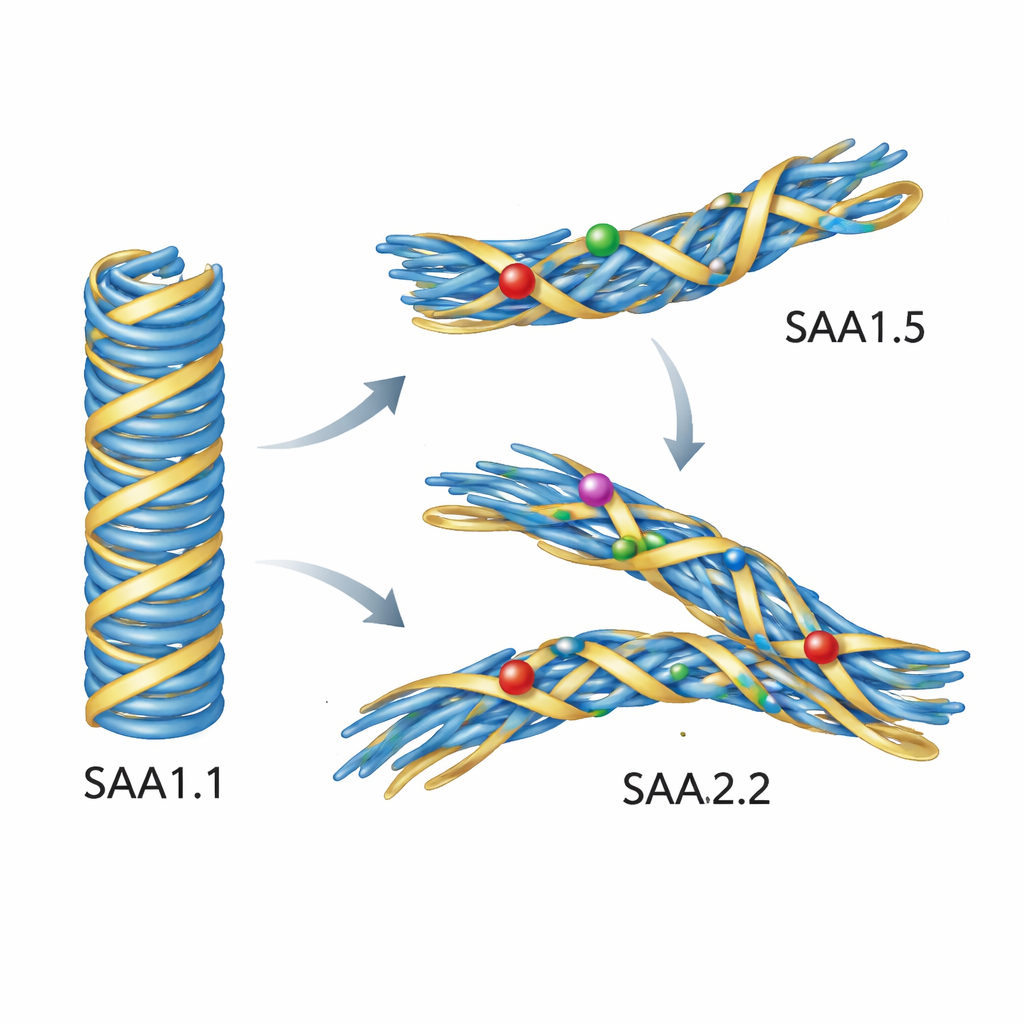
模拟揭示突变蛋白为何拒绝这种有害构象
单靠实验无法精确展示原子层面发生了什么变化,因此作者转向详细的计算机模拟。他们从一种由 SAA1.1 构成的致病小鼠 AA 纤维的高分辨率结构出发,计算性地替换为 SAA1.5 和 SAA2.2 的序列。当在接近生理体温的水环境中模拟这些纤维时,以 SAA1.1 为基础的模型保持了出奇的稳定性。相反,由 SAA1.5 或 SAA2.2 构建的纤维发生了移动和扭曲。核心中的一个关键环区向外移动并松开了与蛋白起始片段的接触,若干侧链翻转到了新的取向。这些细微的重排破坏了定义该致病折叠的紧密堆积。换言之,变体序列并不介意一般性的纤维形成——但它们无法舒适地契合致病 AA 纤维的蓝图。
自然设计如何提示未来疗法
综合来看,这项工作表明“抗淀粉样”小鼠品系受保护并非因为它们的 SAA 完全不能聚集。相反,它们的 SAA 变体在结构上不兼容导致系统性 AA 淀粉样变性的那一种特定纤维形态。这些蛋白仍然可以聚集,但它们以替代的、看似无害的形式聚合。类似的保护性突变在其他蛋白质错误折叠疾病中也有报道,包括某些朊病毒和阿尔茨海默病例。这提示了一个更广泛的原则:对易患病的蛋白进行微调,使其无法采用有毒的结构——同时仍能正常发挥功能——或许足以防止疾病。长远来看,受这些天然“抗性”变体启发的疗法,或由其衍生出的短片段,可能有助于将蛋白质引导离开有害折叠,转向无害构象。
引用: Moderer, T., Schnell, A.F., Scheurmann, N.J. et al. Assessment of the biochemical basis underlying the resistance against systemic amyloidosis. Sci Rep 16, 1313 (2026). https://doi.org/10.1038/s41598-026-35297-9
关键词: AA 淀粉样变性, 血清淀粉样蛋白 A, 蛋白质错误折叠, 淀粉样抗性, 小鼠模型