Clear Sky Science · zh
聚己内酯纳米粒子沉淀的建模与实验验证
微小塑料球为何与医学息息相关
想象把一种强效药物装进一个小到能穿过血管、并在需要处精确释放货物的微粒里。这类微粒称为聚合物纳米粒子,是许多新型治疗和成像工具的核心。但要把它们做成尺寸合适且可重复的形态却出奇地难。本研究展示了一个基于物理的简单计算模型,如何预测并调控一种常用可生物降解纳米粒子(聚己内酯,PCL)的尺寸,这有可能为新纳米药物的开发节省多年反复试错的时间。
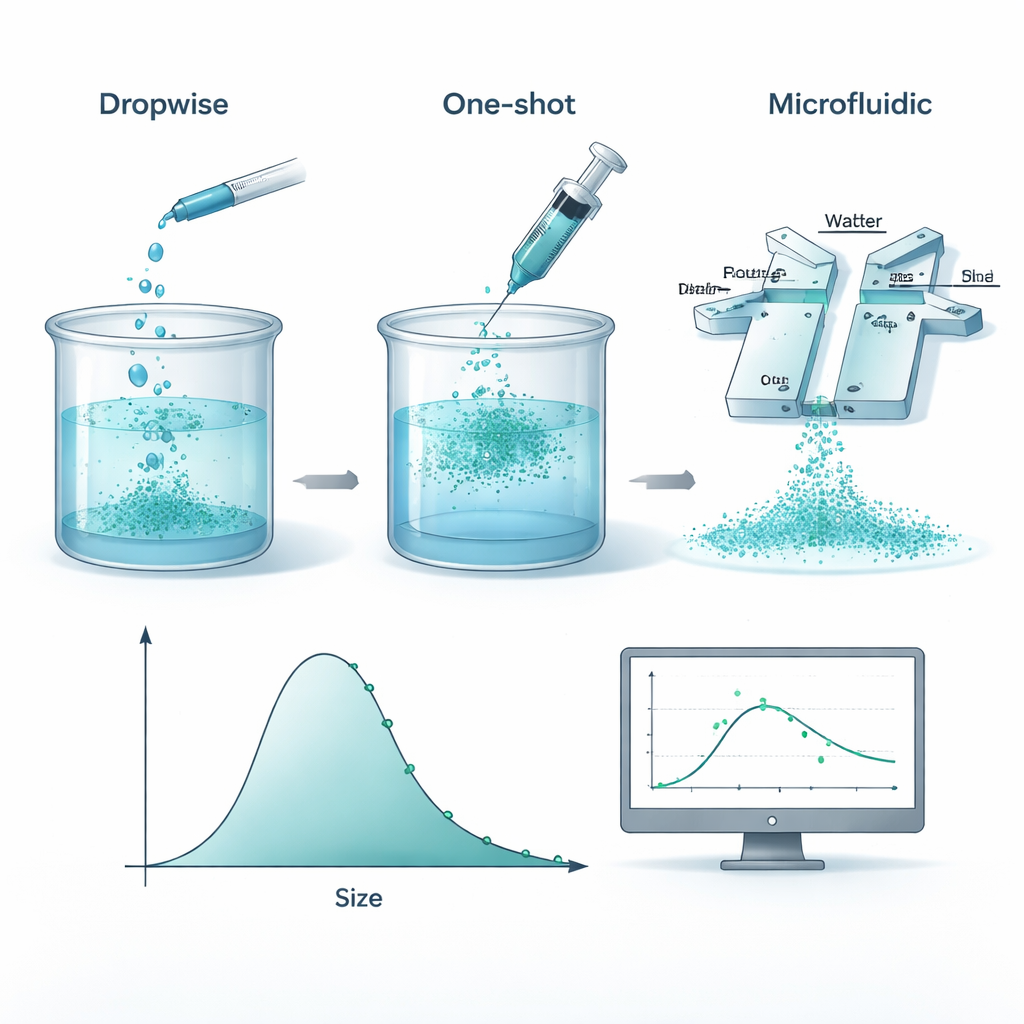
从厨房搅拌到实验室精准
为了制造这些纳米粒子,研究人员把一种可降解塑料聚己内酯溶解在有机溶剂中,然后与水混合,使聚合物“从溶液中析出”并形成微小球状体。团队比较了三种常用的制备方式:缓慢滴加聚合物溶液、一次性倒入,以及将两种液体通过微流控芯片在窄通道中汇合。在受控条件下,三种方法得到的粒子在平均尺寸和尺寸分布上都非常相近。这表明,在所研究的范围内,比起具体的混合装置,更关键的是投入的成分——聚合物和稳定剂的量——而不是如何搅拌。
黏度与助剂如何塑造颗粒
研究人员接着探讨了配方成分如何控制最终粒径。增加有机相中PCL的含量会使该液体变得更稠,也就是粘度增加。可以把它想象成往水里混糖浆而不是果汁:更稠的液体在混合时会分裂成更大的液滴。在这里,较高粘度的聚合物溶液导致了更大的纳米粒子并且尺寸分布略微变宽。加入第二种溶剂乙醇可以在非常高的聚合物浓度下保持工艺稳定,但代价是在高浓度范围内产生更大的粒子。第二种成分,名为Pluronic F‑127的表面活性剂,起到分子级的防粘作用。在低表面活性剂浓度下,颗粒易相互碰撞并粘连,从而增大且均一性下降。随着表面活性剂浓度增加,它会包覆颗粒表面,阻止它们融合,产生更小、更稳定的纳米粒子——但超过某一程度后,进一步提高浓度带来的改善有限,且尺寸分布可能变得更为混合。
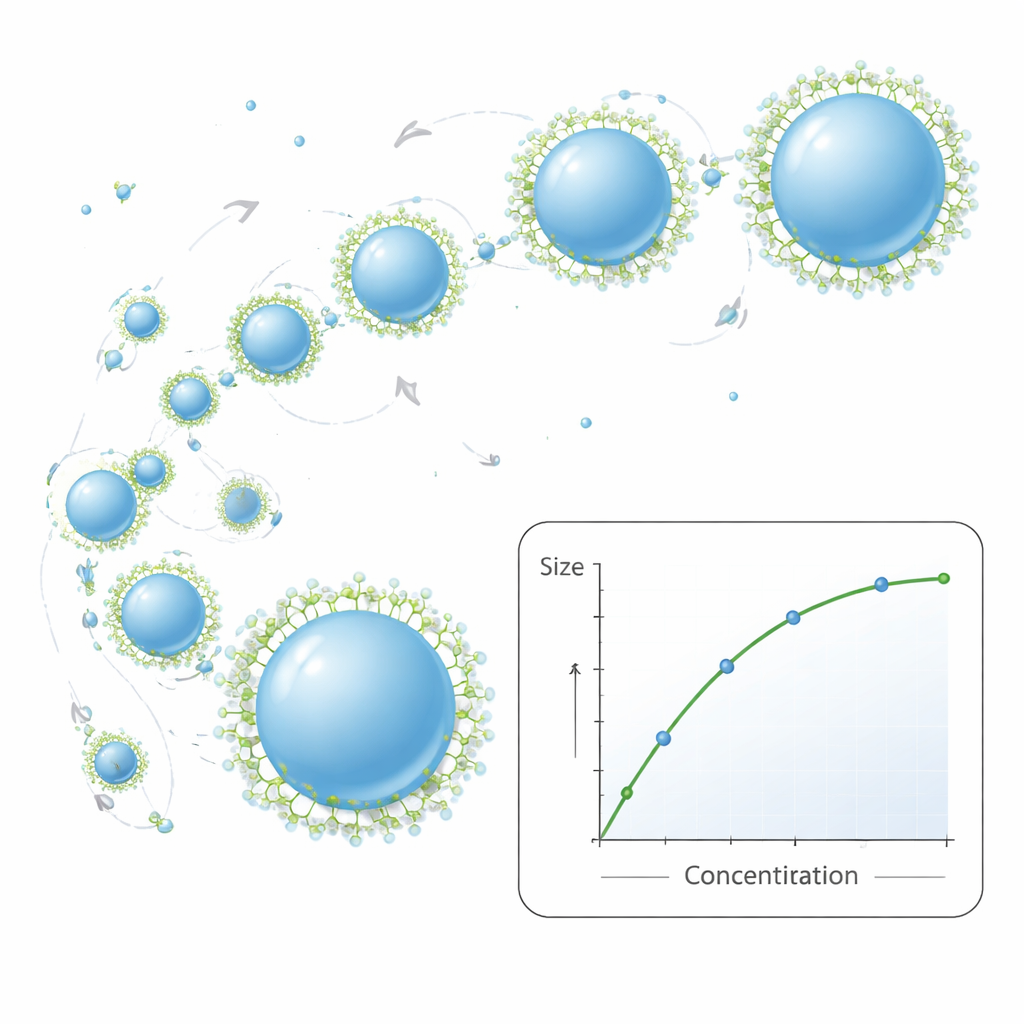
与现实相符的简单生长规则
这项工作的核心是一种紧凑的数学模型,用于描述纳米粒子在首次出现后如何生长。模型将它们的运动视为在液体中的随机抖动,碰撞有时会导致两个颗粒融合成更大的颗粒。先前的模型假定粒子一旦相遇就立刻合并并成为完美球体。新模型加入了两个更现实的因素:首先,它允许两个接触粒子从拉长的形状放松为单一球体需要有限时间;其次,它允许表面活性剂分子逐步“封堵”表面,从而减缓或停止进一步融合。仅用少数可测量的输入参数——如温度、液体粘度和初始聚合物浓度——模型就能预测平均粒径随配方条件的变化。在大量实验中,模型预测的粒径与光散射测得的值高度一致,同时也捕捉到了尺寸分布变宽的总体趋势。
把模型当作设计工具
为了检验该方法的实用性,团队反过来提出问题:不是让模型去解释已有数据,而是让它建议应如何配方以得到三种特定的纳米粒子尺寸和均一度。他们随后在实验室制备了这些“设计”配方。测得的粒子直径与目标值的偏差仅为1–7%——完全在典型实验变异范围内——表明该模型可以可靠地指导配方选择。对尺寸分布宽窄的预测不如直径精确,但仍足以区分相对紧致与更分散的粒群。与那些追踪每个分子或每个流动涡旋的重型模拟方法相比,这种简化模型能在普通计算机上快速运行,且易于推广到其他聚合物和加工体系。
这对未来纳米药物意味着什么
对非专业读者来说,关键信息是:制备有用的纳米粒子不再必须完全依赖于耗时的实验反复。通过把小塑料液滴如何运动、碰撞以及受到表面活性剂保护的基本物理过程纳入模型,这项工作提供了一张从配方选择——聚合物用量、溶剂配比、稳定剂用量——到最终粒径的实用“地图”。由于PCL是一种在药物递送、植入物和造影剂中常用的可降解材料,这个模型可能帮助研究人员更快、更节省材料地设计更安全、更有效的纳米药物。同样的原理可以推广到其他聚合物,为纳米级疗法领域带来更多可预测性和效率。
引用: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
关键词: 聚合物纳米粒子, 纳米沉淀, 药物递送, 数值建模, 聚己内酯