Clear Sky Science · zh
锌稳态受扰会降低正常细胞与肿瘤细胞的组蛋白乙酰化水平
当一种有益金属变得有害
锌常被认为是复合维生素中有助于免疫系统和伤口愈合的营养素。但在细胞内部,锌必须维持在极窄的“正好”范围内。本研究表明,当细胞内锌水平过高时,可能悄然关闭重要基因,通过收紧DNA的包装方式,并且促使细胞走向一种称为自噬的自我清理过程。因为锌补充剂、防头皮屑成分和一些实验性抗癌药物都能改变锌水平,理解这一隐蔽的控制机制对日常健康和未来疗法都有重要意义。
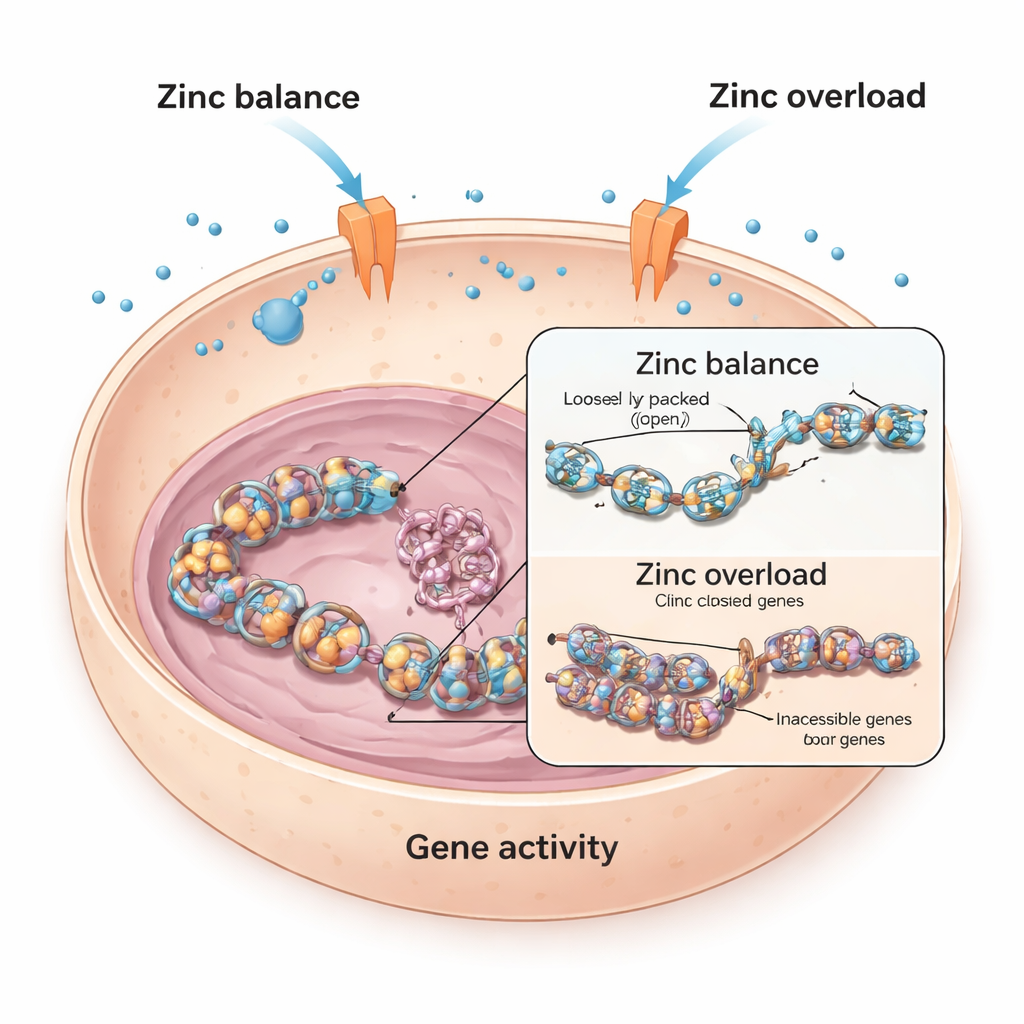
活细胞中平衡锌含量
每个细胞都依赖锌,锌帮助数千种蛋白质发挥作用。为避免缺乏或过载,细胞使用位于膜上的特殊“阀门”,即锌转运蛋白,来调节锌的进出。研究者以小鼠和人类的心肌细胞为起点,探究当这些细胞暴露于额外锌时会发生什么。他们发现,在小鼠心肌细胞中,高锌水平显著降低了一个关键心脏相关基因Bmp4的活性,该基因参与指导心脏发育与功能。相比之下,人类心肌细胞受影响要小得多,暗示不同细胞在防御锌过载方面存在差异性策略。
锌如何收紧DNA的包装
为揭示锌如何沉默像Bmp4这样的基因,团队考察了组蛋白——DNA缠绕其上的线轴样蛋白。当小的化学标记(称为乙酰基)加到组蛋白上时,DNA会变得更松散、更易被读取;当这些标记被去除时,DNA会更紧密地包装,基因更难被激活。研究显示,小鼠心肌细胞中过量锌会导致组蛋白在特定位点(称为H3K9)的乙酰化下降,这与Bmp4活性下降紧密相关。阻断组蛋白去乙酰化酶的药物能够扭转锌的影响并恢复Bmp4表达,表明锌是在倾斜这一化学标记系统的平衡。
内部细胞锌过多,而非仅外部
关键步骤是细胞内水相质中的锌增加,而不仅仅是周围培养液的锌。研究者使用一种在遇到自由锌时会发光的荧光探针,观察到在处理后小鼠心肌细胞内部锌激增。当他们使用一种锌搬运分子将锌直接送入细胞时,即使外部介质中锌远低于先前水平,也观察到了相同的组蛋白乙酰化和基因活性下降。相比之下,人类心肌细胞的膜上转运器反应迅速:一些锌进口通道关闭,出口通道上调,从而防止细胞内锌大幅上升并保护组蛋白乙酰化。小鼠心肌细胞则表现出更“接线错误”的转运反应,允许更多锌涌入并扰乱基因调控。
从基因控制到正常细胞与肿瘤细胞的自我清理
研究者接着询问,这种由锌驱动的DNA包装收紧是否仅限于心肌细胞。他们测试了数种正常人类细胞类型和来自胃、子宫与卵巢的肿瘤细胞株。当借助搬运分子允许锌在细胞内积累时,几乎所有这些细胞都显示出明显的组蛋白乙酰化下降。在一些肿瘤细胞(如胃癌细胞)中,这种变化在特别低的锌剂量下就会发生,暗示某些癌症对锌失衡格外敏感。团队还将乙酰化降低与自噬联系起来——自噬是细胞回收损耗部件的过程。适度的细胞内锌增加促进了自噬,但极高的锌最终会削弱自噬,表明存在一个狭窄的窗口,可用于精细调节这一自清理通路。
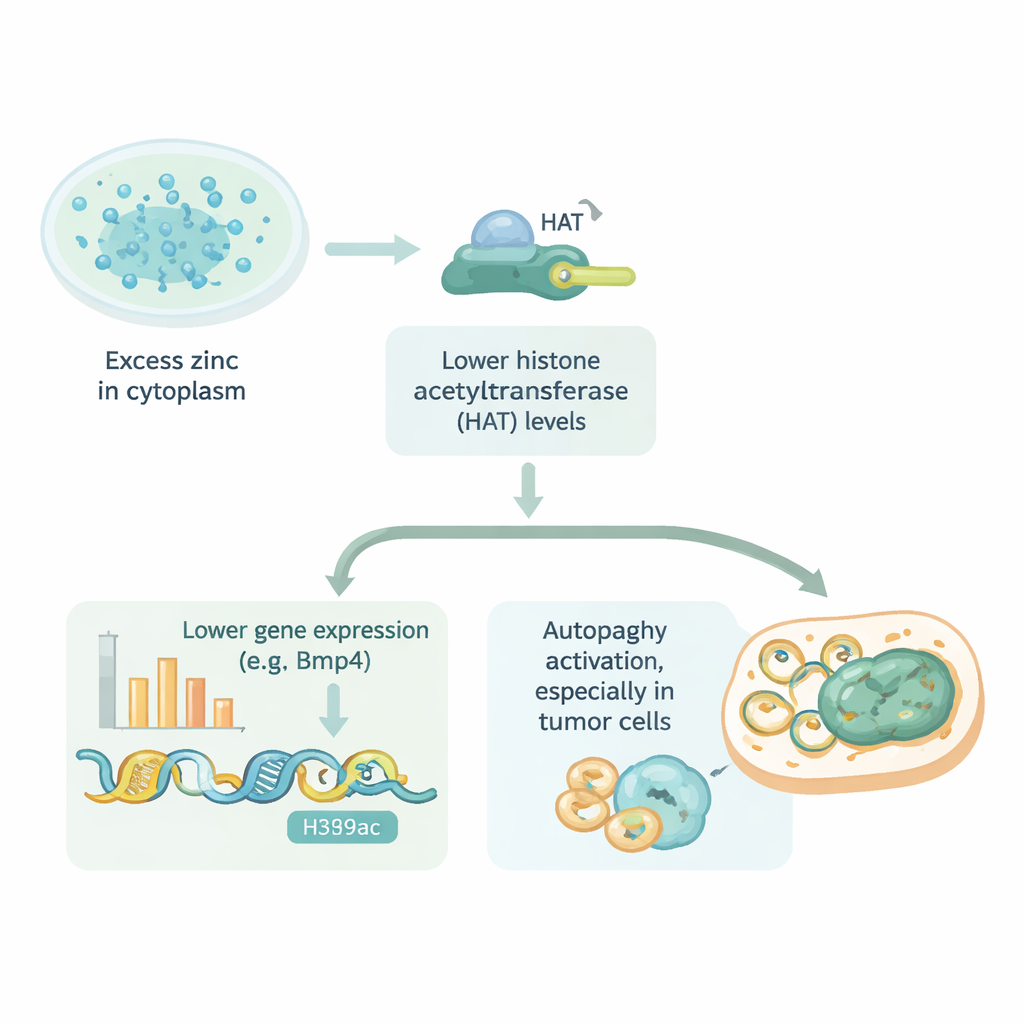
这对健康与治疗意味着什么
简言之,这项工作揭示了细胞内过多的锌可以通过使DNA更难接近来压低基因表达,并且同一路径还能影响细胞自我清理的活跃程度。这一效应并非局限于心肌细胞;在多种正常细胞与癌细胞中均可见,尽管有些细胞更善于防御锌过载。这些见解提示,位于细胞膜上的微小锌转运“阀门”可能是有前景的药物靶点——既可用于保护健康组织免受锌相关损伤,也可用于促使脆弱的肿瘤细胞走向死亡。尽管这些发现来自细胞培养实验,但它们为理解一种日常营养素在其微妙平衡被打破时如何影响基因活性与疾病提供了新的视角。
引用: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
关键词: 锌稳态, 基因调控, 组蛋白乙酰化, 自噬, 癌细胞