Clear Sky Science · zh
缺失Snhg5在小鼠多囊肾病模型中扰乱细胞周期调控但不改变囊肿形成
为何这个带奇怪名字的肾基因重要
多囊肾病(PKD)是一种常见的遗传性疾病,数不清的充液囊泡会逐步占据肾脏,常导致肾功能衰竭。科学家已知两个基因PKD1和PKD2的缺陷推动该病,但许多其他基因因素可能影响疾病进展的速度。本研究聚焦于一种不常见的基因类型——长非编码RNA,名为Snhg5,提出一个简单但重要的问题:这种分子是否实质性地影响PKD的发展,还是主要充当旁观者?
对这一鲜为人知的遗传信使的更深入观察
与提供蛋白质蓝图的典型基因不同,长非编码RNA更像细胞内的分子组织者或开关。早期研究显示Snhg5在小鼠PKD模型中显著上调,并且与若干癌症和肾损伤有关,提示其可能推动有害增生。研究人员首先绘制了Snhg5在正常小鼠中的时空表达图谱。他们发现该基因在多种器官中被激活,肠道表达尤为丰富,并且在出生后肾脏中的活性迅速下降,随着器官从快速生长期转向更稳定的成熟状态。在肾细胞内,几乎所有Snhg5分子都位于细胞核——存放DNA的指挥中心,表明Snhg5更可能通过调控基因活性发挥作用,而非直接合成蛋白质。
病变肾脏中的表达模式并不说明全部
团队随后比较了多种小鼠PKD模型中Snhg5的水平。在进展迅速的模型中,囊肿形成迅速,患病肾脏中Snhg5增加了2到3倍,单细胞成像显示囊壁细胞和邻近组织中存在强烈的核信号。出乎意料的是,在更缓慢、更温和、能更好模拟人类PKD长期过程的模型中,Snhg5并未上调。更令人惊讶的是,在人类晚期常染色体显性PKD的肾脏组织中,该基因的人类同源物SNHG5反而减少了90%以上。这些结果共同表明,该RNA的变化伴随囊肿形成,但变化的方向和时机在物种与疾病阶段之间存在差异,从而对Snhg5是否单独作为囊肿生长的明确驱动因素提出质疑。
当该基因被删除会发生什么
为了超越相关性,研究人员使用CRISPR基因编辑在小鼠中完全敲除Snhg5,建立了全身性“敲除”系。与担忧删除如此显著改变的分子可能有害相反,缺失Snhg5的小鼠按正常比率出生、寿命正常,肾脏在外观和功能上与健康同窝鼠相似。显微镜下检查显示肾脏结构正常,无明显瘢痕或炎症,血液检测也未见肾小球滤过功能受损的迹象。然而在分子水平上出现了更细微的变化:缺失Snhg5的鼠肾以及体外培养的肾小管细胞在与细胞分裂和DNA复制相关的基因活性上显示出一致性变化。在细胞培养中,更多细胞在细胞周期晚期滞留并进入受损的亚G1状态。特别是一个名为ARPC5的蛋白——参与通过重排细胞内支架帮助细胞分裂的复合体,在Snhg5缺失时减少,提示可能存在一条因果链。
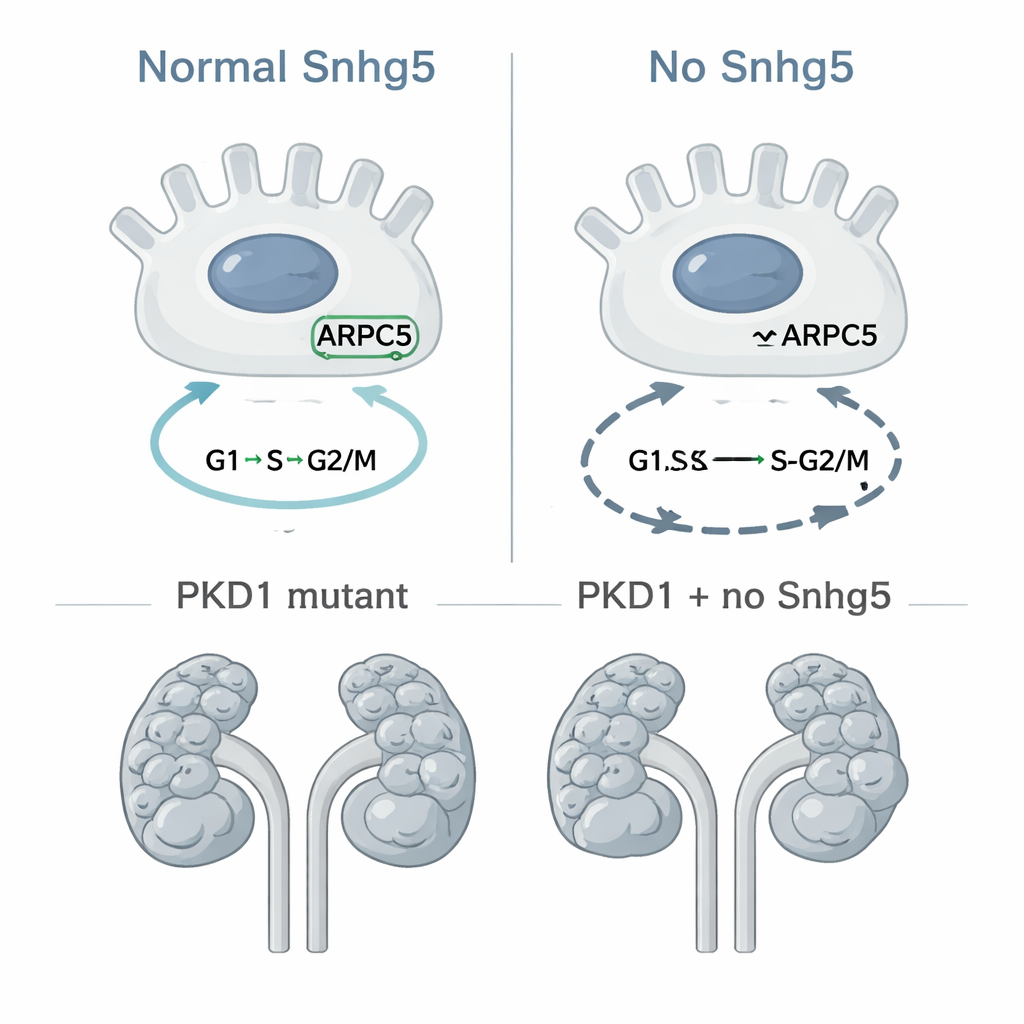
直接测试其对囊肿生长的作用
由于失控的细胞分裂是PKD的核心特征之一,研究团队接着探问在一个成熟的模型中去除Snhg5是否会减缓囊肿形成——该模型在集合管细胞中选择性敲除PKD1,集合管是许多囊肿的来源。他们交配得到一些仅携带PKD1突变的小鼠,另一些同时缺失PKD1和Snhg5。当在出生10天时检查动物,两个组都表现出严重的囊性肾改变,对肾脏大小、囊肿面积及囊肿数量的精确测量显示,删除Snhg5并未带来显著保护。若有差异,双突变小鼠的囊肿负担反而略多,但差异很小且无统计学意义。换言之,尽管Snhg5影响肾细胞的细胞周期基因,其缺失在这一特定的PKD模型中并未明显改变囊肿出现或扩大的速度。
对未来治疗的意义
对患者和药物开发者而言,主要结论是:尽管Snhg5在小鼠PKD中是最显著改变的遗传信号之一,但在集合管来源的疾病早期快速生长期中,它并非囊肿形成的关键枢纽。该基因确实似乎微调肾细胞通过分裂周期的方式,可能通过影响像ARPC5这样的因子,但这种影响足够微妙,以致其完全丧失并未显著改变肾发育和早期PKD进展。这些发现强调了一个更广泛的教训:并非组织中每一种显著的分子变化都是有前景的治疗靶点。在将像Snhg5这样的长非编码RNA作为药物候选前,需要在多种疾病模型和不同时点上进行严格的因果性检验。}
引用: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
关键词: 多囊肾病, 长非编码RNA, Snhg5, 细胞周期, 肾囊肿