Clear Sky Science · zh
壳聚糖-硫酸右旋糖酐纳米胶囊提高替加环素对非伤寒沙门氏菌的疗效
这对食品安全为何重要
大多数人知道沙门氏菌会引起严重的食物中毒,常与未煮熟的家禽有关。但较少人意识到,某些菌株已对多种抗生素产生耐药,甚至强效的“最后防线”药物也可能失效。本研究探讨了一种基于纳米技术的方法,通过将替加环素封装进微小的糖类胶囊,帮助其进入受感染细胞并抑制沙门氏菌的关键耐药机制,从而挽救该药的效力。
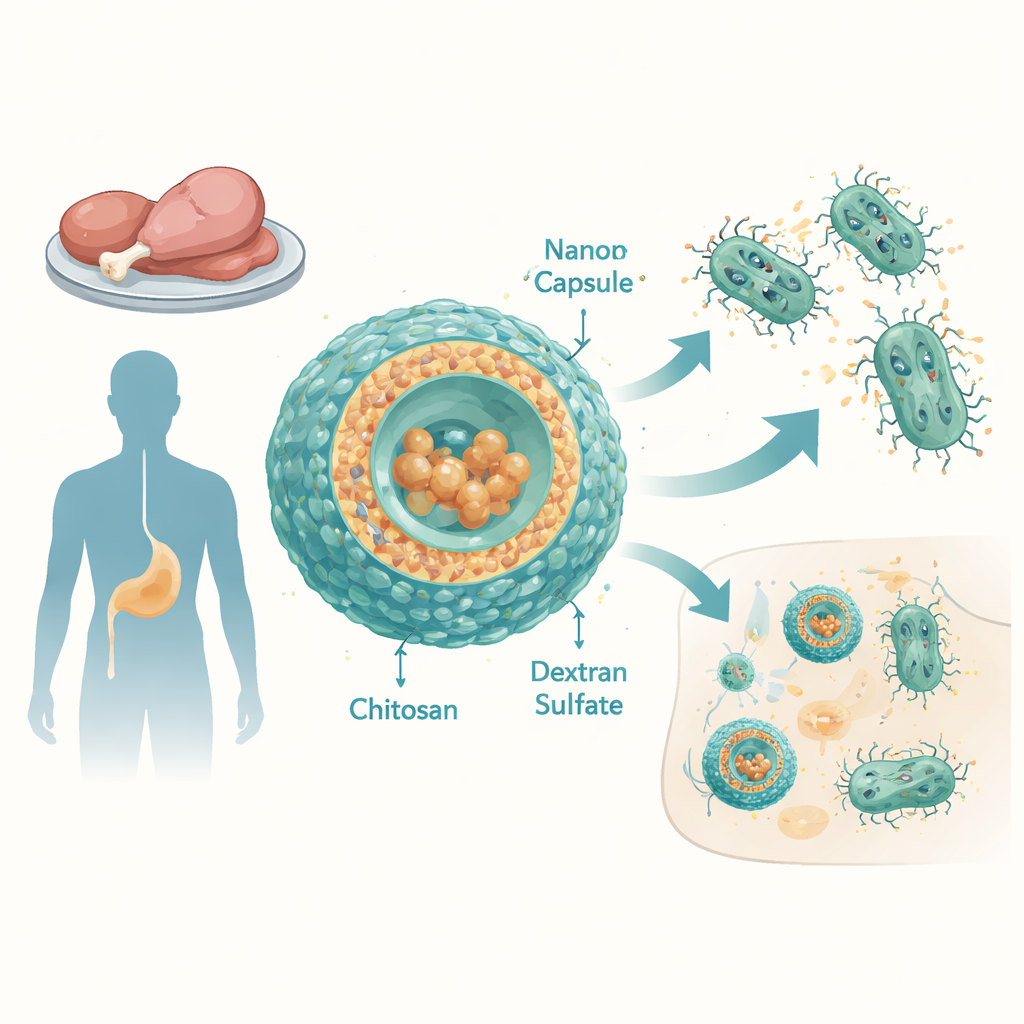
来自顽固沙门氏菌的日益威胁
非伤寒沙门氏菌(NTS)血清型是全球腹泻和血流感染的主要病因,尤其在中低收入国家更为常见。研究人员检测了来自埃及鸡鸭肉的12株沙门氏菌肠炎沙门氏菌。这些菌株对多种常用抗生素表现出耐药,包括青霉素类、头孢类、四环素类等,且多重耐药评分较高。即便是作为疑难病例保留用的广谱药替加环素也效果不佳:菌株能够耐受极高浓度的该药。一个主要原因是“外排泵”过度活跃——这些位于细菌膜上的分子机器不断将抗生素泵出细胞。
构建更智能的药物胶囊
为了解决这一问题,研究团队设计了由两种天然来源聚合物构成的纳米级胶囊:壳聚糖(从壳质素获得,存在于甲壳类外壳)和硫酸右旋糖酐(一种支链糖分子)。通过精细调整这些成分的比例,他们制备了直径约100–150纳米、带正电表面的稳定颗粒,这种正电有助于与细菌和宿主细胞膜相互作用。替加环素以极高的效率装载进这些颗粒——几乎所有药物都被封装在胶囊内。在模拟血流条件的体外测试中,胶囊在数小时内释放出大部分替加环素,表明它们可在感染部位释放出强效药物剂量。
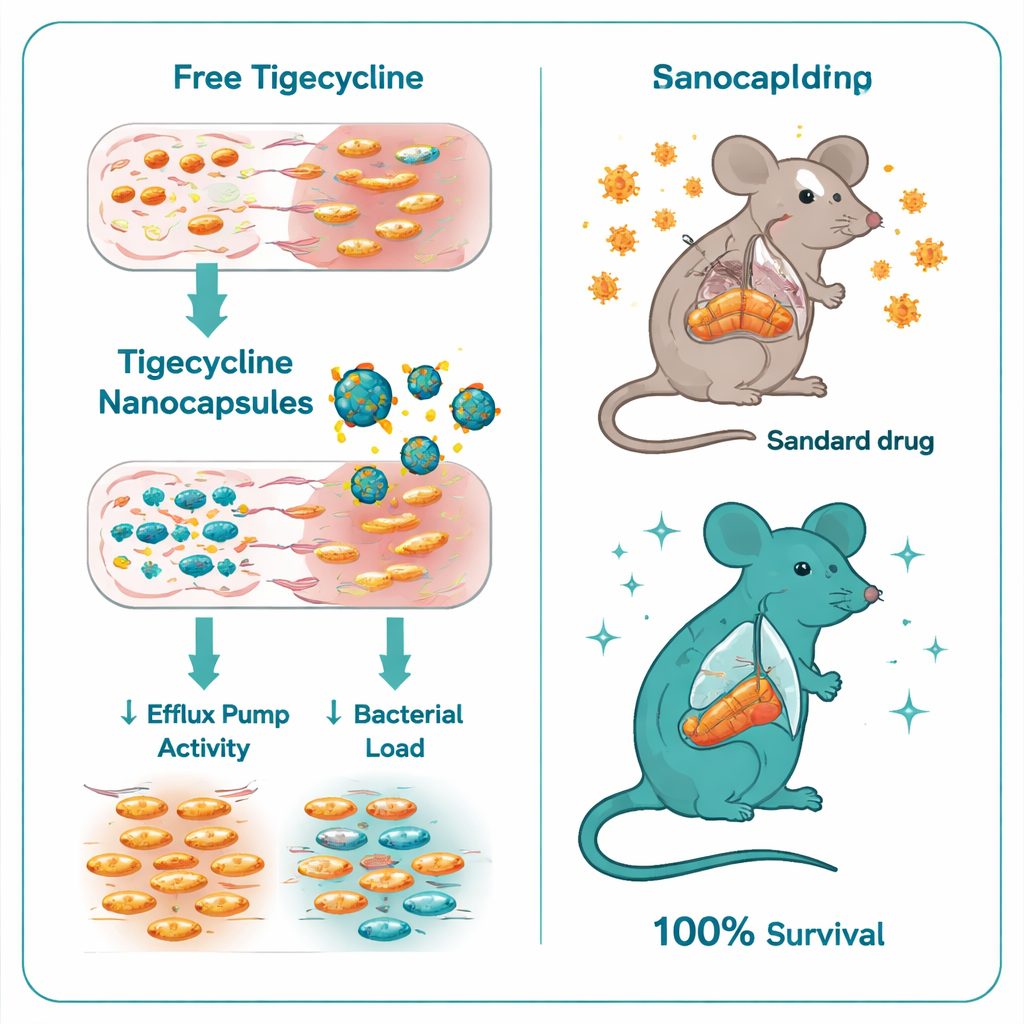
削弱细菌防御
将普通替加环素与壳聚糖–硫酸右旋糖酐负载的替加环素纳米胶囊比较,差异显著。抑制细菌生长所需的最低药物浓度(MIC)从普通替加环素的32–128微克/毫升降至纳米胶囊的仅0.5–1微克/毫升——提高了约6至7倍。时间杀菌实验显示,封装形式对沙门氏菌的杀灭更迅速、更彻底。在基因水平上,纳米胶囊还能抑制关键耐药调控基因:ramA和acrB基因的表达在处理后的细菌中下降了数倍,这些基因参与调控和构成主要外排泵。换言之,胶囊不仅递送了更多药物,还帮助关闭了细菌的一条主要逃逸通路。
保护感染小鼠免于致死性疾病
随后团队在小鼠严重沙门氏菌鼠伤寒沙门氏菌感染模型中测试了该新制剂。未治疗的感染小鼠在八天内全部死亡。接受常规替加环素治疗的小鼠情况有所改善但仍有高死亡率,仅有40%存活。形成鲜明对比的是,所有接受替加环素负载纳米胶囊治疗的小鼠全部存活。这些动物的肝脏和肠道细菌明显减少,血液检查显示肝肾功能接近正常,显微镜下组织损伤也明显减轻。即便是“空载”的壳聚糖–硫酸右旋糖酐胶囊(不含抗生素)也提供了一定保护,可能因为壳聚糖本身具有温和的抗菌和抗炎作用,但与替加环素结合的效果明显更佳。
这对未来治疗可能意味着什么
对非专业读者而言,核心信息是:将现有抗生素封装在智能、生物相容的纳米胶囊中,可以恢复其对高度耐药沙门氏菌的效力。通过帮助药物到达潜藏在细胞内部的细菌并降低通常会将药物泵出的外排泵活性,壳聚糖–硫酸右旋糖酐系统把一个濒临失效的最后防线抗生素转变为在小鼠中高度有效的疗法,实现了100%的生存率。虽然在将此方法应用于人类或农场动物之前仍需更多工作,但它为延长重要抗生素的可用寿命、提高食品安全提供了一条有希望的途径,而无需从头发明全新的药物。
引用: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
关键词: 沙门氏菌, 抗生素耐药性, 纳米颗粒, 药物递送, 替加环素