Clear Sky Science · zh
DNA 修复基因 XRCC1 的遗传多态性与糖尿病性多发性神经病的风险
为什么微小的 DNA 变化对糖尿病患者很重要
对于许多 2 型糖尿病患者,首个危险信号往往不是化验单上的高血糖,而是双脚或双手的刺痛、灼热或麻木。这种被称为糖尿病性多发性神经病的情况,可能导致疼痛、平衡丧失,甚至截肢。然而,并非所有糖尿病患者都会发生这种并发症,即便他们的血糖指标相近。本研究提出了一个简单但影响深远的问题:遗传性的小差异,尤其是 DNA 修复基因中的变异,能否解释谁更容易罹患神经病?现代数据科学是否能帮助医生更早发现这些高风险人群?
更细致地看糖尿病中的神经损伤
糖尿病性多发性神经病是由于长程神经(尤指腿和足部)在多年高血糖、血流不良以及持续性活性氧分子造成的“氧化损伤”下逐步受损而产生的。这些活性氧会损害细胞的关键成分,包括 DNA。细胞并非无能为力:它们携带着不断修补这类损伤的修复工具。其中一种工具是由 XRCC1 基因编码的蛋白,参与修复 DNA 的单链断裂。如果这一修复系统功能欠佳,神经细胞在糖尿病的持续应激下可能更难存活,从而增加并加重神经损伤的风险。
研究者在埃及患者中检验了什么
研究团队招募了 732 名埃及成年人:其中 503 人为 2 型糖尿病患者,229 人为健康志愿者。在糖尿病组中,大约一半已出现神经损伤,另一半未出现。科学家们关注 XRCC1 基因的两个常见“拼写差异”,即 Arg399Gln 和 Arg194Trp。这些微小变化称为单核苷酸多态性,会将 XRCC1 蛋白的某一氨基酸替换为另一种,可能改变其修复 DNA 的效率。研究者采用常规的血液基因检测,确定每位受试者在这两个位点上的基因型,并将这些基因型与神经问题的存在及严重程度进行比较。
与更高神经风险相关的遗传模式
结果显示出明确的规律。携带 XRCC1 不常见等位型的人——在 399 位点为 A 型、在 194 位点为 T 型——比携带常见等位型的人更容易发生神经损伤。具体而言,在 399 位点携带两个 A 等位基因的个体,比携带两个 G 等位基因者的神经病发生几率高数倍,即便在校正了年龄、性别和吸烟等因素后仍然如此。同样,在 194 位点至少有一个 T 等位基因也会提高风险。当把这两个位点作为单体型(haplotype)共同考虑时,A–T 组合尤其与神经疾病相关,而其它组合即便带有一个风险字母,反而显示出一定保护作用,提示可能存在更复杂的基因间互作。
机器学习如何使图景更清晰
为了超越简单的比较,研究者使用了机器学习——一种能够同时筛选多种变量的人工智能方法。采用随机森林(Random Forest)和 XGBoost 算法,他们在 80% 的数据上训练模型,并在剩余数据上进行测试。这些模型不仅突出了 XRCC1 的变体,还将传统临床因素列为神经病的关键预测因子,例如更长的糖尿病病程、更高的空腹血糖与“坏”LDL 胆固醇、更低的“好”HDL 胆固醇、较高的年龄和更高的体重指数。一个名为 SHAP 的解释工具帮助可视化每个因素如何推动个体患者的风险上升或下降。研究组还比较了两种床边神经损伤评分系统,发现多伦多临床神经病评分(Toronto Clinical Neuropathy Score)比旧的残疾评分更能反映疾病严重程度。
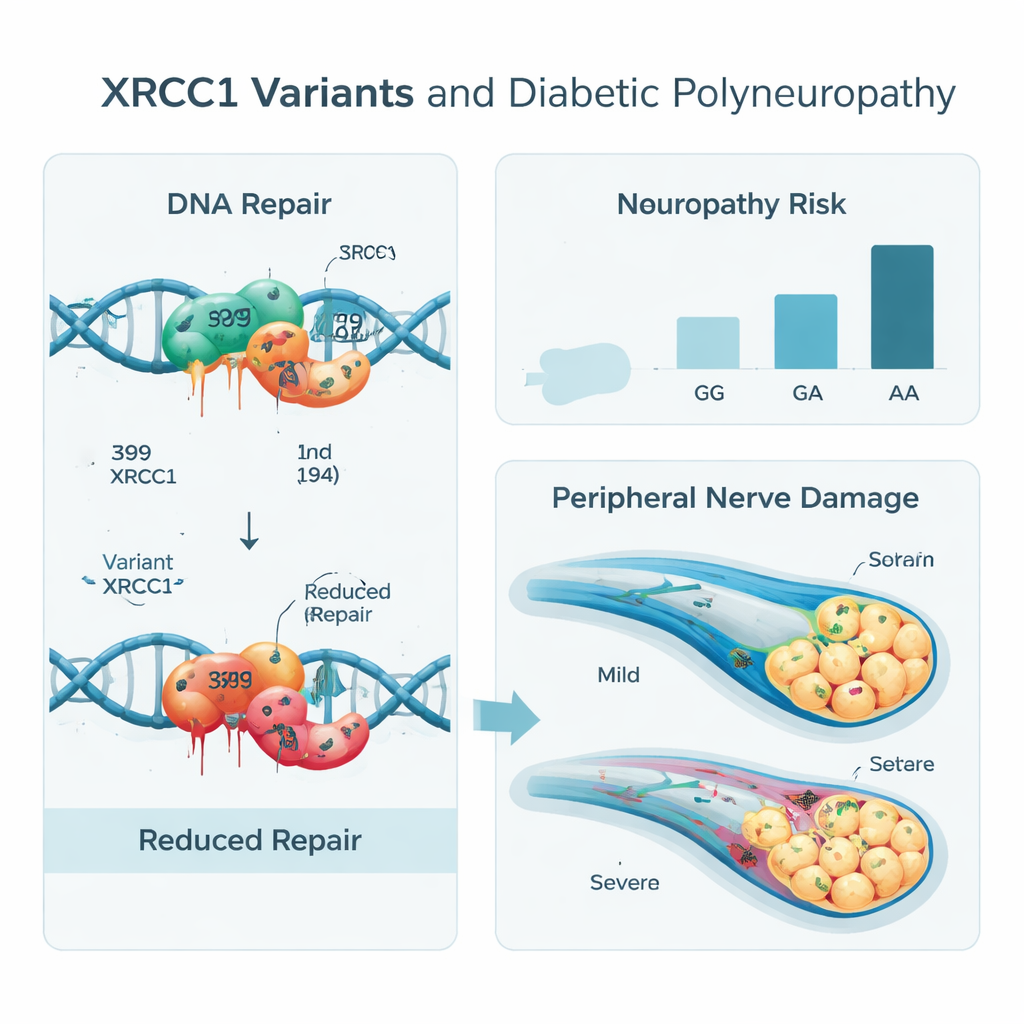
这对患者与预防意味着什么
简而言之,研究表明部分 2 型糖尿病患者天生携带较弱的 DNA 修复“工具包”,使其神经更易在高血糖与异常血脂的长期影响下受损。XRCC1 基因的这些遗传差异似乎并不导致糖尿病本身,但在糖尿病存在的情况下,会增加发生疼痛性和致残性神经并发症的几率。通过将简单的血液检测、临床指标、神经评分工具和遗传信息结合到智能计算模型中,未来医生或可及早识别高风险患者,并在严重神经损伤发生前,针对性地调整随访与治疗——例如严格控制血糖和血脂、改变生活方式以及采用保护神经的治疗措施。
引用: Hashim, N.A., El-Baz, H.A., Afya, Z.I.A. et al. Genetic polymorphisms in DNA repair gene XRCC1 and the risk of diabetic polyneuropathy. Sci Rep 16, 4815 (2026). https://doi.org/10.1038/s41598-026-35213-1
关键词: 糖尿病性神经病, DNA 修复, XRCC1, 遗传风险, 机器学习