Clear Sky Science · zh
REAC RGN-AR 处理调节脂肪组织来源干细胞的脂肪生成分化
为何重塑脂肪细胞很重要
大多数人只把体脂看作多余的体重,但脂肪组织是一个活跃的器官,会与全身交流,并能够保护或损害我们的健康。在肥胖及相关疾病如2型糖尿病中,脂肪细胞常常变得肥大、发炎并在代谢上有害。本研究探索了一种新的非侵入性技术,该技术温和地利用无线电波引导来源于脂肪的干细胞远离形成不健康的“储存型”脂肪细胞,而朝向更具活性、消耗热量的细胞类型。理解并利用这一转变,可能为治疗代谢紊乱和改善组织修复开辟新的途径。
与细胞交流的新方式
我们的身体在脂肪组织中含有能自我更新并分化成多种细胞类型(包括脂肪、骨和软骨)的干细胞。这些脂肪组织来源的干细胞(ADSCs)从常规手术中易于获得,并已经在再生治疗中受到探索。挑战在于,尤其是在代谢问题的个体中,这些细胞倾向于成为普通的白色脂肪细胞,储存大量脂质并助长低度慢性炎症。研究人员测试了一种称为无线电电不对称传导器(Radio Electric Asymmetric Conveyer,REAC)的技术,采用他们称之为 TO RGN-AR 的特定方案,旨在微调细胞自身的电活动。目标是观察这种生物电“调谐”是否能保持干细胞的青春可塑性,同时抑制它们转变为不健康的脂肪细胞。
保持细胞青春与可塑性
在体外实验中,ADSCs 来自无肥胖或糖尿病的成年人体内小块脂肪样本被分离出来。随后这些细胞在通常会促使其成为脂肪细胞的培养条件下生长。一部分培养皿在培养基中放置微小探针接受了为期72小时的 REAC 处理,另一部分则作为未处理的对照。当科学家后来检查基因活性时,发现 REAC 暴露提高了关键“干性”基因——Oct-4、Sox2 和 Nanog 的表达,这些基因有助于细胞保持多能性和自我更新能力。值得注意的是,这种保护效应即便在细胞暴露于强烈促脂诱导条件下仍然持续,表明无线电电处理帮助细胞抵抗单向走向普通脂肪细胞的分化承诺。
远离储存型脂肪的引导
团队还测量了驱动白色脂肪形成的基因,如参与脂肪储存和脂质代谢的 PPAR-γ、LPL 和 ACOT2。在仅以分化培养基处理的细胞中,这些基因显著上调,与向大而富含甘油三酯的脂肪细胞转变一致。相比之下,接受 REAC 处理的细胞这些促脂标记显著下降,而细胞存活或生长并未受到影响。与此同时,与产热且代谢活跃的脂肪相关的基因 UCP1 增加。该模式表明 REAC 并非简单阻断细胞生长;相反,它将发育程序从构建更多储存型脂肪重定向为更具能量消耗特征的身份。
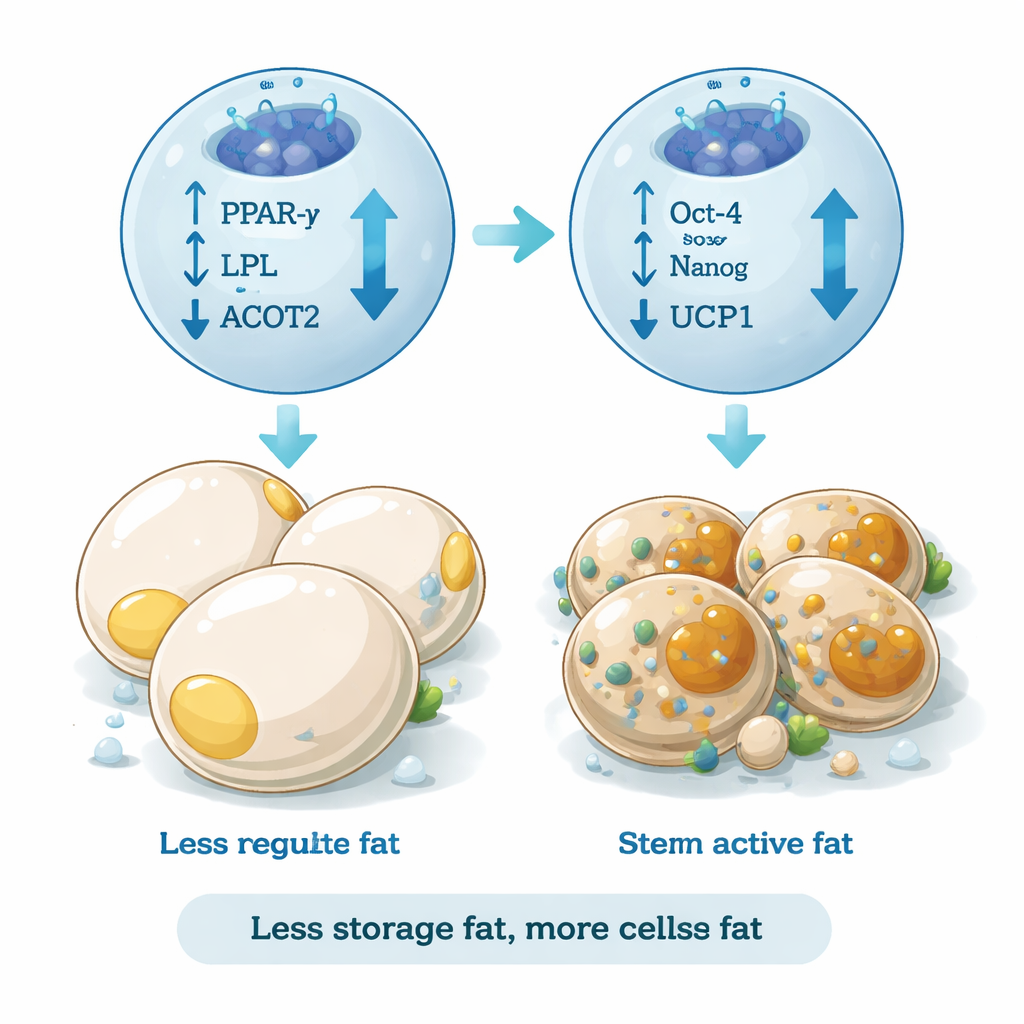
鼓励“良性”脂肪特征
除了基因活性,研究者还检查了细胞的实际形态和表面标志物。通过荧光标记,他们追踪区分不同脂肪细胞类型的蛋白质。自发分化的细胞表达高水平的 ASC-1,这是经典白色脂肪的标志。接受 REAC 处理后,ASC-1 水平下降,而与米色和棕色脂肪相关的标志物(包括 TMEM26 和 PAT2)变得更为显著。米色脂肪细胞尤其引人关注,因为它们可以通过燃烧热量来产热,并倾向于释放抗炎信号。在显微镜下,REAC 处理的培养物也包含更少成熟、充满脂质的脂肪细胞,而保留了更多呈干细胞样形态的细胞,进一步表明朝向更健康、更具可塑性的脂肪谱系发生了转变。
这对未来治疗的可能意义
总体而言,研究结果表明 REAC TO RGN-AR 能温和“引导”脂肪来源的干细胞保持更年轻、避免转变为有害的储存型脂肪细胞,并转而获得米色、代谢活跃脂肪的特征。尽管这些实验是在培养皿中完成而非患者体内,但它们指向一种有前景的策略:使用精细调控的电学信号来恢复脂肪组织的平衡、减轻慢性炎症并支持更好的代谢健康。如果未来在动物和人体研究中证实这些效果,这类非侵入性治疗可作为饮食、运动和药物治疗的补充,以应对与肥胖相关的疾病,并可能提升基于干细胞的再生医学疗法的效果。
引用: Cruciani, S., Rinaldi, S., Fontani, V. et al. REAC RGN-AR treatment modulates adipogenic differentiation in adipose tissue-derived stem cells. Sci Rep 16, 4860 (2026). https://doi.org/10.1038/s41598-026-35204-2
关键词: 脂肪干细胞, 生物电调制, 米色脂肪, 代谢紊乱, 再生医学