Clear Sky Science · zh
整合蛋白质组学与代谢组学揭示植物倍半萜内酯通过耗竭ATP合成并重编程初级代谢抑制三阴性乳腺癌细胞活性
使侵袭性乳腺癌“饿死”的植物化合物
三阴性乳腺癌是最难治疗的乳腺癌类型之一,因为它缺少许多药物可依附的常见激素“靶点”。本研究探索了从一种药用植物中提取的两种分子,它们似乎能关闭这些癌细胞的内部能量站,切断其能量供应,同时较少伤及正常乳腺细胞。弄清其作用机制可能为目前选择有限的患者带来更温和、更具有针对性的治疗路径。
为何瞄准癌细胞的动力源很重要
每个细胞都依赖称为线粒体的微小结构来制造ATP,这是细胞的基本燃料。癌细胞,尤其是侵袭性细胞,通常异常依赖线粒体以支持快速生长、扩散并在压力下生存。研究者聚焦于三阴性乳腺癌细胞——约占乳腺癌的15–20%,且较易复发与转移。他们研究了一种天然分子脱氧象鼻素(deoxyelephantopin, DET)及其改良衍生物DETD‑35,均为来自象牙草属(Elephantopus)的倍半萜内酯。先前工作显示这些化合物会引发氧化应激与非典型的细胞死亡方式,但它们如何扰乱细胞的能量工厂尚不清楚。
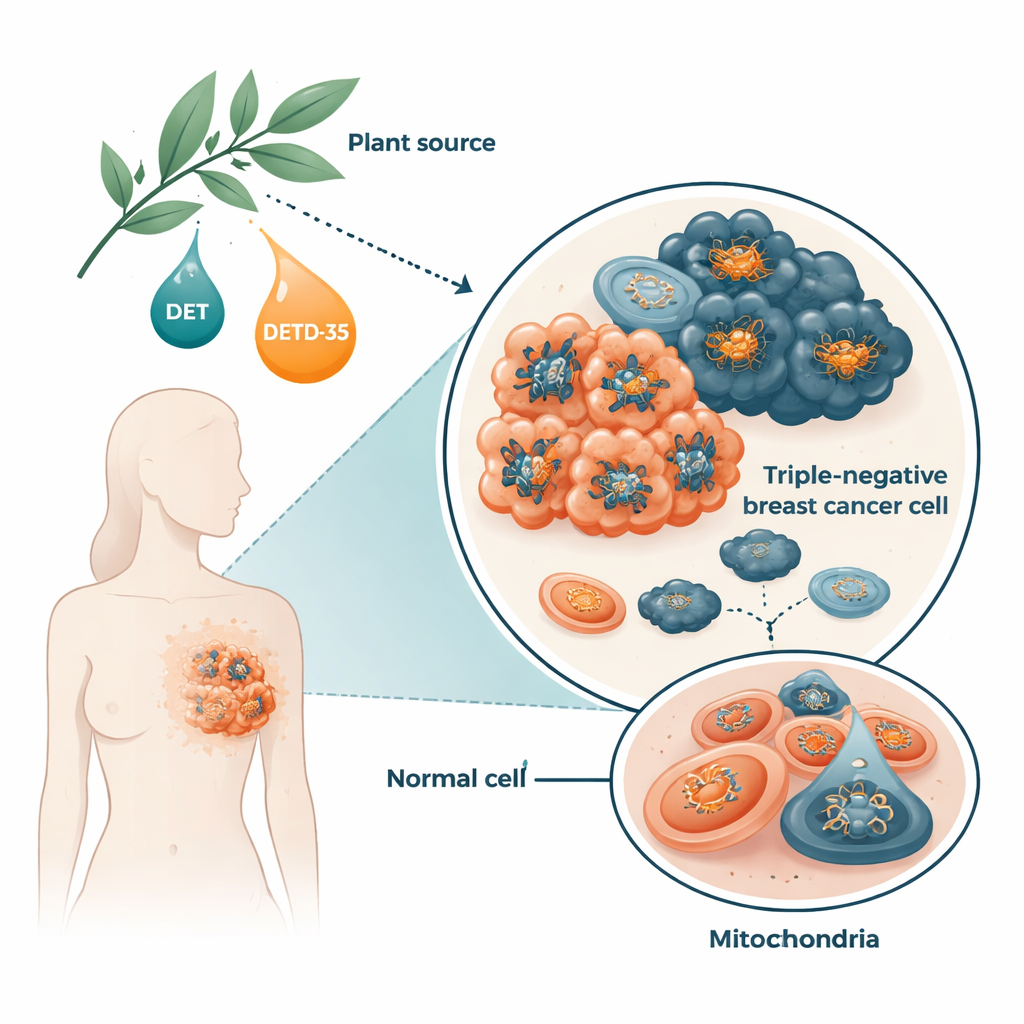
植物分子如何扰乱癌细胞线粒体
在体外培养的人类三阴性乳腺癌细胞中,研究组发现DET与DETD‑35迅速增加了活性氧(reactive oxygen species)的产生,这是一种在能量生成过程中产生的化学“尾气”。细胞对此上调了某些保护性酶类,但不足以恢复稳态。这些化合物还促使线粒体膜上的通道——即通透性转变孔(permeability transition pore)打开,该变化与线粒体肿胀、膜电位丧失和细胞死亡的早期步骤相关。仅数小时内,癌细胞内的ATP水平显著下降。当研究者事先加入抗氧化剂时,这些损伤性效应在很大程度上被逆转,表明氧化应激是该过程的关键环节。
绘制对蛋白质与代谢的损伤图谱
为理解整体情况,科学家将两种强大的组学方法结合起来。他们编目了数千种线粒体蛋白,并比较了处理组与对照组中大量小分子代谢物。该整合视角揭示DET与DETD‑35扰动了参与氧化磷酸化(线粒体制造ATP的主要途径)的蛋白,并激活了与死亡相关的信号通路。与此同时,处理氨基酸、脂质以及DNA合成所需构件的核心代谢通路被重新编程。某些有助于构成线粒体内膜形态的脂类,以及与抗氧化防御和糖类分解相关的分子发生了变化,这些变化与处于应激且能量匮乏的癌细胞一致。关键的是,在相同剂量暴露下,正常乳腺细胞并未出现这些广泛改变,提示对肿瘤细胞存在一定选择性。
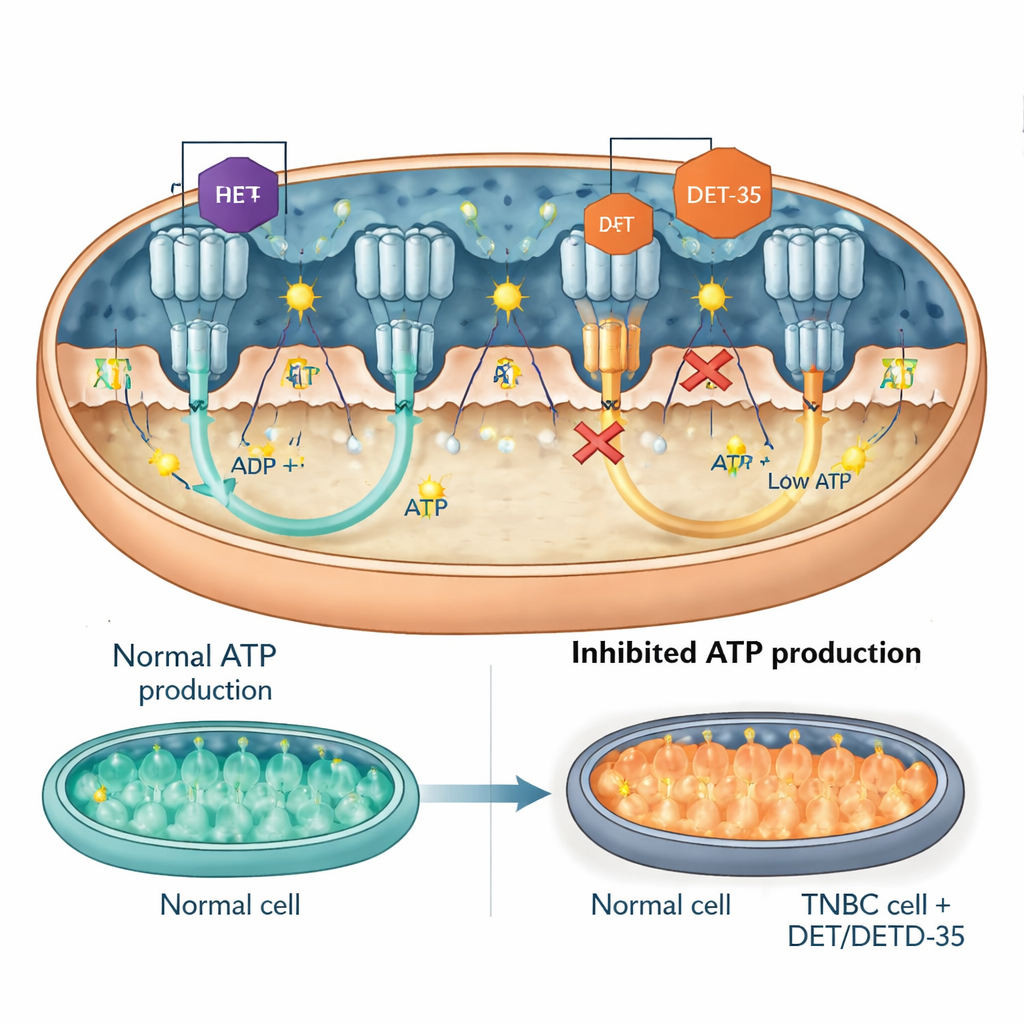
一个关键的信号蛋白与ATP的“涡轮机”本身
随后,团队将目光集中在这些被扰动网络中的特定角色上。其中一个是PRKCA,一种可进入线粒体并影响能量产出与应激反应的信号蛋白。DET与DETD‑35在癌细胞中提高了PRKCA的水平。当研究者用基因学工具降低PRKCA表达时,药物的毒性减弱:癌细胞更有可能存活、产生更多ATP,并且显示出较少的线粒体功能失常与凋亡迹象。另一个焦点是ATP合酶——这个分子“涡轮机”通过旋转产生ATP。测量显示DET与DETD‑35直接降低了癌细胞线粒体中ATP合酶的活性。计算机对接模型提示这两种化合物滞留在该酶的关键界面位置,与已知的ATP合酶抑制剂结合的大致区域相当,物理上妨碍了其转动并削减ATP产出。在携带人源三阴性乳腺肿瘤的小鼠体内,任一化合物处理均降低了肿瘤组织中ATP合酶组分的水平,支持了细胞培养中的发现。
这对未来癌症治疗意味着什么
总体而言,该研究描绘出一个连贯的图景:这些来源于植物的化合物通过使癌细胞承受过量氧化应激、撬开线粒体孔并直接阻滞产ATP的机械装置,迫使三阴性乳腺癌细胞陷入能量危机。随着ATP耗竭和代谢紊乱,癌细胞丧失生长与存活能力,而在相同条件下正常乳腺细胞大体保持完好。对普通读者而言,结论是科学家可能能够利用癌细胞对其内部能量站的高度依赖,借助一些经植物启发、精心设计的小分子来耗尽肿瘤细胞的“电池”,而不切断健康组织的电源。要将此类药物推向临床还需更多工作,但对蛋白质、代谢物与能量流的整合性观察提供了一条有前景的路线图。
引用: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
关键词: 三阴性乳腺癌, 线粒体, ATP合酶, 天然产物, 癌症代谢