Clear Sky Science · zh
乳酸通过调控YTHDF2-FTH1轴促进心肌细胞铁死亡并加重心肌缺血再灌注损伤
为什么心脏病患者应关心这种化学反应
当医生在心脏病发作后重新打通被堵塞的冠状动脉时,新鲜血液的回流既能挽救心肌,也可能造成额外损伤,称为缺血–再灌注损伤。这项研究揭示了心肌细胞内一个出人意料的祸根:常见的代谢副产物乳酸。作者显示乳酸能翻转一个分子开关,使心肌细胞走向一种特定的铁依赖性细胞死亡,从而加重损伤。理解这条被隐藏的通路可能为在急救治疗中更好保护心脏指明新的药物靶点。
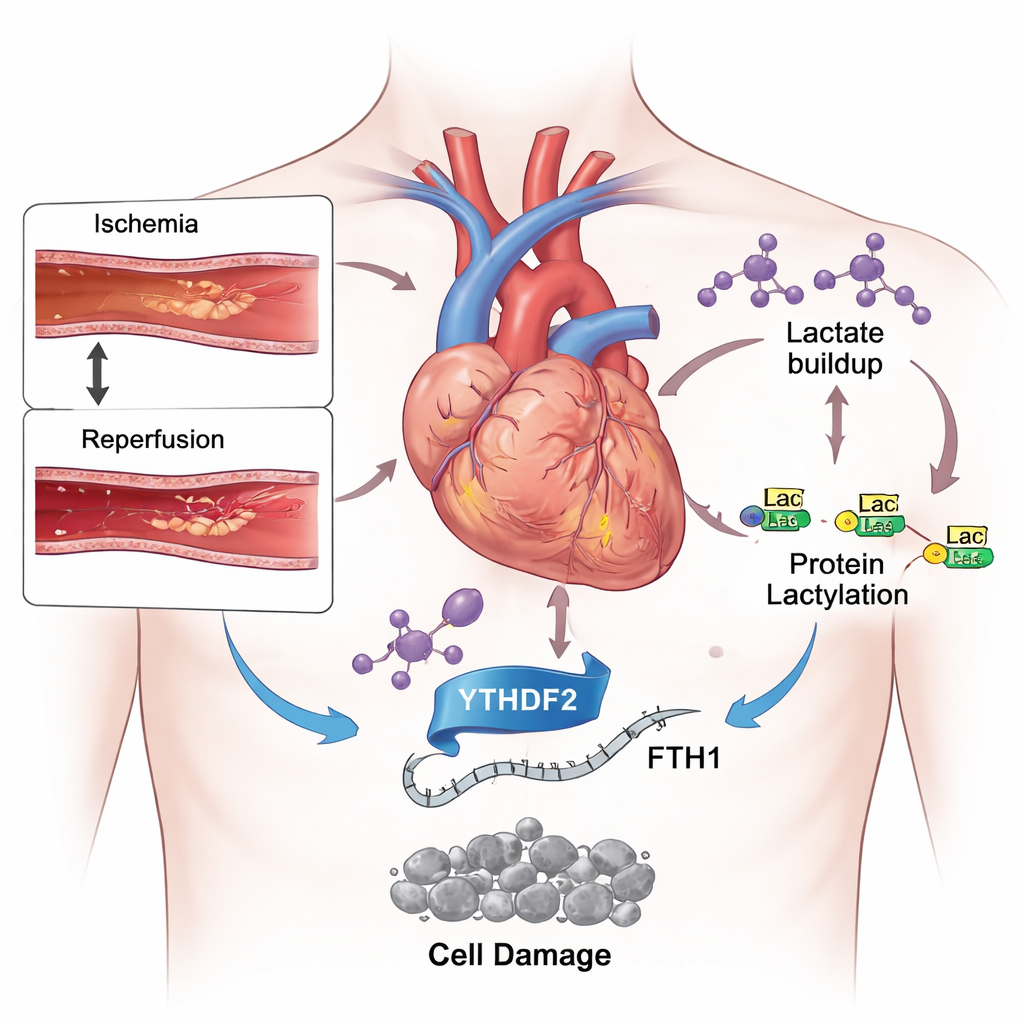
心脏病治疗中的双刃剑
现代医学在迅速重启堵塞的冠状动脉方面取得了很大进步,能限制心脏病发作的初期损伤。然而在恢复血流后,患者仍可能失去大面积心肌。部分原因是氧气和营养物质的突然回流在心肌细胞内引发了一场化学应激风暴。在这种情况下触发的多种细胞死亡类型中,一种较新的形式称为铁死亡(ferroptosis)引起了广泛关注。与更为人熟知的程序性死亡(如凋亡)不同,铁死亡依赖于铁和细胞膜脂质的失控氧化,这会对心脏造成持久的损害。
乳酸如何超越“肌肉灼痛”的概念
在心脏病发作期间,缺血的心肌将能量代谢转向糖酵解,这是一种快速分解糖的替代机制,但会产生大量乳酸。通过对经历短暂动脉阻断与再通的小鼠以及在低氧后再供氧的培养心肌样细胞的研究,研究人员发现乳酸水平显著升高。同时,他们在许多蛋白质和组蛋白(组织 DNA 的支架)上检测到更多的乳酰化标记。当他们给予动物一种抑制糖酵解、降低乳酸生成的药物时,心脏损伤减轻,血液中的损伤标志物下降,有害铁与保护性抗氧化剂之间的平衡得到改善。这些结果表明,过量乳酸不仅是应激的副产物,还是损伤的主动推动者。
松开铁的束缚的分子开关
进一步研究中,团队将注意力集中在YTHDF2上,这是一种识别RNA上化学标记并决定某些信息降解速度的蛋白。他们发现缺血–再灌注以及外加乳酸都能提高YTHDF2的水平,并在编码其基因附近增加乳酰化,从而放大其表达。YTHDF2的一个关键靶标是编码铁蛋白重链1(FTH1)的RNA,FTH1是细胞铁贮存笼的核心部分。FTH1通常将铁以安全形式封存,防止其参与有害反应。在受压的心肌细胞中,YTHDF2与FTH1 RNA的结合增强并加速其降解,导致细胞内可利用的铁增多、氧化应激加剧,并出现铁死亡的典型特征。
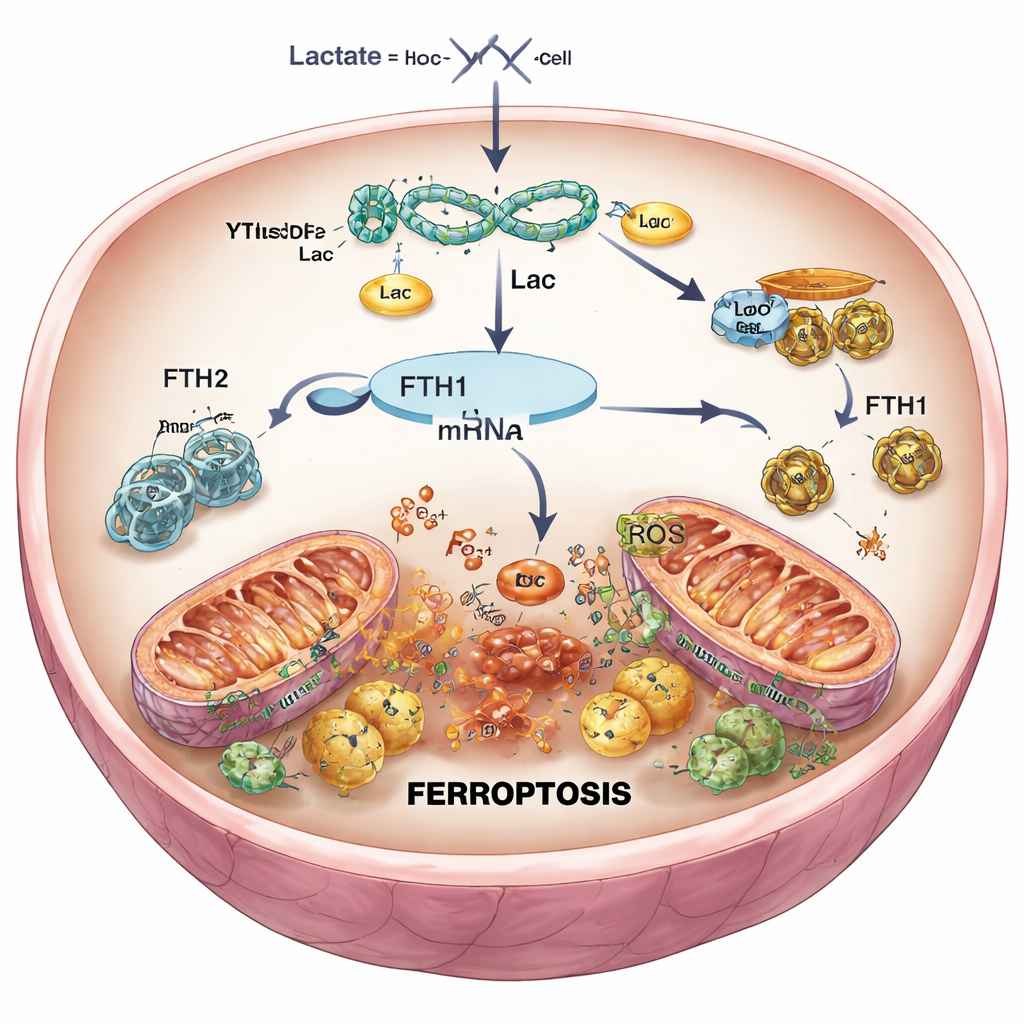
在心肌细胞中降低死亡信号
为检验因果关系,研究人员使用基因工具选择性下调心肌细胞和小鼠体内的YTHDF2。YTHDF2被敲低后,FTH1水平回升,铁和活性氧下降,线粒体保持更正常的形态,模拟再灌注后的细胞存活率整体提高。在小鼠中,降低YTHDF2导致梗死疤痕变小,组织外观更健康。然而,当同时降低FTH1时,这些益处大多消失:铁含量再次上升,氧化损伤恢复,梗死面积增大。这证实了YTHDF2主要通过抑制FTH1来促进铁死亡,从而削弱了心肌细胞对铁的控制。
对未来心脏治疗的启示
综合各项发现,这项研究勾画出一条新的事件链:动脉先阻塞后再通导致乳酸积聚;乳酸通过乳酰化提高YTHDF2;YTHDF2随后破坏负责守护铁的蛋白FTH1的RNA指令;由此产生的铁过载触发铁死亡,加剧心脏损伤。对患者而言,这一结论带来希望:该通路提供了多个新的干预点。限制有害乳酸信号、阻断YTHDF2特定修饰或维持FTH1功能的药物,或许能使急诊再通更安全,保护更多心肌。尽管这些发现仍需在人体组织中进一步验证,但它们为为心脏病幸存者提供更温和、更有效的治疗打开了有前景的途径。
引用: Xiang, Z., Xiang, B., Ouyang, T. et al. Lactate regulates the YTHDF2-FTH1 axis to promote cardiomyocyte ferroptosis and aggravate myocardial ischemia-reperfusion injury. Sci Rep 16, 4865 (2026). https://doi.org/10.1038/s41598-026-35130-3
关键词: 心脏病发作, 乳酸, 铁驱动的细胞死亡, 缺血再灌注损伤, 心肌细胞保护