Clear Sky Science · zh
双特异性磷酸酶6削弱叉头盒O1对CYP4A11的抑制活性,从而介导肝脏脂质堆积
为什么肝脏脂肪重要
肝脏中过多的脂肪,通常称为脂肪肝疾病,随着现代高糖高脂饮食变得越来越常见。虽然很多人听说过胆固醇或血糖,但较少有人知道肝细胞内存在一些微小的分子开关,它们决定脂肪是被燃烧还是被储存。本研究关注三种这样的开关——名为DUSP6、FOXO1和CYP4A11的蛋白——并揭示它们之间的拉锯如何将肝细胞推向储存多余脂肪的方向。理解这个隐秘的控制系统,可能为脂肪肝及相关代谢问题提供新的治疗思路。
肝细胞内的隐形交通指挥
研究人员聚焦于一种名为DUSP6的蛋白,已知其主要功能是关闭一种称为ERK通路的细胞信号通路。既往研究表明缺乏DUSP6的小鼠对饮食诱导的脂肪肝具有出人意料的抵抗力,其肝脏中CYP4A酶的水平较低,这类酶参与脂质代谢。在本项工作中,研究团队探究了DUSP6在人肝来源细胞中的作用,以及它如何影响人类对应的酶CYP4A11。他们使用两种常用的肝癌细胞系HepG2和HuH‑7作为人肝细胞的替代模型,并用棕榈酸和油酸的混合物使其暴露于模拟不健康高脂环境的条件下。 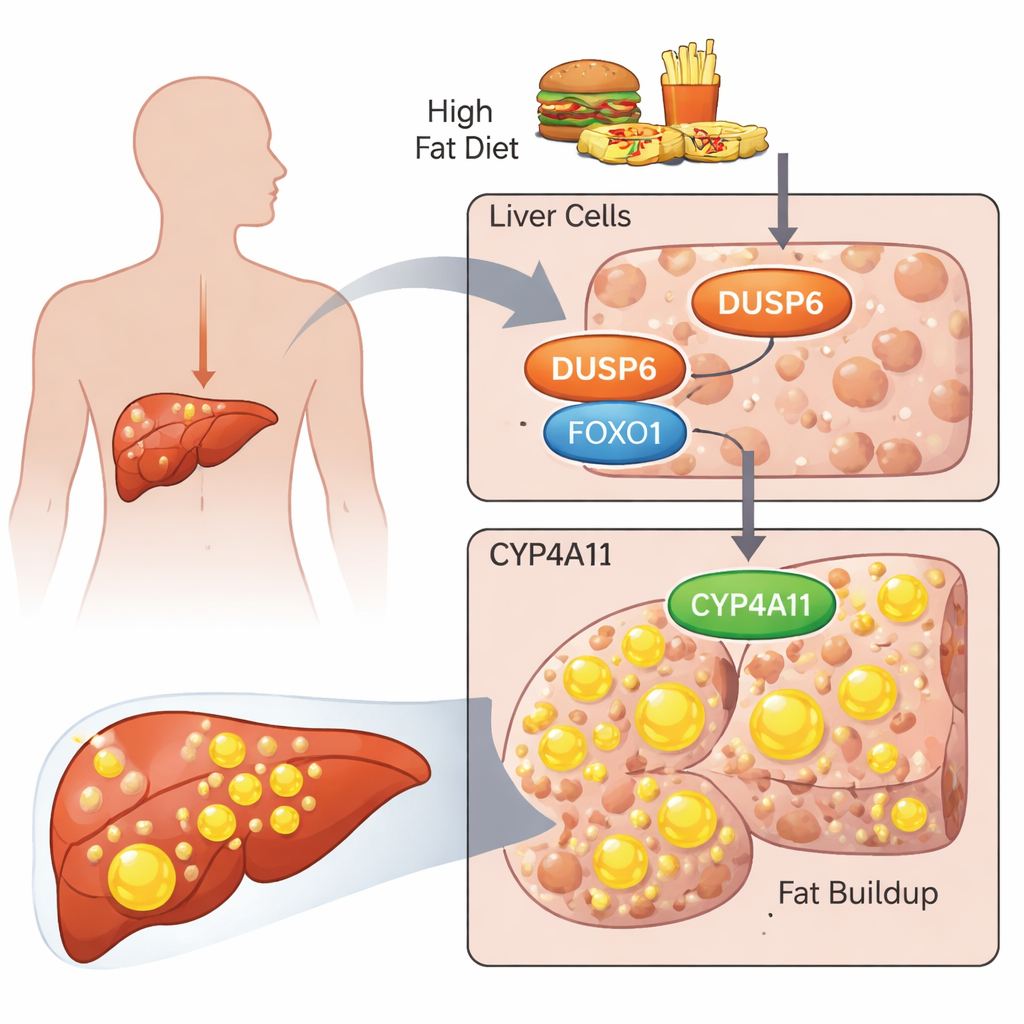
从脂肪酸到脂肪饱和的细胞
当细胞受到这些脂肪酸刺激时,能明显看到脂滴的积累,研究者对其进行了染色和定量。同时,DUSP6和CYP4A11的水平升高,伴随着两种主要信号蛋白AKT和FOXO1的活化形式。用靶向RNA降低DUSP6表达会扭转这一模式:细胞储存的脂肪减少,CYP4A11水平下降,但活化的ERK、AKT和FOXO1反而增加。单独阻断ERK通路实际上会加剧脂肪堆积,而单独抑制AKT则能减少脂肪。当同时抑制ERK和AKT时,脂肪积累下降,CYP4A11水平也随之降低。这些实验将CYP4A11与脂肪积累程度紧密关联,并表明AKT活性在推动脂肪储存方面尤为重要。
对促脂基因的刹车
另一个关键角色FOXO1是转录因子——能进入细胞核并开关基因的蛋白。已知FOXO1对CYP4A11所属酶家族的若干成员有抑制作用。研究团队发现,降低FOXO1水平会使细胞囤积更多脂肪并增加CYP4A11,而直接过表达CYP4A11会使细胞变得更脂肪化。相反,强制增加FOXO1表达会减少CYP4A11和脂肪积累。阻断CYP4A11活性的药物(HET0016)能够削减因FOXO1降低而引起的额外脂肪,支持了CYP4A11并非旁观者而是促进脂质堆积的驱动因子。化学检测显示,HET0016降低了由CYP4A11生成的20‑HETE,这一产物与氧化应激和炎症相关,进一步将该通路与肝损伤联系起来。
DUSP6如何解除刹车作用
为了解FOXO1如何控制CYP4A11,科学家们检查了CYP4A11基因前端的DNA区域,发现了FOXO1可结合的序列。通过染色质免疫沉淀实验,他们证明了FOXO1——尤其是其未磷酸化形式——直接结合CYP4A11启动子,符合其对该基因起抑制作用的角色。共免疫沉淀实验显示DUSP6与FOXO1发生物理相互作用,但不与其磷酸化形式相互作用。分馏和显微镜研究表明DUSP6位于细胞质中,并且在其存在时会使更多的FOXO1滞留在细胞质中。当敲低DUSP6时,更多FOXO1进入细胞核,在那里结合DNA并抑制CYP4A11。实际上,DUSP6起到类似锚定的作用,将FOXO1隔离在细胞质中,阻止其发挥对CYP4A11的刹车功能。 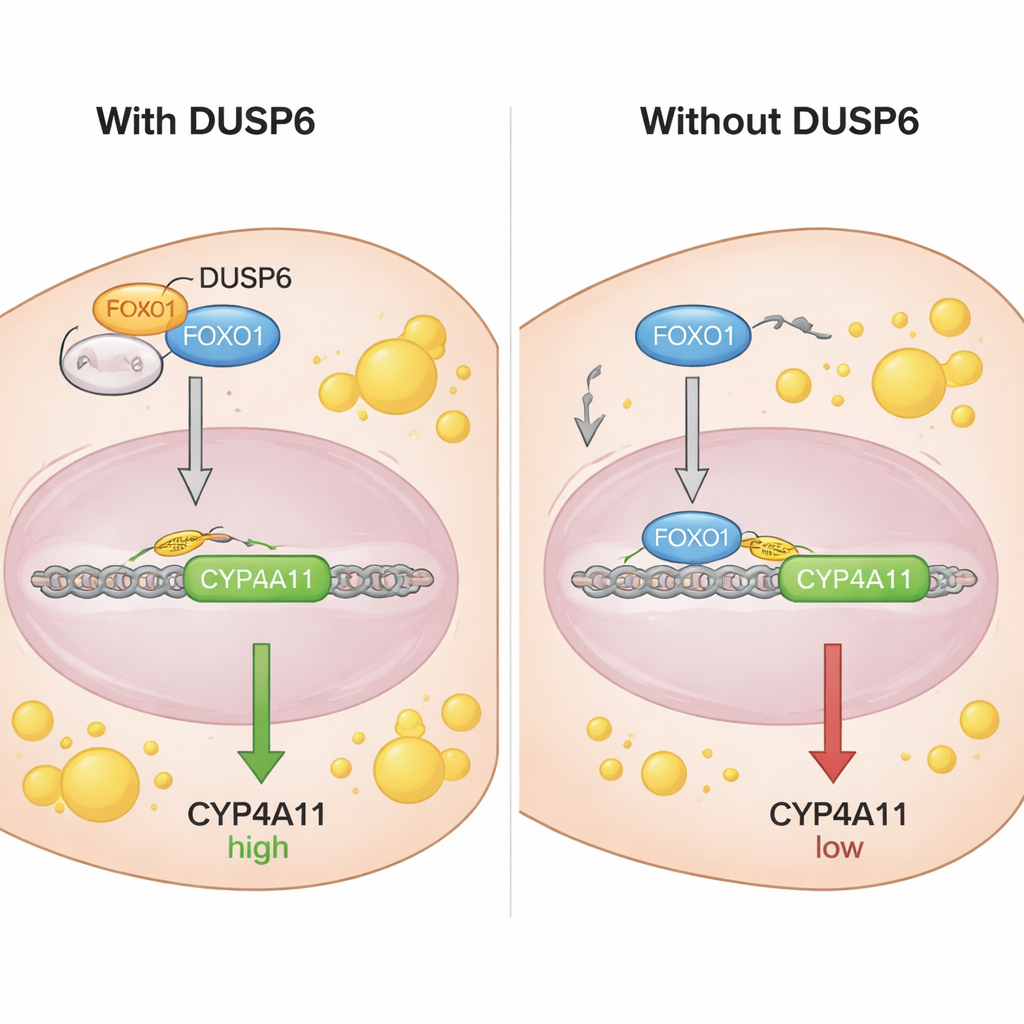
这对脂肪肝及其他方面的意义
简而言之,这项工作绘制出肝细胞内的一串事件:DUSP6将FOXO1滞留在细胞质,削弱了FOXO1关闭CYP4A11基因的能力。FOXO1被边缘化后,CYP4A11活性升高,促进细胞储存更多脂肪并产生像20‑HETE这样的分子,可能推动氧化应激和炎症。尽管这些发现来自培养的肝源性细胞系,而非健康人肝组织,但它们突出了DUSP6和CYP4A11作为治疗代谢功能障碍相关脂肪性肝病的潜在新靶点。理论上,降低DUSP6活性或抑制CYP4A11作用的疗法,可能恢复FOXO1的刹车功能,从而有助于控制肝脏脂肪的积累。
引用: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
关键词: 脂肪肝疾病, DUSP6, FOXO1, CYP4A11, 肝脏代谢