Clear Sky Science · zh
用机器学习挖掘DrugBank揭示新的BCL-2抑制剂候选物
为何寻找更聪明的抗癌药物很重要
癌细胞常常在应当死亡时拒绝死亡。许多肿瘤通过过度使用一类被称为BCL-2的“保镖”蛋白来阻断细胞的内在自杀程序而得以存活。尽管已有针对BCL-2的药物,但它们可能引发副作用,且并非对所有患者都有效。本研究探讨了现代机器学习如何在数千种已知药物中筛选出新的、更安全的候选物,这些候选物可能解除BCL-2的保护作用,帮助癌细胞启动自我毁灭。
细胞如何在生与死之间做出选择
健康组织通过一种受控的自我毁灭过程清除受损或不需要的细胞,这一过程称为凋亡或程序性细胞死亡。一组称为BCL-2家族的蛋白质充当了这一决定的核心开关。部分成员推动细胞走向存活,而另一些则推动细胞走向死亡。在许多癌症中,促进存活的成员(包括BCL-2及其近亲BCL-XL)过度表达。这种额外的保护使癌细胞忽视死亡信号并抵抗化疗。因此,阻断BCL-2成为癌症治疗中的一种有吸引力的策略,但现有药物常常也作用于相关蛋白,导致如血小板计数危险下降等副作用。
教计算机识别有前景的分子
研究人员并未从零开始寻找新化合物,而是转向已被研究或用作药物的分子数据库。他们首先使用了一个大型公共资源ChEMBL,该数据库包含不同化学物质与BCL-2结合强度的实验测量值。在仔细清理这些信息——去除重复项、不确定的测量以及过大或不寻常的分子——之后,最终得到601种表征良好的化合物。每个分子被转换为一种数字指纹,捕捉其结构特征。这些指纹用于训练并比较七种不同的机器学习模型,以判断新分子是否有可能成为强效的BCL-2阻断剂或基本无活性的物质。 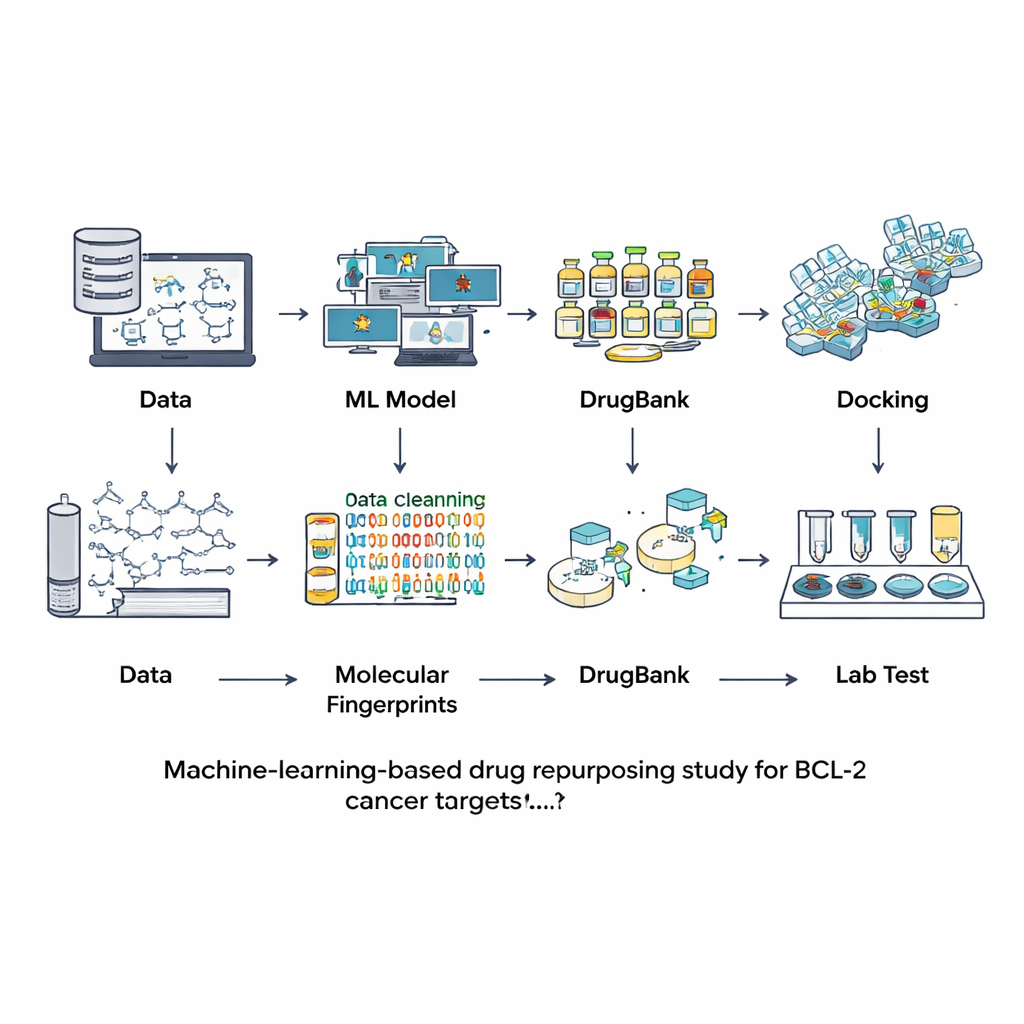
挑选最佳模型并扫描药物库
团队使用一组在训练期间未见过的独立测试集评估这些模型,不仅检查每个模型的正确率,还评估其区分活性与无活性分子的能力以及预测的平衡性。一种名为LightGBM的模型——一种现代的基于树的提升方法——在大多数指标上表现最佳,包括整体准确度和赋予可靠概率的能力。借助这一经调优的模型,研究人员转向DrugBank,这是一个收录了超过1.2万种已批准、实验性和已撤回药物的整理库。计算相同类型的指纹后,他们请LightGBM判断哪些分子看起来像潜在的BCL-2抑制剂。只有九种化合物得分很高,约为整个库的万分之十,表明虚拟筛选非常有选择性。其中四种已知为BCL-2抑制剂,这让团队对该方法的可靠性感到放心。
从计算命中到分子互作
在剩余的高分分子中,研究人员将注意力集中在三种此前未与BCL-2相关联的化合物:Dersalazine、Opelconazole 和 Zongertinib。为了评估这些候选物是否有可能契合BCL-2的结合口袋,他们使用了分子对接技术,这种技术可以预测小分子如何嵌入蛋白表面。模拟结果显示,尤其是Opelconazole和Zongertinib,可与与已知参考药物ABT-737相同的关键氨基酸形成有利的接触网络。它们的预测结合强度接近已确立抑制剂的水平,这暗示机器学习模型确实发现了可能解除BCL-2保护作用的分子。 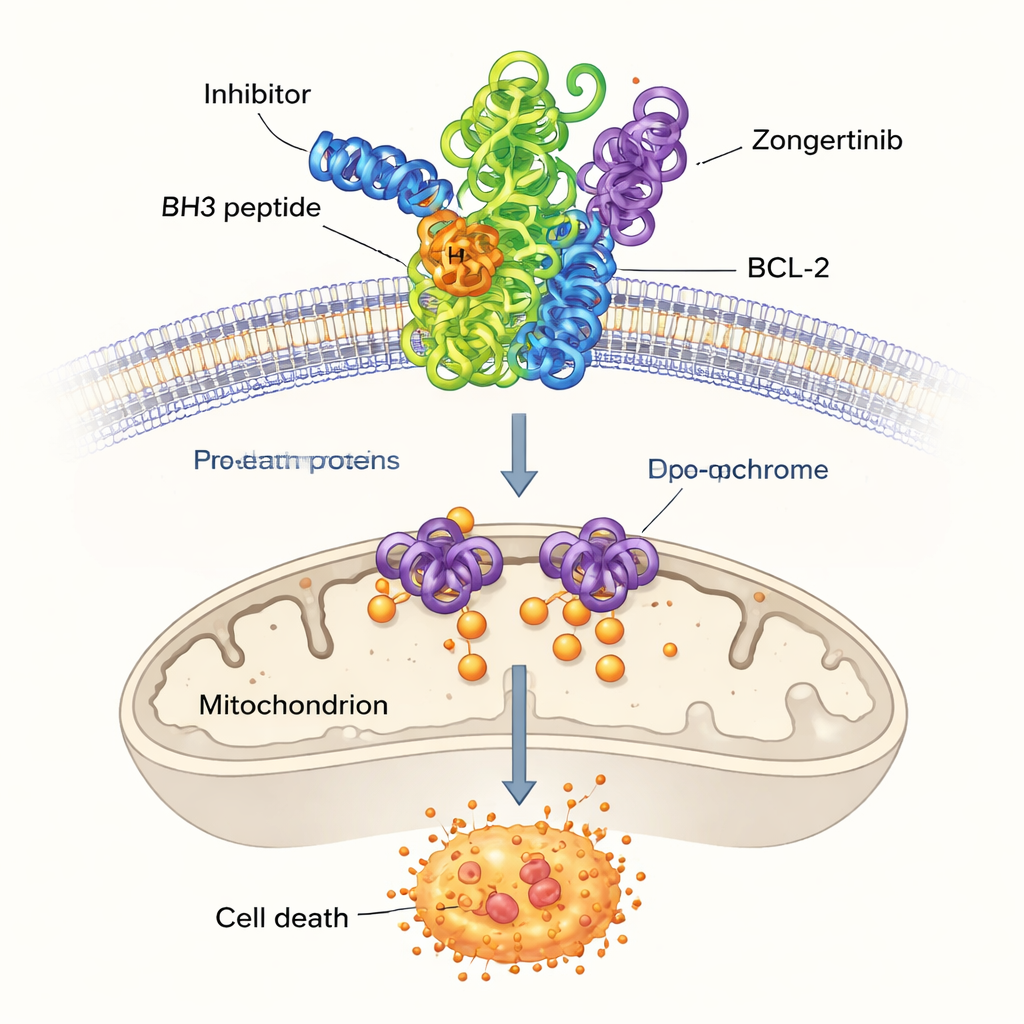
在实验室中检验预测
只有在真实条件下站得住脚时,计算提示才有意义。于是团队在生化测定中测试了这三种候选物,该测定衡量化合物阻止BCL-2与其天然配体结合的能力。在不同浓度范围内,Dersalazine几乎没有作用。Opelconazole和Zongertinib则在高剂量下均降低了BCL-2活性,其中Opelconazole几乎使信号关闭。尽管这些浓度高于临床理想水平,但这些结果表明这些候选物确实与BCL-2发生相互作用,并验证了整体发现流程。
这对未来癌症疗法意味着什么
给非专业读者的关键信息是:研究人员成功训练出一个计算机系统,能识别出什么样的分子“看起来像”BCL-2阻断剂,随后用它来挖掘一个大型的现有药物与类药物库。该方法既重新发现了已知的BCL-2药物,又指出了新的候选物,其中两种在实验室测试中显示出真实的抑制活性。虽然仍有大量工作要做——提高效力、评估安全性并在细胞和动物中测试——本研究展示了机器学习与精明的数据整理如何通过回收并重新评估我们已知的化合物,加速寻找更好抗癌药物的进程。
引用: Park, J., Cho, S., Lee, H. et al. DrugBank mining with machine learning reveals novel candidates for BCL-2 inhibition. Sci Rep 16, 5482 (2026). https://doi.org/10.1038/s41598-026-35117-0
关键词: BCL-2抑制剂, 机器学习, 药物重新定位, 凋亡, 癌症治疗