Clear Sky Science · zh
一种物理启发的图神经网络用于近似基于对接的DYRK2结合亲和力,助力阿尔茨海默病药物重新定位
这对阿尔茨海默病为何重要
阿尔茨海默病在全球范围内上升,但大多数现有药物只能缓解症状,而不能阻止病情进展。在实验室中测试新药既慢又昂贵,尤其是对于那些可能在记忆和神经健康中起作用但尚未充分研究的大脑蛋白。本研究探讨了一种智能捷径:使用带有物理知识的人工智能模型来预测现有阿尔茨海默药物与一个未被充分研究的蛋白DYRK2的结合强度,可能为治疗开辟新途径。
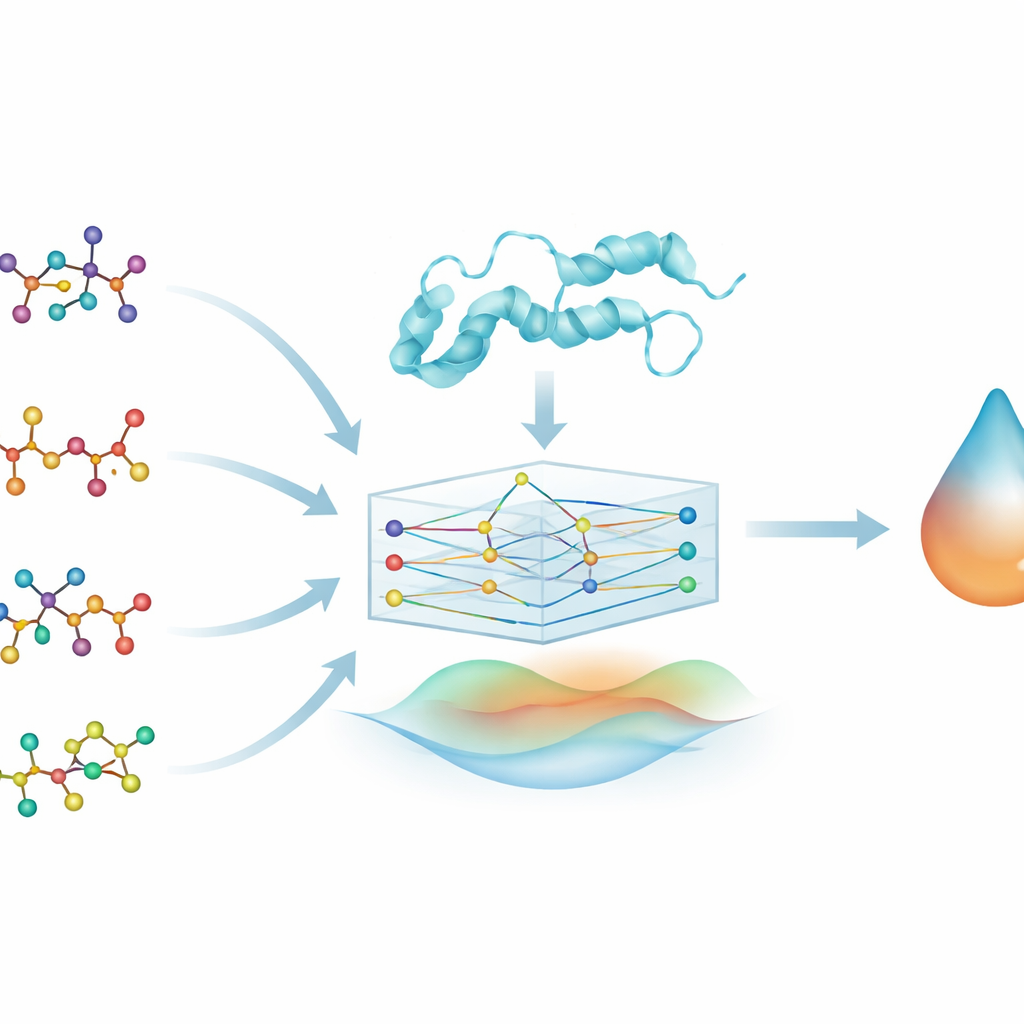
重新审视老药的新方法
研究者并非从头设计全新的化合物,而是聚焦于药物重新定位——为已获批准且安全性较明了的药物寻找新的用途。他们考察了四种熟悉的阿尔茨海默药物(brexpiprazole、donepezil、galantamine 和 rivastigmine),并探问每种药物可能与参与神经细胞生长与功能的蛋白激酶DYRK2结合得有多紧密。DYRK2 在阿尔茨海默病中的研究甚少,但早期证据将其与突触、轴突和记忆联系起来,使其成为一个有趣的靶点,可补充当前的治疗手段。
把分子变成网络
为研究这些药物—蛋白关系,团队将每个药物分子转换为图:原子变为节点,化学键变为连接它们的边。他们对 DYRK2 蛋白也做类似表示,将其氨基酸序列表示为一串相连的单元。图神经网络(GNN)这种机器学习模型天然适合处理这些图状输入,通过沿连接传递信息来学习形状和化学的模式。这样,名为 PhysDual‑GCN 的模型就能将药物和 DYRK2 当作相互作用的网络来“阅读”,而不是简单的字符串或特征列表。
将物理学与人工智能融合
药物发现中的大多数深度学习工具仅从数据中学习,这会使其内部机制难以解释。本文作者有意将原子相互作用的基本物理概念编织进模型中。除了学习到的图特征外,PhysDual‑GCN 还计算了两个经典能量项:一个描述部分电荷间的电吸引与排斥,另一个描述范德华力的推拉作用。这些基于物理的能量与 GNN 的内部表示相结合,随后输出预测的结合强度。实际上,该模型被训练来模拟标准对接程序(尤其是 AutoDock Vina 等相关工具)的行为——但运行更快,同时仍以熟悉的物理原理为基础。
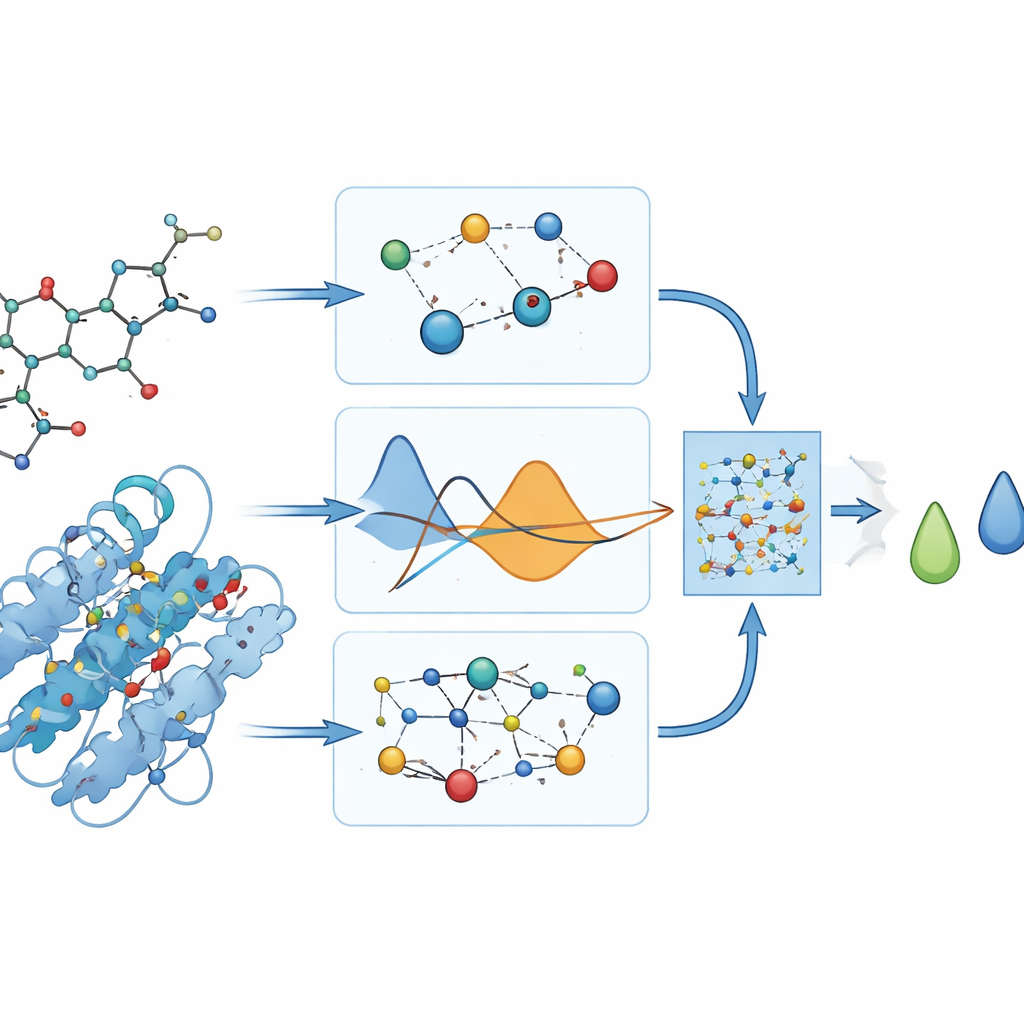
模型实际预测的内容
由于尚无实验室测量数据来说明这些药物与 DYRK2 的实际结合强度,作者依赖对接程序提供以能量为单位的“参考”结合评分。他们小心避免在训练过程中使用这些评分,而是在之后用它们来评估 PhysDual‑GCN 的学习效果。对于这四种阿尔茨海默药物,模型以较小的平均误差(约三分之一千卡/摩尔)重现了对接值,并且正确地对化合物进行了排序:donepezil 和 brexpiprazole 被判定为结合力最强,而 galantamine 和 rivastigmine 则显得较弱但仍相对稳定。这些结果表明,带物理约束的 GNN 可以作为较慢对接计算的计算替代方案。
该方法的潜力与局限
尽管这些结果令人鼓舞,作者强调他们的研究有严格的边界。仅考察了四种药物,所有评估都依赖其他计算程序而非真实的生化实验。DYRK2 蛋白主要被建模为一维序列图,而非完整的三维结构,因此模型尚不能考虑结合位点的详细形状。物理能量本身也被简化,使用了标准力场参数和截断值。因此,这项工作应被视为概念验证:它表明在低数据情形下,物理引导的图神经网络可以紧密追踪经典对接评分,但尚不能证明这些预测在试管或临床中与现实一致。
这对未来阿尔茨海默病研究意味着什么
对非专业读者而言,主要信息是:智能且具物理意识的算法可能帮助科学家比传统方法更快地探索像 DYRK2 这样的新阿尔茨海默靶点。通过将 donepezil 和 brexpiprazole 突出为有希望的 DYRK2 结合剂并提供一种透明的近似对接结果的方法,PhysDual‑GCN 为更深入的实验室研究提供了起点。借助更大的药物库、更丰富的三维蛋白信息和实验验证,这类模型有望成为筛选候选治疗药物并指导药物重新定位以减缓或改变阿尔茨海默病进程的实用工具。
引用: Gider, V., Budak, C. A physics-informed graph neural network to approximate docking-based binding affinity for DYRK2 in Alzheimer’s drug repurposing. Sci Rep 16, 8357 (2026). https://doi.org/10.1038/s41598-026-35102-7
关键词: 阿尔茨海默病, 药物重新定位, 图神经网络, 蛋白质–配体结合, DYRK2 激酶