Clear Sky Science · zh
多房棘球蚴囊泡细胞色素抑制蛋白B的晶体结构揭示了经典stefin的新特征
为何这种肝寄生虫的“秘密武器”重要
多房棘球蚴病这个名字有些拗口,它指的是一种在肝脏内行为类似缓慢生长肿瘤的小型绦虫感染。该病常致命,现有药物疗效有限且可能有严重副作用。本研究聚焦寄生虫分泌的一种特定分子——称为EmCystatin-B的蛋白——以弄清它如何帮助绦虫逃避免疫防御,以及将来如何把它作为新疗法的潜在靶点。
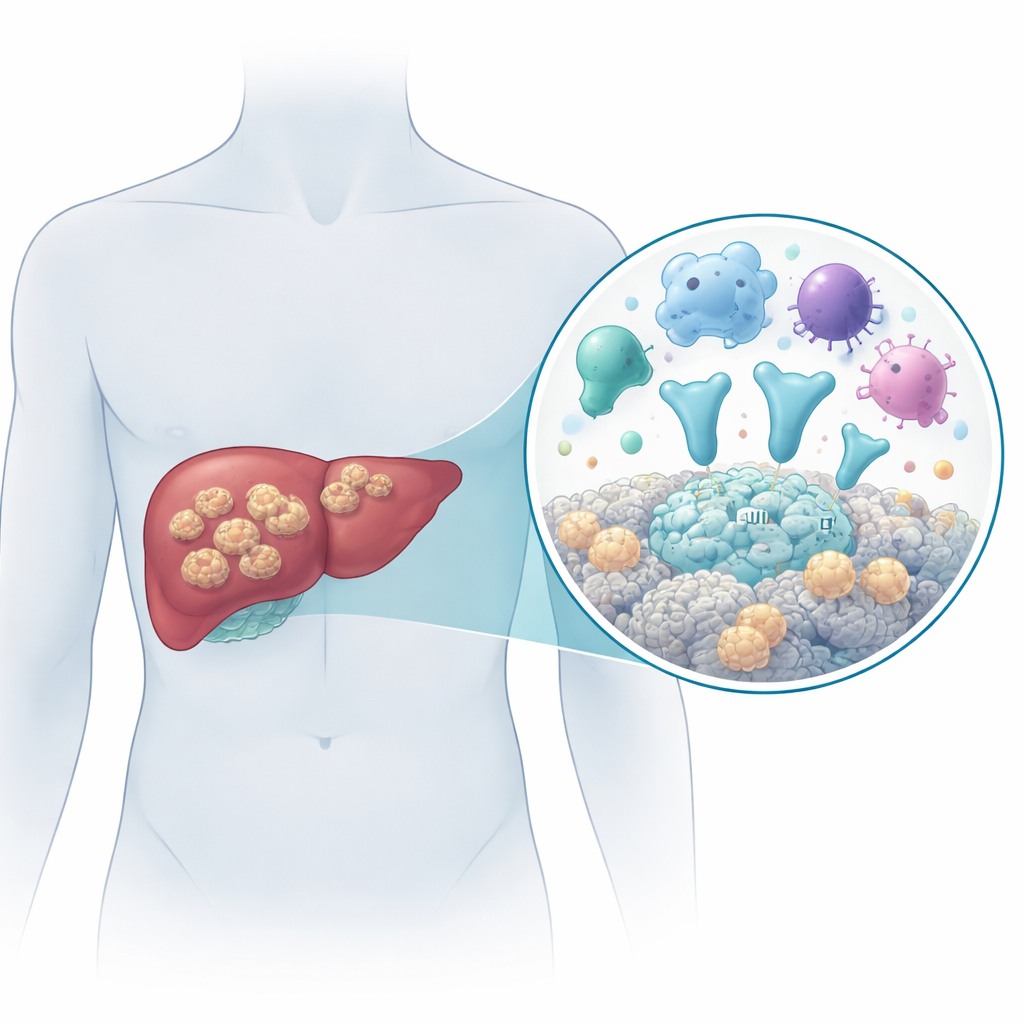
像肿瘤一样生长的危险绦虫
该病由绦虫Echinococcus multilocularis的幼虫期引起。人类通常通过误食受污染的食物或水而吞入寄生虫卵感染。一旦进入体内,幼虫主要定植于肝脏,形成许多充满液体的小囊,侵入周围组织、扩散到脾等邻近器官,有时甚至远及肺或脑。若未得到有效治疗,超过90%的患者会在10到15年内死亡。外科手术联合长期抗寄生虫药物目前是最佳方案,但早期诊断困难且药物不能可靠治愈感染。这就使得在分子层面理解寄生虫与人体的相互作用变得至关重要。
使切割酶失效的寄生虫蛋白
许多动物,包括人类,在体内产生一类称为囊蛋白(cystatins)的蛋白,作为对强效消化酶——半胱氨酸蛋白酶(cysteine proteases)的安全锁。这些酶能切割其他蛋白,在降解受损细胞成分和激活免疫反应等过程中很重要。寄生虫学会产生类似囊蛋白的分子来干扰宿主的酶活性与免疫系统。在这项工作中,研究者鉴定出来自E. multilocularis的一个囊蛋白样蛋白并命名为EmCystatin-B。他们发现EmCystatin-B的基因在寄生虫成熟幼体的头部(原头囊)中比在周围囊组织中表达得更高,并且该蛋白存在于寄生虫细胞的胞质和细胞核中,尤其富集于分裂的“类干细胞”生殖细胞中。体外实验表明,EmCystatin-B能强烈抑制人类的cathepsin B——一种参与免疫与组织重塑的重要半胱氨酸蛋白酶。
熟悉的构象带来意外转折
为精确观察EmCystatin-B的构建方式,团队对纯化的蛋白进行结晶,并用X射线晶体学解析其近原子分辨率的三维结构。像囊蛋白家族的其他成员一样,每个EmCystatin-B单元具有典型的构象:一段中心α螺旋与几条扁平的、带状的β链相衬,形成一个通常嵌入蛋白酶活性位点的楔形结构。根据序列特征且缺乏明显的分泌信号肽,EmCystatin-B归属于囊蛋白中的“stefin”亚组,这类蛋白通常较小、位于细胞内且不含稳定的二硫键。令人惊讶的是,尽管每个EmCystatin-B单元具有预期折叠,但这些单元之间的相互联结方式不同于人类对应物cystatin B,表现出异常且具有物种特异性的结合模式。
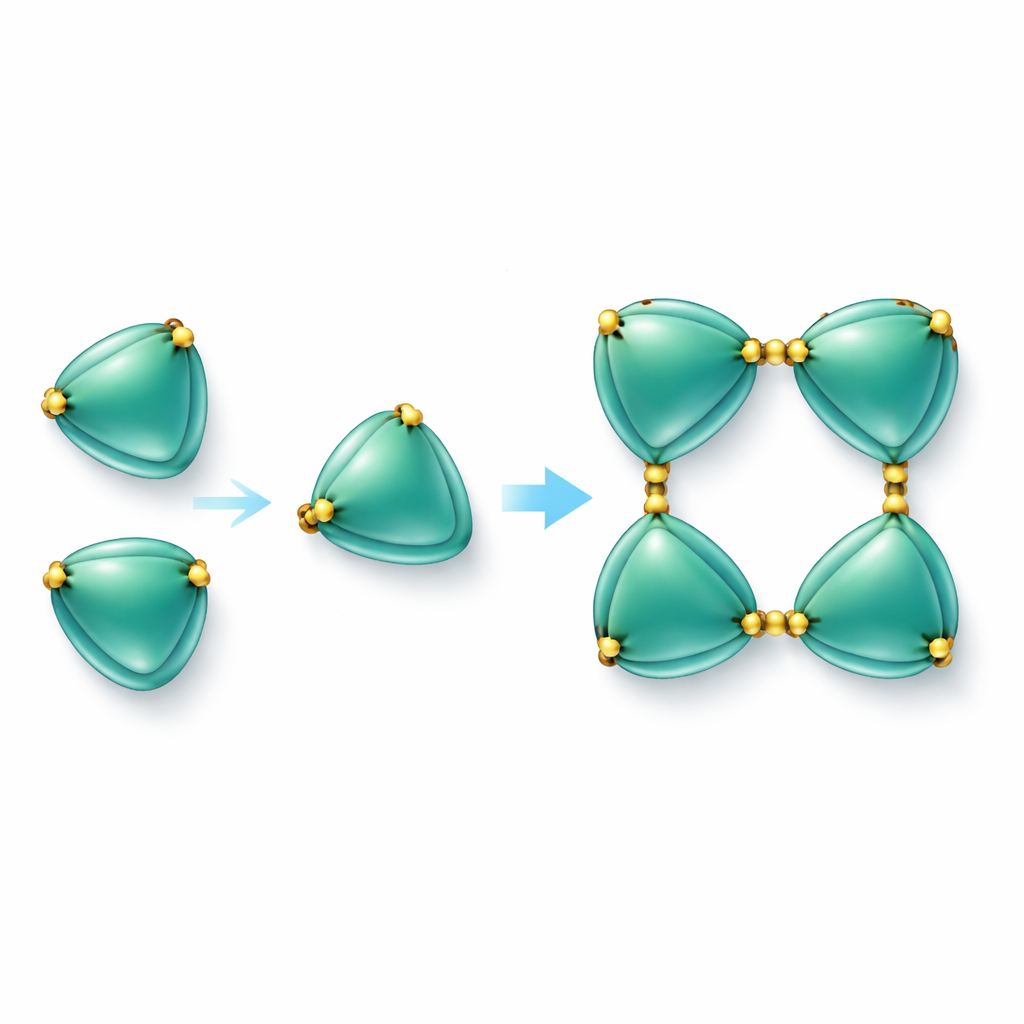
用硫键构建蛋白链
最引人注目的发现是EmCystatin-B分子并非仅以单体形式存在。相反,它们可以以阶梯式连结形成二聚体(成对)进而形成四聚体(四聚)。形成初始二聚体有两种不同机制。一种是分子的一部分摆动过去并完成邻近分子的结构,这种现象称为结构域互换(domain swapping)。另一种是分子对通过二硫键相连——即含硫氨基酸(半胱氨酸)之间的强化学键。在EmCystatin-B中,一个分子第4位的半胱氨酸与配对分子的第76位半胱氨酸形成键合。四个这样的交叉键随后稳定了四聚体。这种利用多重分子间二硫键的做法在经典stefin中是全新的,因为此类蛋白通常不含此类键。当研究者将这些关键的半胱氨酸替换为其他氨基酸时,蛋白无法有效组装成更高阶的复合体,其抑制cathepsin B的能力也显著下降。
对抗感染的含义
对非专业读者而言,该研究的要点是:寄生虫进化出一种特殊改造的常见蛋白家族成员,使用额外的化学“铆钉”将多个抑制单元锁定在一起。这种寡聚形式似乎对于关闭宿主本可用于控制感染的酶至关重要。通过揭示EmCystatin-B及其独特二硫键联结组装的精确结构,研究扩展了我们对囊蛋白如何在不同物种间被调节的认知。从长远来看,这些见解可为设计药物提供指导,药物要么阻断EmCystatin-B对寄生虫的保护作用,要么模仿其免疫抑制特性以治疗炎症性疾病。
引用: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
关键词: 多房棘球蚴病, 多房棘球蚴, 囊蛋白B, 蛋白质结构, 免疫调节