Clear Sky Science · zh
通过配体诱导的吡啶结构域界面重塑破坏 NLRP3 炎症小体组装
为何抑制失控炎症至关重要
从关节炎和痛风到心脏病与神经退行性疾病,许多慢性病都源自细胞内过度活跃的免疫报警系统。该报警系统的关键组成部分之一称为 NLRP3 炎症小体,它在抗感染中发挥作用,但在误触发时也会驱动有害炎症。本文描述了一种新型小分子 E9,它作用于 NLRP3 激活的早期步骤,为设计能够降低有害炎症而不完全抑制免疫系统的药物提供了新的思路。
有阴暗面的细胞火警
当机体感知到危险时,免疫细胞会组装 NLRP3 炎症小体,这是一种像分子火警一样的大型蛋白复合体。一旦形成,该结构会激活一种称为 caspase-1 的酶,进而激活强效的炎性信使分子,包括细胞因子 IL-1β 和 IL-18。这些信号对于抵抗感染和清除受损组织至关重要。但如果炎症小体长期维持开启状态或在不适当的时候被激活,就会促进影响关节、血管、脑和其他器官的慢性炎症性疾病。因此,全球研究者正寻求精确调控 NLRP3 的方法,而不进行广谱免疫抑制。
超越常见药物靶点的视角
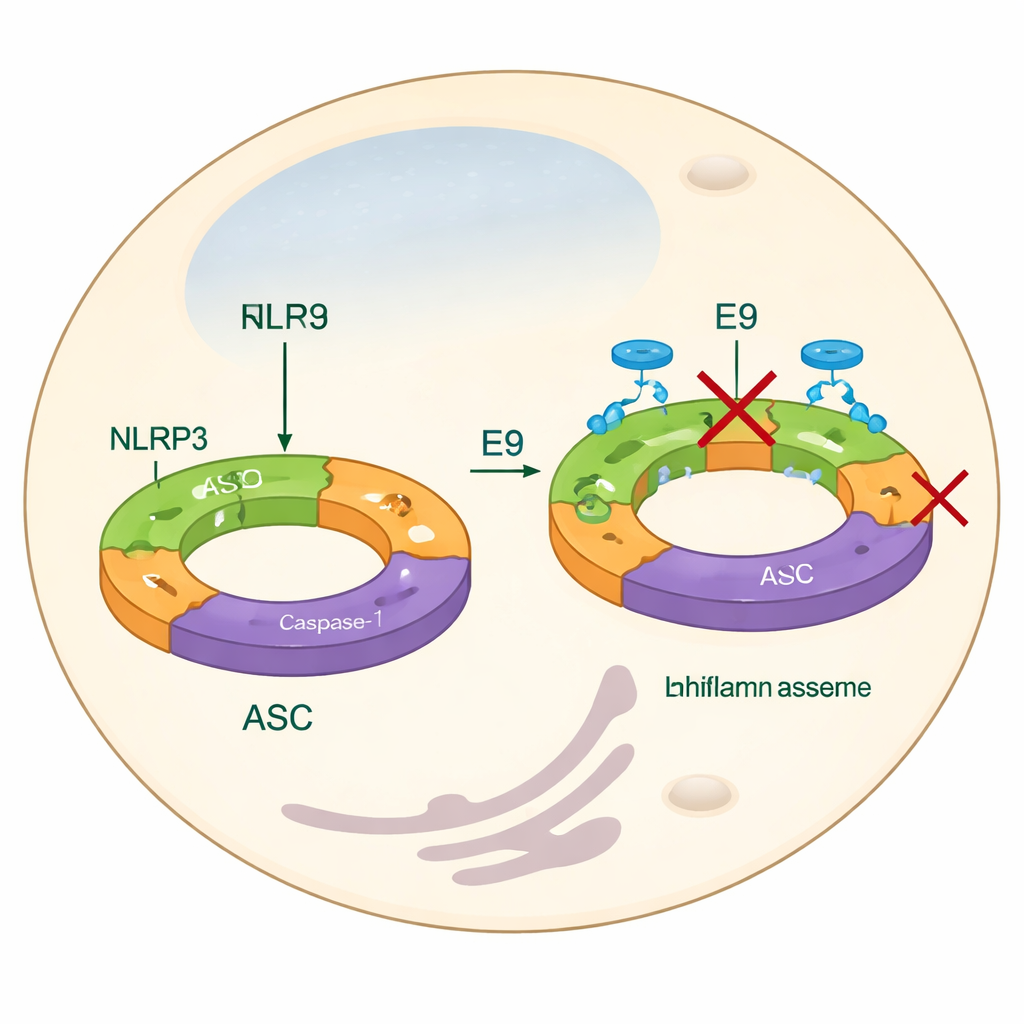
目前大多数抑制 NLRP3 的策略着眼于阻断其产物(如 IL-1β)或干扰利用 ATP 等能量分子的中心“发动机”样结构。尽管这些方法可能有效,但它们可能错过最早的组装步骤,也无法充分解决 NLRP3 蛋白如何结合形成功能性机器这一问题。本文作者转而聚焦于吡啶结构域——NLRP3 的一部分,帮助各个单元咔嚓地连接成长链丝状结构。这些丝状结构随后招募另一种适配蛋白 ASC,ASC 在细胞内聚集成明亮的“斑点”,这是炎症小体激活的视觉标志。通过寻找能阻止吡啶结构域正确配对的化合物,研究团队旨在从源头阻止炎症小体的形成。
找到可断裂链条的分子
研究者用一个巧妙的光学检测方法筛选了 1500 种新合成的小分子化合物。他们将分裂的荧光素酶片段与 NLRP3 吡啶结构域融合;当两个吡啶结构域结合时,酶片段重新组装并发出光。阻断吡啶—吡啶接触的化合物会导致光信号下降。该筛选鉴定出四个有前景的候选分子,其中 E9 以其强效且一致的抑制作用脱颖而出。随后的微量热泳(microscale thermophoresis)测定显示,E9 在非常低(亚微摩尔)浓度下与吡啶结构域紧密结合,证实其作用并非随机伪像,而是由特异相互作用引起。
在活细胞中观察效果
为检验 E9 在活体系中的作用,团队使用了经工程改造以表达荧光化 ASC 的类人免疫细胞。当这些细胞用细菌成分和第二信号刺激时,NLRP3 激活,ASC 蛋白聚成可在显微镜下计数的明亮斑点。在 E9 存在时,这些斑点的数量显著减少,效果可比或优于一些已知的 NLRP3 阻断剂。这表明干扰吡啶结构域接触足以减少炎症小体的组装和炎性细胞死亡的早期步骤,至少在体外条件下如此。
E9 如何重塑炎症小体支架
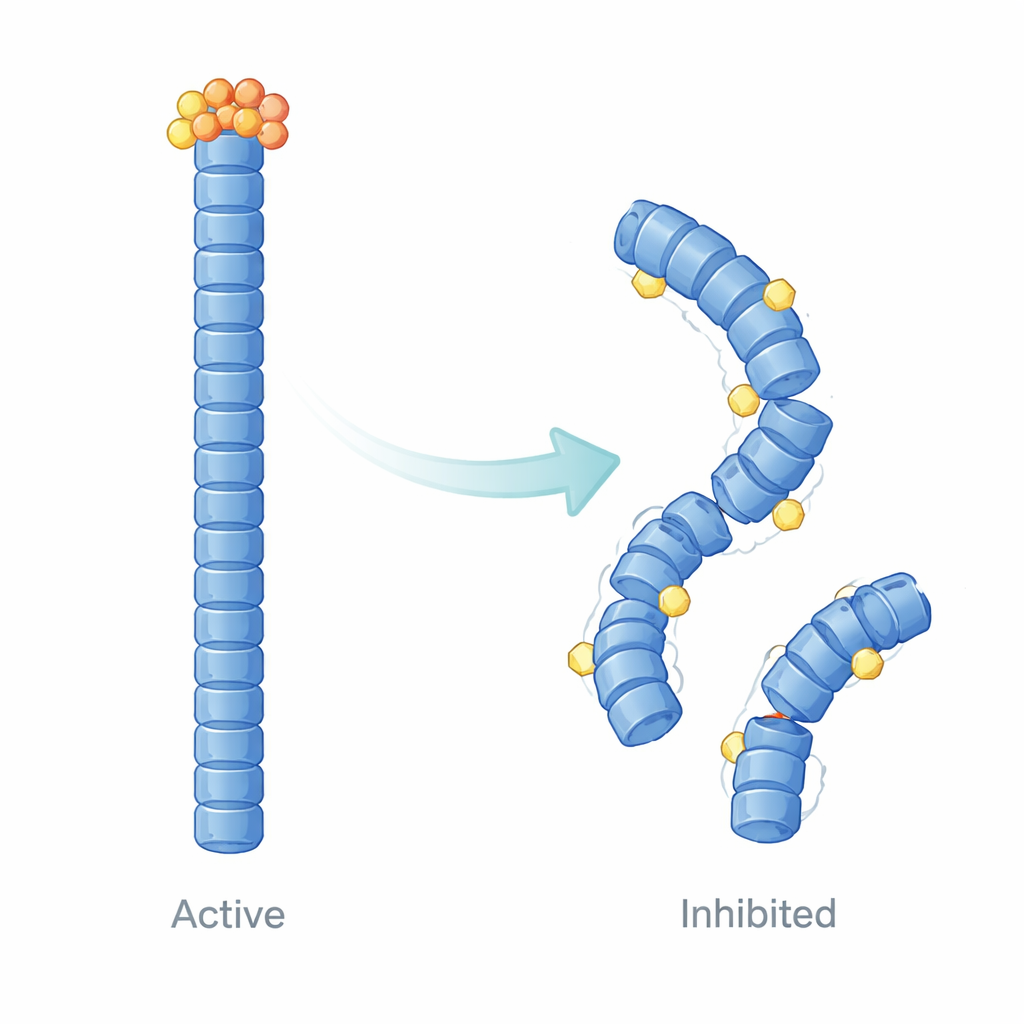
除了单纯测定结合外,作者还使用基于计算的结构建模与分子动力学模拟来可视化 E9 随时间如何改变 NLRP3 丝状体的行为。他们的计算表明,E9 嵌入于吡啶结构域接触的特定表面,微妙地放松并重塑丝状结构。丝状体不再是均匀稳定且协同的结构,而变得不规则:靠近结合 E9 的区域更为柔性并丧失精确对齐,而其他部分则变得动态隔离。这些变化削弱了规模化运动和进行有效 ASC 招募所需的紧密通信,为细胞中观测到的斑点减少提供了物理学上的解释。
这对未来疗法意味着什么
总体而言,这些发现将 E9 定位为一类新型炎症小体靶向药物的原型,这类药物通过破坏 NLRP3 构件之间的界面起效,而不是阻断其能量利用或终产物。尽管当前研究仅限于体外试验、计算模拟和培养细胞——仍需在动物和人体中进行进一步研究——但研究表明,精心设计的小分子可以直接重塑炎症小体的支架。对于由失控炎症驱动的疾病患者而言,这类聚焦于界面的药物未来可能提供更精确的控制,降低有害免疫激活的同时尽量保留必要的防御功能。
引用: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
关键词: NLRP3 炎症小体, 吡啶结构域, 小分子抑制剂, 先天免疫, 焦亡