Clear Sky Science · zh
miR-181d-5p/SPP1 轴通过 RhoA 通路抑制结直肠癌的迁移与侵袭
这项研究为何与日常健康相关
结直肠癌是全球最常见且致死率高的癌症之一,部分原因在于它常在被发现之前已经向身体其他部位扩散。该研究关注一种微小的基因调控因子——一种名为 miR-181d-5p 的微小 RNA,它像天然制动器一样抑制结直肠癌细胞的移动与侵袭能力。理解这种内在制动如何发挥作用,或能为放慢肿瘤扩散、改善存活率提供新的思路。
体积虽小但具重要保护作用的 RNA
微小 RNA 是非常短的 RNA 片段,虽然自身不编码蛋白质,但通过微调其他基因的开关来发挥作用。miR-181 家族已与多种器官的癌症相关。在这项工作中,作者发现其成员 miR-181d-5p 在人类结直肠癌组织及若干结直肠癌细胞系中显著降低,相较于邻近的非癌组织和正常肠上皮细胞。这一模式提示在健康状态下,miR-181d-5p 通常有助于抑制细胞增殖与运动,而其丧失可能使癌细胞更易扩散。
这枚“制动器”如何影响癌细胞行为
为观察 miR-181d-5p 的实际作用,团队在一种结直肠癌细胞系中人为提高其水平,在另一种细胞系中降低其水平。当 miR-181d-5p 被提升时,癌细胞增殖变慢,在培养皿上的“划痕”愈合更慢,通过多孔膜迁移的能力也下降——这三项都是衡量肿瘤侵袭性的常用实验。相反,当该微小 RNA 降低时,这些行为均加速。细胞形态也发生改变:miR-181d-5p 增高使细胞更趋圆形且胞内支架较弱;而水平降低则产生细长且具有明显应力纤维的细胞形态,这种形态更利于在体内迁移。
参与癌症扩散的关键蛋白靶点
研究者接着探查 miR-181d-5p 控制的是哪个基因。借助计算预测与报告基因实验,他们证明该微小 RNA 直接结合并抑制一种名为 SPP1(亦称骨桥蛋白)的蛋白的信使 RNA,从而阻断其生成。SPP1 在侵袭性癌症中常呈高表达,已知能促进细胞运动与存活。在患者样本与细胞系中,SPP1 在 miR-181d-5p 水平低的情况下升高,二者呈负相关。通过改变癌细胞中 miR-181d-5p 的水平能够相应驱动 SPP1 的上下调,同时影响下游调控子 RhoA,后者重塑细胞内骨架并协助细胞爬行。
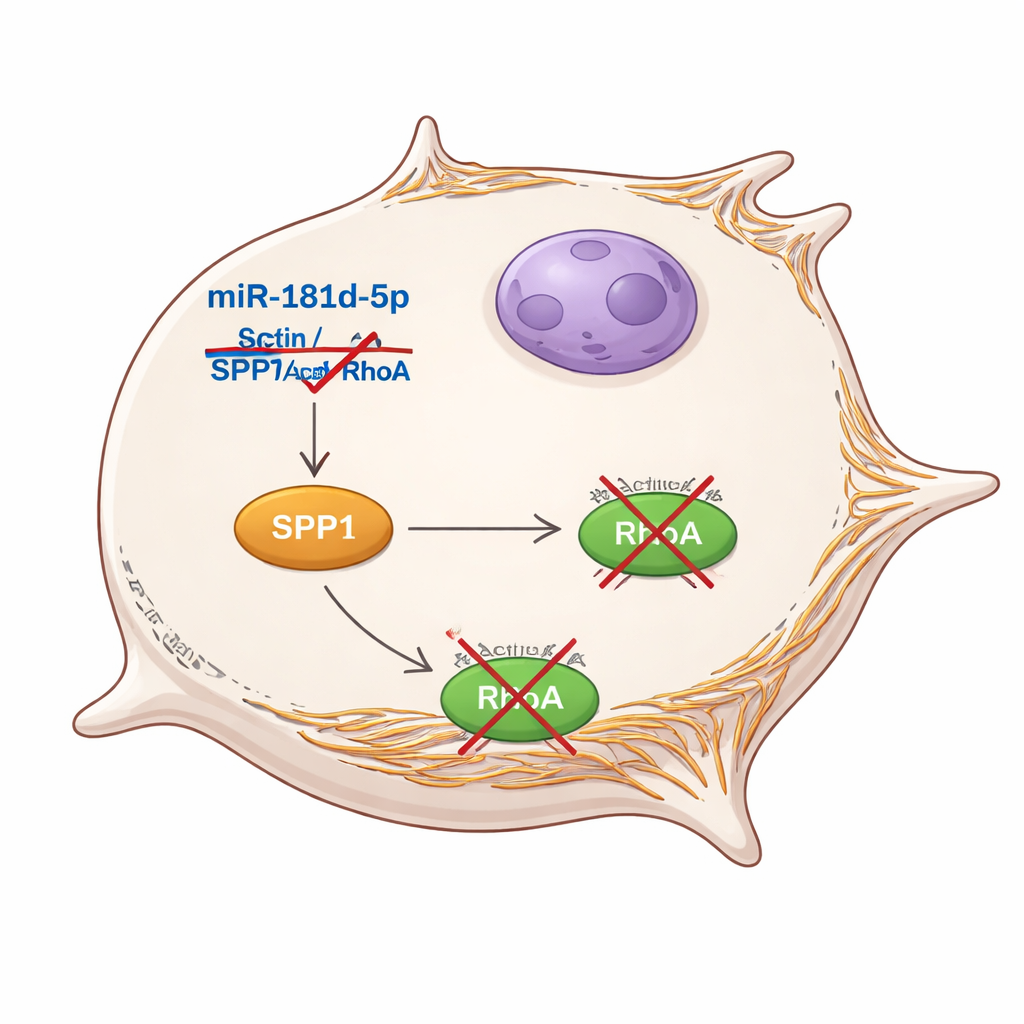
解析驱动侵袭的通路
随后,作者直接操控 SPP1。对 SPP1 高表达的细胞,增殖、迁移与侵袭均增强,分子标志也转向更易移动、附着性降低的状态。抑制 SPP1 则出现相反变化。关键的是,当他们提升 miR-181d-5p 的同时强制细胞额外表达 SPP1 时,miR-181d-5p 所带来的许多抑制效应被抵消。这一“拯救”实验表明,miR-181d-5p 之所以能限制结直肠癌细胞,主要是通过抑制 SPP1,从而控制 RhoA 通路。在小鼠模型中,由富含 miR-181d-5p 的细胞形成的肿瘤生长更慢,侵袭性组织改变较少,且 SPP1、RhoA 与细胞分裂标志 Ki-67 的表达较低。
对未来治疗可能的意义
简言之,本研究揭示了结直肠癌中的一条指挥链:微小 RNA miR-181d-5p 充当主控开关,下调 SPP1,进而抑制有助于细胞重塑与扩散的 RhoA 系统。当这种保护性的微小 RNA 丧失时,SPP1 与 RhoA 变得过度活跃,肿瘤更易生长与侵袭。尽管要将这些发现转化为治疗手段仍需大量工作,但恢复 miR-181d-5p 或阻断 SPP1 有朝一日可能成为减缓或预防结直肠癌转移、改善患者预后的策略之一。
引用: Hou, S., Guo, T., Wu, J. et al. The miR-181d-5p/SPP1 axis inhibits the migration and invasion of colorectal cancer via the RhoA patyway. Sci Rep 16, 4883 (2026). https://doi.org/10.1038/s41598-026-35040-4
关键词: 结直肠癌, 微小 RNA, 转移, SPP1, RhoA 信号