Clear Sky Science · zh
原发与配对异时性转移性透明细胞肾细胞癌的分子谱分析揭示肿瘤免疫微环境的异质性
为什么这项肾癌研究很重要
肾癌常常转移到身体的其他部位,而现代免疫疗法并非对每位患者或每个肿瘤都同样有效。本研究深入探讨透明细胞肾细胞癌——最常见的肾癌类型——以观察原发肾肿瘤与其后期转移灶中免疫系统的不同表现。理解这些差异有助于解释为何部分肿瘤对治疗反应更好,并可能指导更精准、个体化的治疗决策。
窥探原发与转移肿瘤
研究者选取了19名患者,这些患者切除了肾部原发肿瘤,随后在肺、骨、肝、肾上腺、淋巴结或软组织等处出现转移灶。共收集了42份肿瘤样本:19份原发肿瘤和23份未经治疗的转移灶。他们从石蜡包埋的薄切片中提取RNA——一种反映基因被激活情况的分子——并使用高通量测序捕捉每份样本中数千个基因的表达情况。 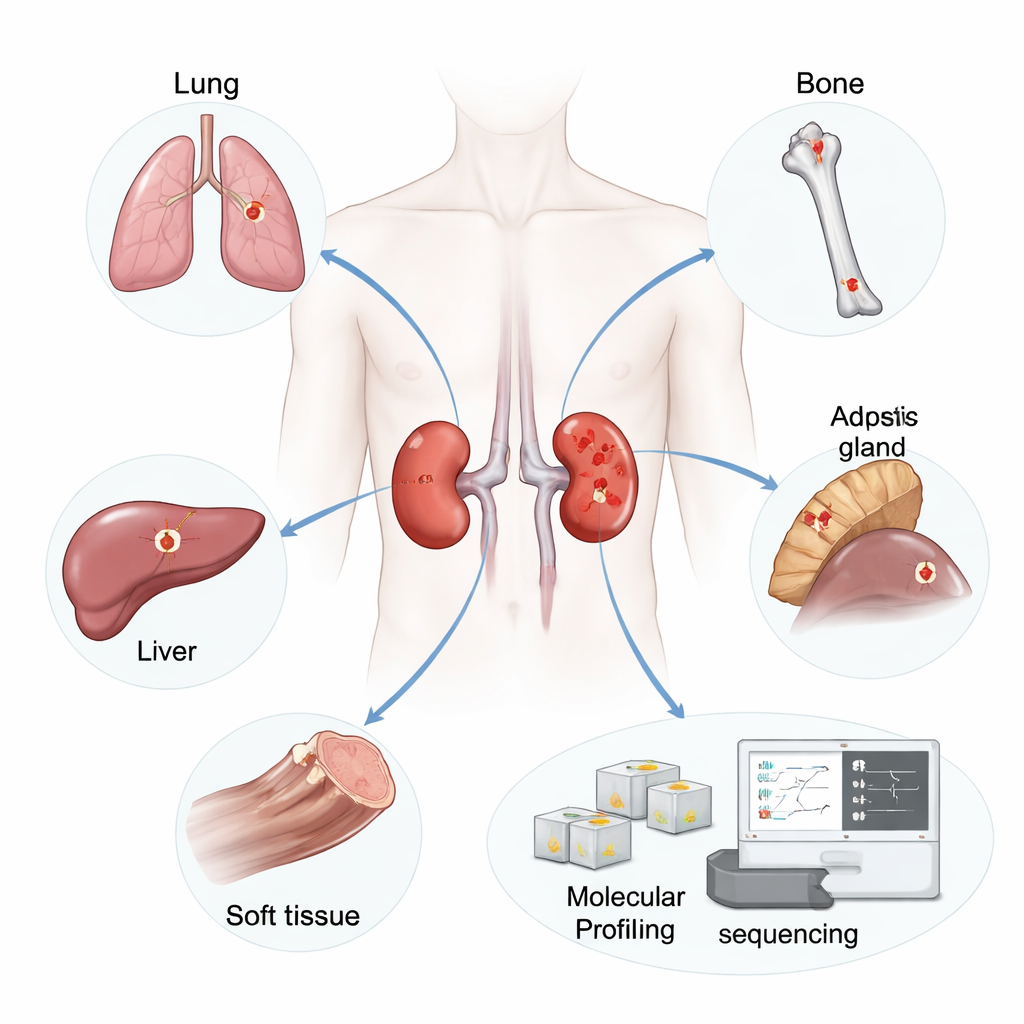
原发与转移肿瘤在分子上各不相同
当团队分析基因表达模式时发现,原发肾肿瘤往往彼此聚类,相互之间比与自身的转移灶更相似。换句话说,某位患者的转移灶可能与其原发肿瘤的差异比与另一位患者的转移灶的差异还大。数千个基因在转移灶与原发肿瘤之间表现出更高或更低的活性。与原发灶相比,转移肿瘤在与快速细胞分裂和侵袭性行为相关的基因程序上表现出更强的信号,包括细胞周期检查点和蛋白质合成通路。而原发肿瘤则更富集于应激和信号传导通路,如缺氧(低氧)与炎性信号,暗示肾脏内与远处器官存在不同的生物学压力。
随着癌症扩散,免疫格局发生变化
除了原始的基因表达外,科学家们还使用一种从总体RNA数据反卷积出免疫细胞成分的计算方法,估计每个肿瘤中存在哪些免疫细胞类型。他们发现了显著差异:原发肾肿瘤含有明显更高比例的调节性T细胞(Tregs),这是一类抑制免疫反应、能保护肿瘤免受攻击的免疫细胞。原发灶还富含静息树突状细胞、单核细胞、自然杀伤细胞和CD8+ T细胞。相反,转移灶中M2型巨噬细胞更为丰富——这类细胞常与伤口愈合及支持肿瘤的微环境相关——并伴有更多浆细胞和活化的树突状细胞。 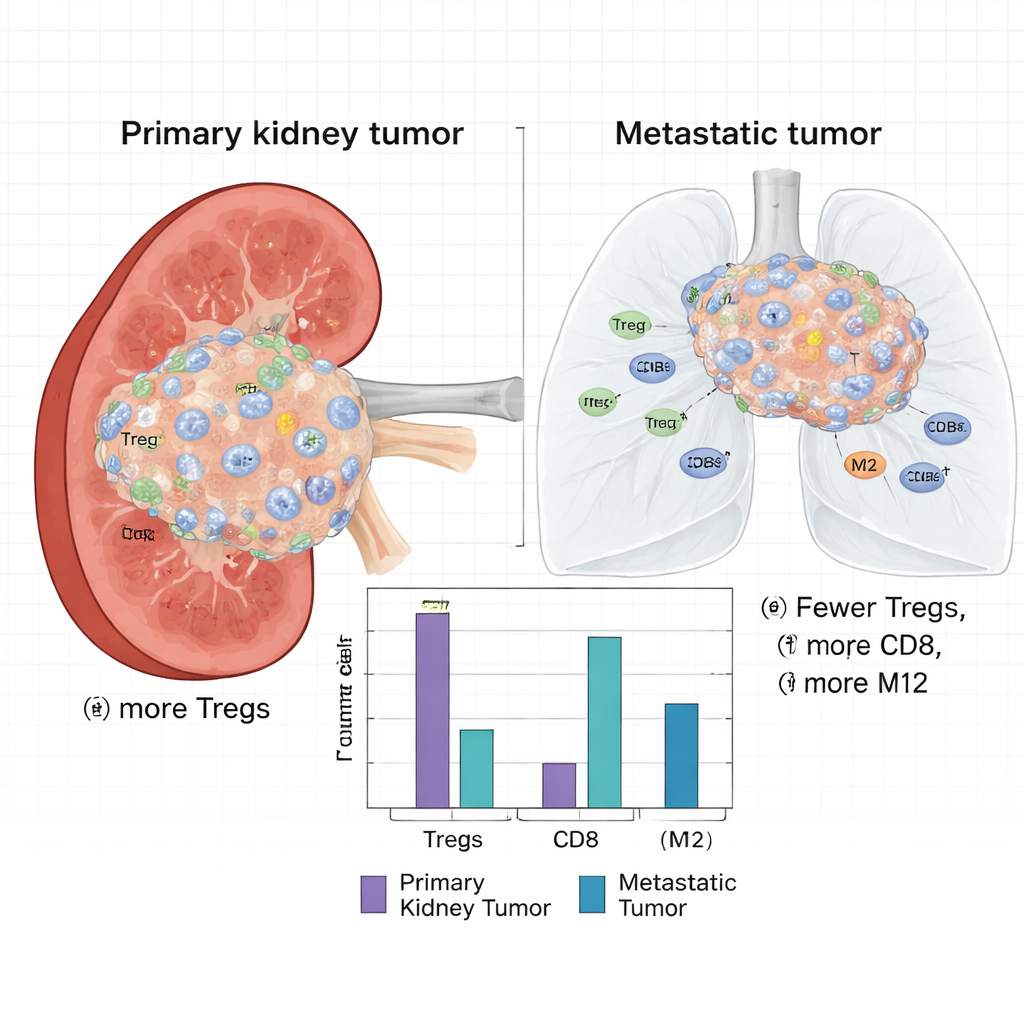
肺与骨转移呈现不同的免疫特征
当研究者聚焦具体的转移部位时,出现了重要的细微差别。肺转移灶显示出与细胞分裂控制(G2M检查点)和E2F转录因子相关的基因集合活性增加,并且高表达hornerin——一种与肿瘤血管生成相关的蛋白。配对的原发肾肿瘤则更富集于缺氧相关的基因程序,并再次显示出更多的Tregs。相比之下,骨转移灶以上皮-间质转化(EMT)的更强激活为显著特征,这一过程有助于癌细胞变得更具移动性和侵袭性。这些骨病灶还含有更高水平的M2型巨噬细胞,而导致这些转移的原发灶则显示出HHLA2(一种新近被认识的免疫检查点分子)表达增加。综合来看,这些发现强调转移灶的免疫与分子环境不仅与原发灶不同,而且不同转移部位之间也存在差异。
免疫细胞平衡与患者结局
为了解这些免疫模式对患者意味着什么,团队转向三组大型公开的透明细胞肾癌数据集。他们使用相同的计算方法估计Treg和CD8+ T细胞水平,并将其与生存结局相关联。在各个队列中,那些肿瘤呈现低CD8+ T细胞(主要的抗肿瘤T细胞)且Treg水平高的患者,其无进展生存或疾病特异性生存往往更差,即便在调整了年龄、肿瘤分级和分期后仍然如此。总体分期仍然强烈影响生存,但抑制性Tregs与攻击性CD8+细胞之间的平衡则显现为额外的风险标志。
这对未来肾癌治疗的意义
通俗地说,本研究表明原发肾肿瘤与其转移灶存在不同的免疫“邻里”环境。原发肿瘤特别擅长召集抑制免疫反应的和平维持细胞,这可能部分解释为何原位肾肿瘤对免疫治疗的响应往往弱于转移灶。与此同时,转移灶会在不同器官中演化出各自的局部支持系统。这些见解表明,临床上有时可能需要同时取样肾肿瘤和转移灶以全面评估患者病情,并且将免疫检查点抑制剂与针对Tregs或M2型巨噬细胞的策略联合使用,可能改善转移性透明细胞肾细胞癌患者的预后。
引用: Cotta, B., Nallandhighal, S., Monda, S. et al. Molecular profiling of primary versus paired asynchronous metastatic clear cell renal cell carcinoma reveals heterogeneity in tumor immune microenvironment. Sci Rep 16, 5473 (2026). https://doi.org/10.1038/s41598-026-35021-7
关键词: 肾癌, 肿瘤微环境, 免疫治疗, 转移, 调节性T细胞