Clear Sky Science · zh
衰弱症患者骨骼肌异常可变剪接的转录组学特征
为什么衰老的肌肉会失去力量
衰弱症——随年龄增长逐渐丧失肌肉质量和力量——是老年人日常活动变得困难的主要原因之一,从爬楼梯到提购物袋都受影响。这项研究在 RNA 水平上深入研究了衰老的肌肉,即那些告诉细胞合成何种蛋白的信使。作者表明,在衰弱症中,许多这类 RNA 信息被异常地剪切和拼接,可能破坏肌肉的能量生成,并指向新的治疗靶点。
肌肉流失与体内基因“编辑”系统
我们的基因写在 DNA 中,但细胞是根据基因的 RNA 复制本工作。在 RNA 信息被使用之前,细胞通常会对其进行修剪和拼接——有点像编辑影片——使同一个基因能产生多种蛋白版本。这一过程称为可变剪接,在肌肉中尤为活跃,因为肌肉需要精细调控的蛋白来收缩、修复并适应运动。当剪接出错时,可能产生错误的蛋白版本或丢失重要蛋白,从而促成诸如肌营养不良症和某些脑部疾病等病症。作者怀疑,类似的隐藏性 RNA 错误编辑也可能在驱动衰弱症。
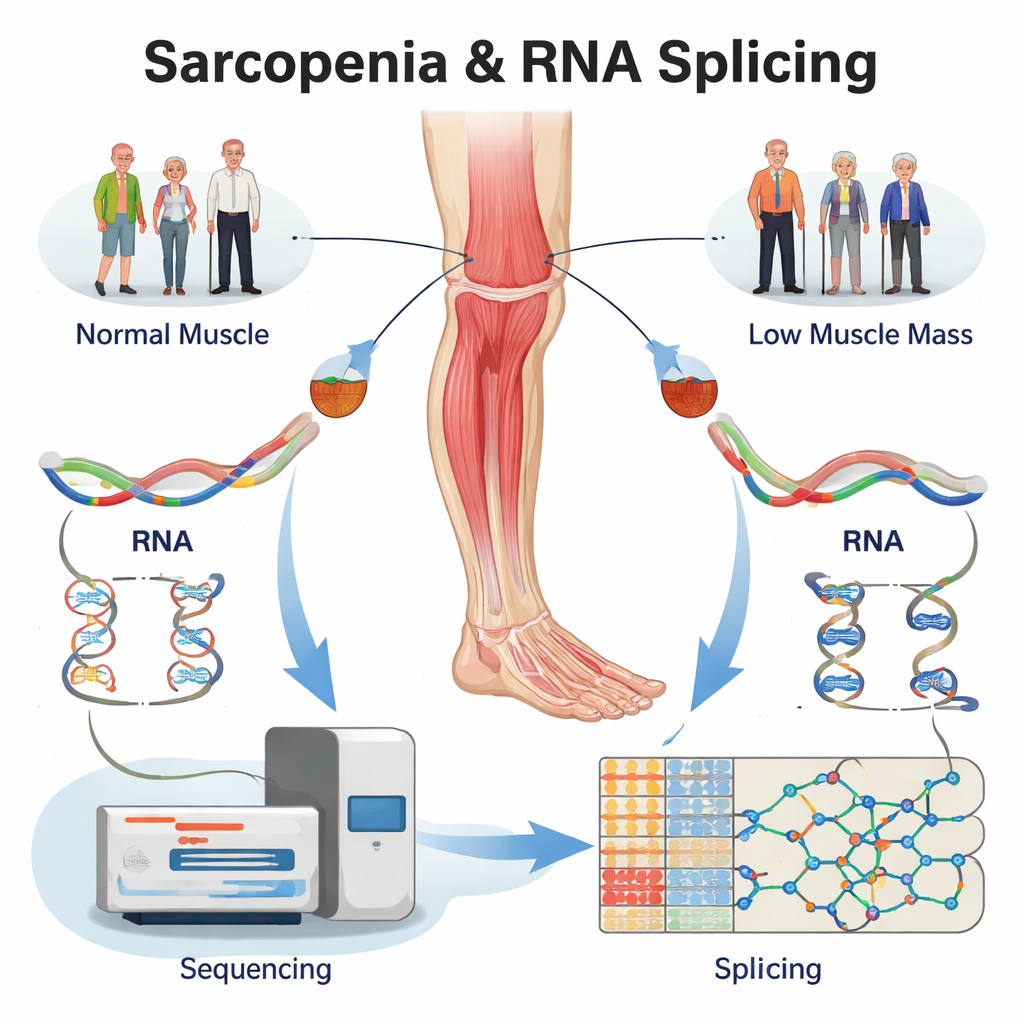
重读现有数据以发现隐藏的 RNA 错误
研究团队没有招募新志愿者,而是重新分析了一组来自人体大腿肌肉活检的大型 RNA 测序现有数据。样本来自四个组:确诊衰弱症的老年人、仅有低肌肉量的人、仅有低肌力的人,以及年龄匹配的健康对照。使用专门软件,他们首先证实数百个基因在病变肌肉中表达水平升高或降低。更重要的是,他们随后检查了每个基因的 RNA 剪接方式,记录了在与健康肌肉相比的三个问题组中超过 5,000 个剪接改变。这些改变集中在几种基本类型——例如跳过外显子或选择替代切点——这些模式已知会强烈改变蛋白结构。
能量工厂和细胞“燃料表”通路受扰
剪接改变出现在处于肌肉生物学核心的基因中。许多受影响的基因构建线粒体的部分,线粒体是为肌肉收缩提供动力的微小能量工厂。在衰弱症肌肉中,16 个参与氧化磷酸化(将营养物转化为可用能量的过程)的基因显示出剪接异常,尤其是处理电子传递和质子泵送的线粒体复合体成分。其他变化出现在合成或利用 NAD⁺ 的基因中,NAD⁺ 是细胞能量和修复的关键分子。重要酶类如 CD38、PARP2 以及若干 sirtuin 并非简单地在数量上改变,而是产生了不同的 RNA 变体,这表明 NAD⁺ 产生与消耗之间的平衡在剪接层面被扭曲。被影响的基因还聚集在已知的肌肉信号通路中,包括 AMPK 和 FoxO 路径,这些通路像细胞的燃料表和应激响应器。
不同阶段以及不同物种间的共享模式
值得注意的是,许多相同的基因在确诊衰弱症的人以及仅有低肌肉量或仅有低肌力的人中都显示出剪接改变。这表明异常剪接在早期就开始出现,并跨越疾病的不同临床表现。为测试这些改变能否在动物模型中复制,研究人员用糖皮质激素地塞米松诱导小鼠肌肉萎缩,这是模拟衰弱症某些特征的常用方法。小鼠表现出握力减弱以及跑步和平衡测试成绩下降。对小鼠肌肉 RNA 进行测序时,研究组再次发现数百个基因的剪接发生改变。约五分之一与人类衰弱症基因重叠,许多相关基因参与转录、染色质结构和剪接本身的调控——这些更高级的开关可以重塑细胞的整体蛋白输出。
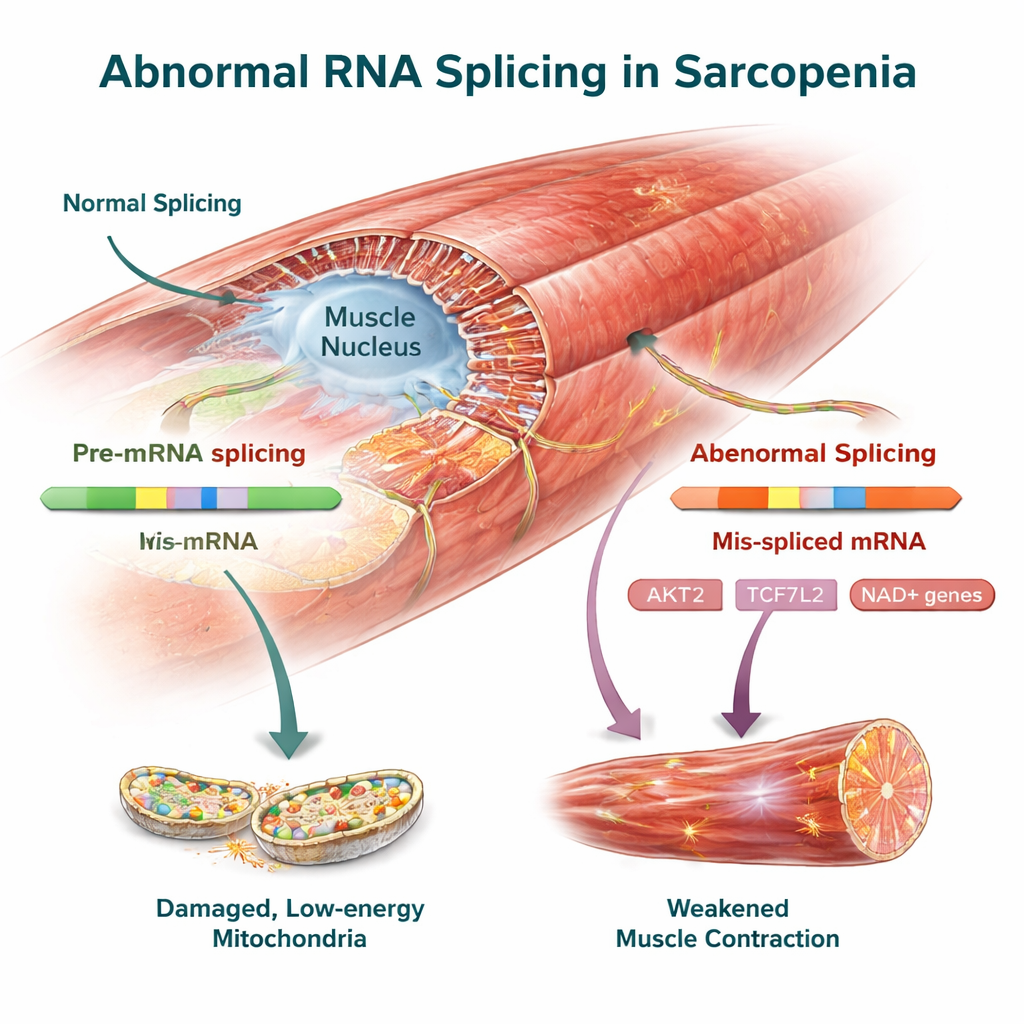
作为潜在治疗靶点的关键肌肉调控基因
在跨物种的改变中包括数个已与肌肉健康相关的基因。AKT2 是肌肉中调节生长和蛋白合成的核心因子,在人和小鼠中都显示出明显的剪接变化,可能削弱其维持肌肉质量的能力。TCF7L2(属于 Wnt 信号通路)以及有助于组织肌肉内部骨架和蛋白质质量控制的 FMNL2 和 USP40 也携带改变的 RNA 变体。研究团队在小鼠肌肉中通过实验进一步证实了这些剪接改变,加强了这些改变是真实的疾病特征而非数据分析伪像的证据。
对预防虚弱的意义
对非专业读者来说,结论是:衰弱症不仅仅是肌肉“磨损”或基因简单地被打开或关闭。它还涉及普遍的 RNA 信息错误编辑,这些信息指导肌肉细胞如何制造和维护其机器,尤其是那些产生能量和感知应激的系统。因为可变剪接原则上可以用精确设计的 RNA 类药物进行纠正,这里发现的保守剪接错误——特别是在 AKT2 和 TCF7L2 等基因中——为开发帮助老年肌肉更持久强健的疗法提供了新的线索。
引用: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
关键词: 衰弱症, 肌肉衰老, RNA 剪接, 线粒体, AKT2