Clear Sky Science · zh
甲状腺素结合球蛋白稳定性的现象学模型
这对患者和家庭为何重要
甲状腺素结合球蛋白(transthyretin,TTR)淀粉样变性是一种严重疾病,其中一种正常的血液蛋白TTR会解体,其片段可能在心脏和神经中聚集成有害沉积物。诸如塔法米司和阿科拉米司(acoramidis)等新药旨在保持该蛋白的安全四聚体形态,并已改善许多患者的结局。然而临床上有一个令人困惑的现象:接受治疗的患者血液中TTR水平常常升高超过30%,其原因并不明显。本文使用一个精简的、基于数学的模型来探讨体内可能发生的过程,以及这些过程对这些药物实际作用机制的含义。 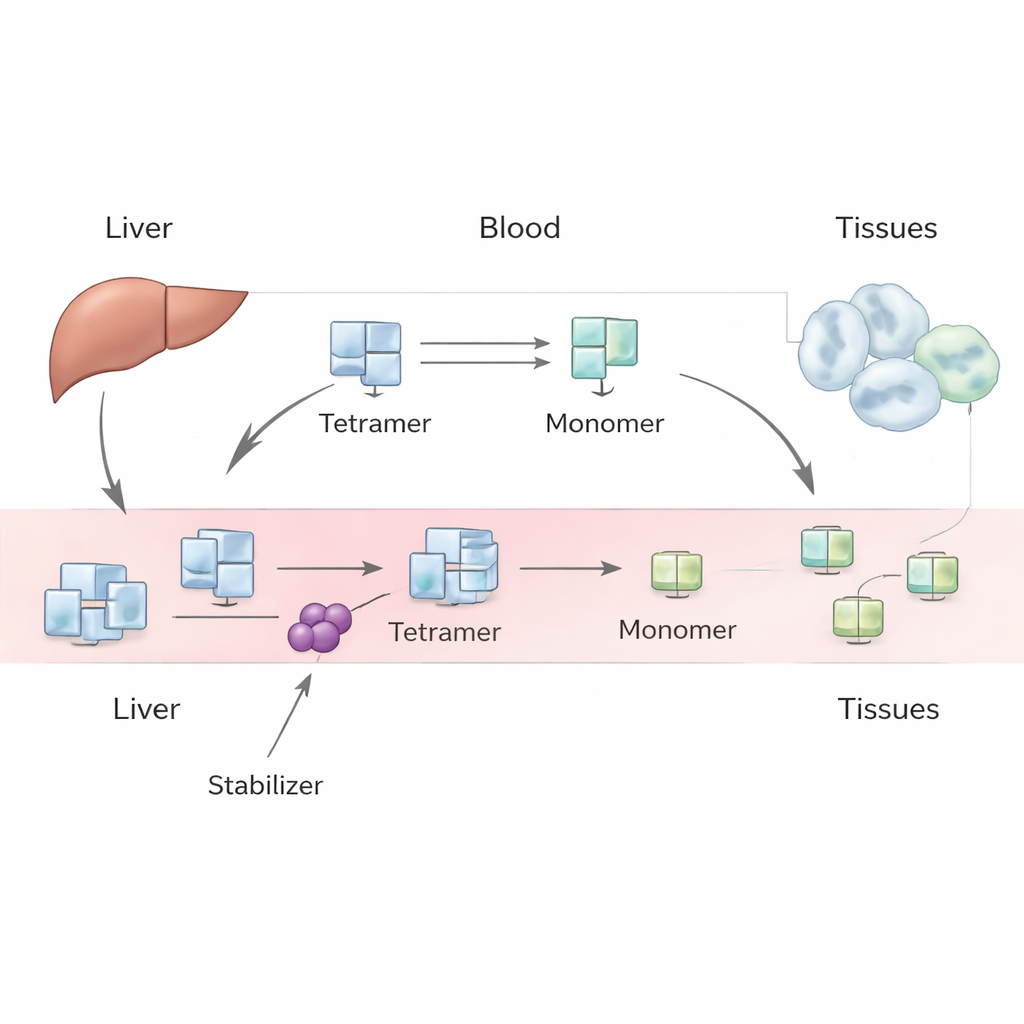
一种既可助益亦可致害的蛋白
TTR主要在肝脏合成,通常以四个相同亚基组成的稳定四聚体形式在血液中循环,负责运输甲状腺激素和维生素A。在某些情况下,包括衰老或遗传基因变异,这一四聚体可以解离为单个亚基(单体)。这些单体可能错误折叠并聚集为淀粉样纤维,损伤组织并导致心脏(心肌病)或神经(神经病变)的TTR淀粉样变性。像塔法米司和阿科拉米司这样的药物通过结合四聚体使其更难解体,从而减缓疾病进展。然而,当患者开始服用这些药物时,血液中测得的TTR水平可靠地上升,这一增幅比简单的体外实验所预测的要大得多。
为复杂系统构建一个简单图景
作者用一个现象学模型来解决这一难题——该模型关注可观测的总体行为,而非每一个微观细节。在他们的框架中,肝脏以稳定速率产生TTR四聚体,这些四聚体进入血液循环。在循环中,四聚体可以解离为单体并重新聚合,同时四聚体和单体都可以通过组织摄取和降解从血液中清除。通过为四聚体和单体写出一对质量平衡方程,研究团队考察了不同情形:单体主要重新加入四聚体、单体被迅速清除,以及两者兼顾的中间情况。他们使用历史性的人体示踪研究和现代实验室数据来估算关键量,例如四聚体的清除速率、解离速度以及药物减缓该解离的强度。
仅稳定四聚体为何不足以解释现象
有了这些估算,研究者提出了一个明确的问题:如果一种药物能完全阻止四聚体解离,血液中TTR水平会升高多少?在所有合理的参数区间内,答案都是有限的——对于典型参数值,顶多约15%,通常更少,具体取决于单体如何被处理。这远远低于临床上观察到的超过30%的增幅。即使允许对已知参数给予宽松的不确定性,差异仍然存在。因此该模型表明,仅仅减缓四聚体解离本身无法完全解释临床上看到的全部效应。与TTR合成速率、细胞摄取速率或降解速率相关的其他过程在稳定剂存在时也必须发生变化。 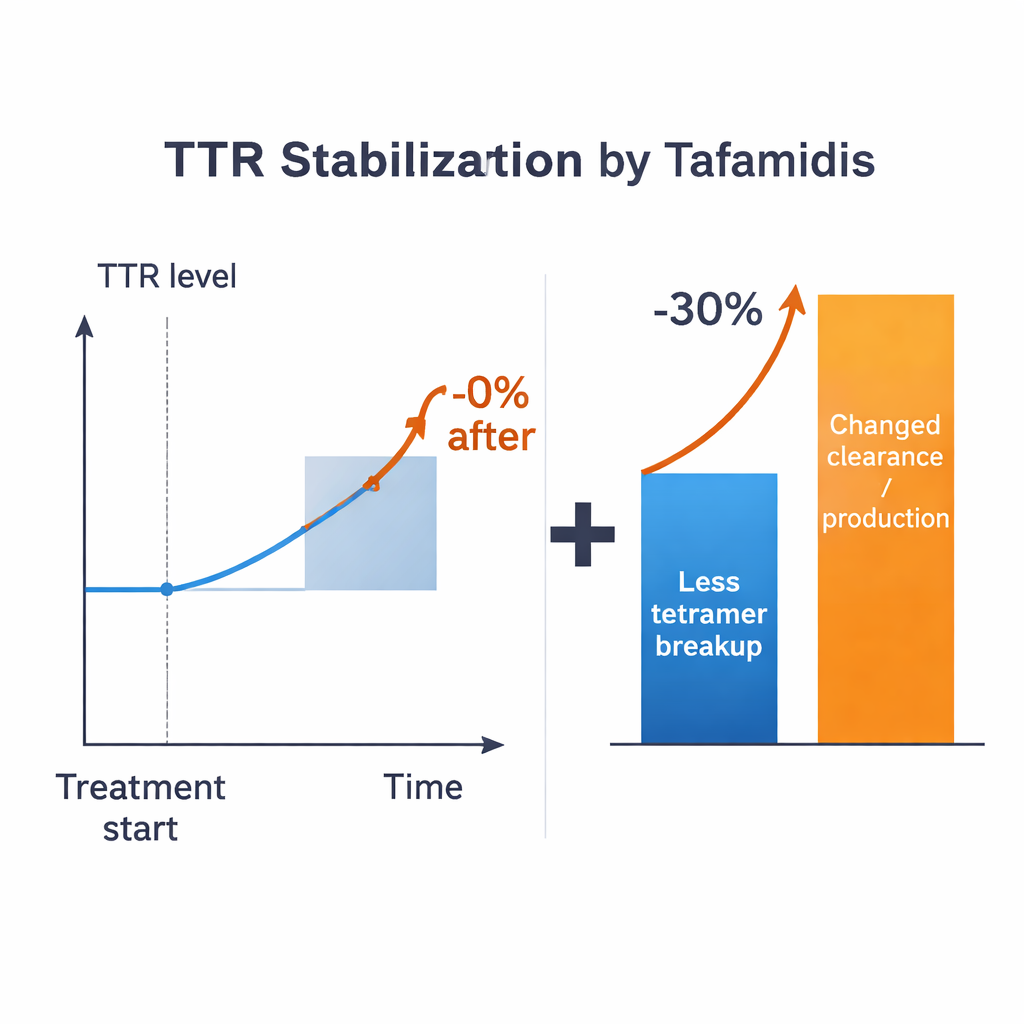
来自药物水平与巧妙实验的线索
为将药物暴露与TTR行为联系起来,作者将一个简单的塔法米司药代动力学模型(药物随时间在体内的分布)与专门的“亚基交换”测定结合。在这些实验中,将标记和未标记的TTR四聚体混合于人血浆中,亚基的渐进交换揭示四聚体解离的频率。在不同药物浓度下测量这一过程,提供了塔法米司水平与有效四聚体稳定性之间的直接数据驱动联系,而无需确切知道有多少药物与白蛋白或甲状腺激素结合。这个现象学链接被引入模型,巧妙地避开了许多生化未知数。然而即便有这种优势,计算仍将预期的TTR升高限制在临床观察值的大约一半,进一步支持了这样一个观点:清除、内化、降解甚至合成的变化也必须参与其中。
未来的方向与意义
对非专业读者而言,关键结论是这些稳定剂药物很可能不仅仅是把TTR四聚体“黏”在一起。它们很可能还影响身体如何产生、移除或回收该蛋白。作者主张,像他们这样的简单且透明的模型非常有价值,因为它们揭示了我们理解中的空白并指向具体的实验——例如直接测定单体的清除速度、不同TTR形式被细胞摄取的速率,或有无药物结合的TTR是否被差异性处理。对这些问题有更好的答案,不仅会改进TTR淀粉样变性的治疗,也可能揭示关于其他正常蛋白转变为有害聚集体的疾病的一般性规律。
引用: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
关键词: 甲状腺素结合球蛋白淀粉样变性, 蛋白质稳定化, 塔法米司(tafamidis), 药代动力学建模, 淀粉样疾病