Clear Sky Science · zh
用于肠道微菌落存活测定的数字图像分析的全自动工作流程
更快、更公正的组织读片为何重要
当医生和科学家研究放射线如何影响肠道时,他们常依赖对显微镜图像的细致检查。专家需要目视计数小肠内再生细胞形成的微小腔体,这项工作既缓慢又费力,而且出人意料地主观。本文提出了一种将大部分工作交给计算机的方法,利用现代图像分析和人工智能(AI)自动计数这些结构。目标既简单又强大:让放射学研究更一致、更快速,并且不那么依赖稀缺的专家时间。
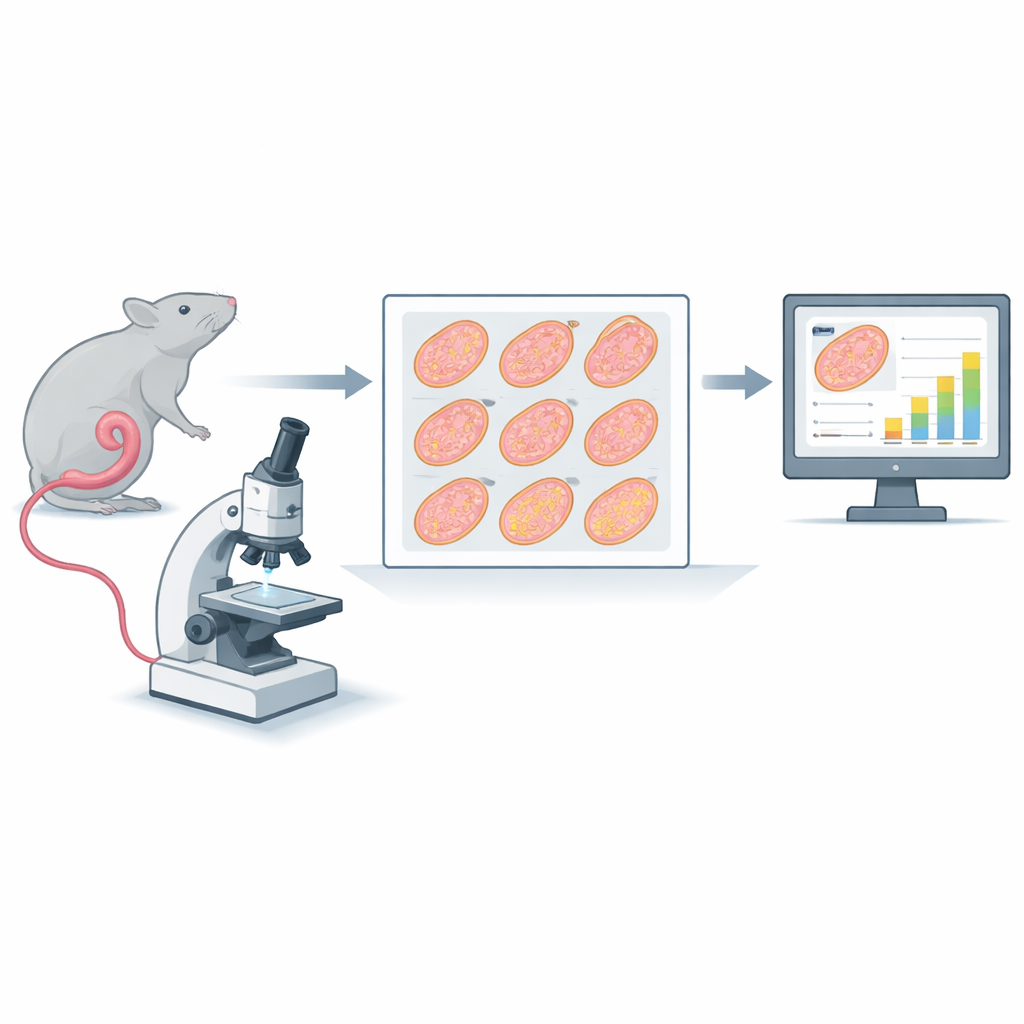
从小鼠肠道到数字切片
这项研究聚焦于一种经典检测方法,称为肠道微菌落存活测定。在该测定中,给小鼠腹部照射放射线。大约三天半后,取出一段小肠(空肠),将其切成九个短段,包埋于石蜡,切成超薄横切片,染色并以高分辨率扫描。每次扫描都会生成一幅包含九个肠组织圆形剖面的巨大数字图像。传统上,受过训练的观察者会对每个圆形区域放大并计数隐窝——沿着内缘分布、负责细胞再生的小腺腔。存活的隐窝越少,表明放射或放疗联合治疗造成的损伤越严重。
手工计数的问题
手工计数听起来很直接,但本文表明情况远非如此。十五名参与者,包括经验丰富者和新手,均按标准规则接受了什么算作隐窝的培训。即便如此,他们对相同图像的计数往往相差很大。在300多张切片中,个别计数与组平均值的平均差约为三分之一,且当隐窝很少时分歧最大。即便在三位有多年经验的专家之间,仍存在约百分之十的差异。这样的变异可能与科学家试图测量的处理效应同量级,增加了重要发现被人为噪声掩盖的风险。
自动化工作流程如何运行
作者设计了一个四步自动化工作流程,以模仿细致人工的操作,并增加额外功能。首先,计算机脚本对每张大切片图像自动裁剪出九个组织圆形,并对图像大小和染色差异进行调整。第二,名为 nnU-Net 的深度学习模型在每个圆形中标注属于隐窝的像素,生成黑白“掩膜”以表示可能的隐窝区域。第三,自定义算法勾画每个区域的边界,过滤掉过小的不可能是真正隐窝的噪点,并且——关键在于——尝试分离那些实际包含多个相邻隐窝的融合区域。最后,图形界面让人工审阅者在原图上看到轮廓覆盖层,几次点击即可修正错误,并自动保存最终计数和测量结果。
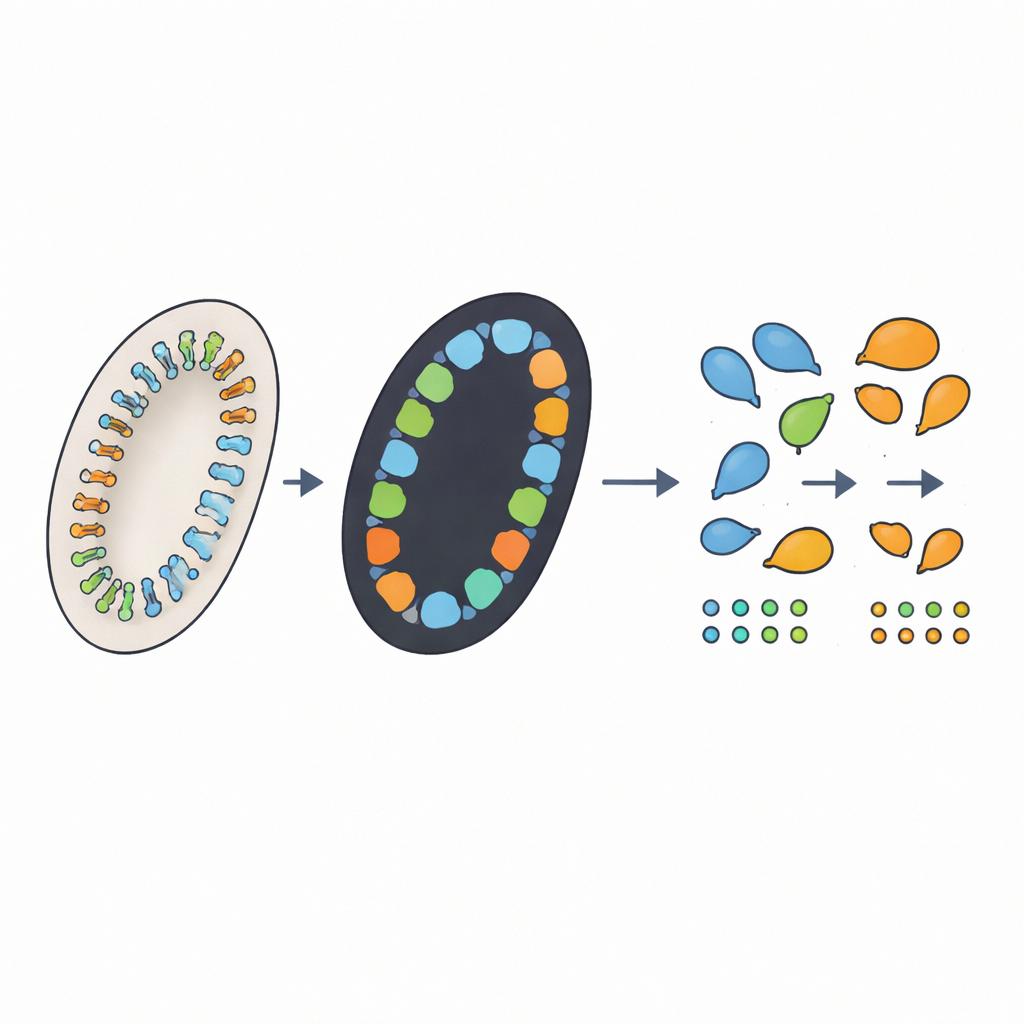
匹敌人类专家,但用时是几小时不是几周
为评估自动工作流程的表现,研究团队将其计数与多个数据集上的专家评估进行了比较。对于用于训练系统的图像,深度学习步骤在标注隐窝区域方面精度很高,计数算法在加入融合隐窝分离步骤后,通常能与专家共识相差仅几处隐窝。在训练集之外的新图像上,自动计数与三位专家平均值的差异约为百分之十——这与专家之间的差异相当或略优。当专家通过界面对自动结果进行复核和修正时,通常每张图像所需不到一分钟。总体而言,处理涉及60只小鼠的完整实验通常只需几小时的计算时间和几分钟的人工作业。
描述肠道损伤的新方法
由于该工作流程分析完整的数字图像,它可以轻松测量手工难以跟踪的特征,例如肠道周长的长度或每个隐窝的面积。作者探讨了是否通过这些特征调整隐窝计数——本质上是询问“每单位肠长的隐窝数”或“按隐窝大小调整的隐窝数”是否能更好地反映放射损伤——以期获得更清晰的信号。在本研究中,没有一种替代度量能持续优于原始隐窝计数,但该方法展示了自动图像分析如何为更丰富、更细致的组织损伤标记物打开大门。
这对未来研究的意义
对非专业读者而言,关键结论是:研究者构建了一个实用的数字助手,能够以接近资深专家的可靠性读取复杂的组织切片,但速度更快且一致性更高。通过减少繁琐的手工工作并平滑人为差异,这一自动化系统可以使肠道放射研究更稳健、更容易在不同实验室之间进行比较。作者还指出了进一步改进的明确途径,例如使用直接分离相邻隐窝的模型。超越这一单一测定,他们的框架为自动化其他显微评估提供了范式,使病理学朝着这样一个未来发展:经过审慎的人类判断由透明且值得信赖的AI工具支持——而非被替代。
引用: Baikalov, A., Wang, E., Neill, D. et al. A fully automated workflow for the digital image analysis of the intestinal microcolony survival assay. Sci Rep 16, 9633 (2026). https://doi.org/10.1038/s41598-025-34719-4
关键词: 肠道微菌落存活测定, 自动化组织病理学, 深度学习图像分析, 放射性诱导的肠道损伤, 隐窝计数工作流程