Clear Sky Science · zh
LBPs 纳米颗粒通过抑制 YAP1 表达诱导铁死亡并改变能量代谢,从而抑制乳腺癌进展
莓果成分遇上乳腺癌
很多人把枸杞当作茶饮和零食混合物中的“超级食物”。本研究把目光远远超出货架,探问这些浆果中的关键多糖链能否被制成精准、微小的药物来对抗乳腺癌。通过研究这些天然分子被封装进纳米颗粒并在体外传递到乳腺细胞时的行为,研究者揭示了一种新途径:促使癌细胞走向自我毁灭,同时让正常细胞更不易演变为恶性。
开启与关闭生长开关
研究核心是名为 YAP1 的蛋白,它在细胞内像一个生长开关。当 YAP1 过度活跃时,正常乳腺细胞会表现出更多癌样特征:增殖加快、抗凋亡、细胞骨架重组并增强侵袭能力。研究组让正常乳腺细胞额外表达 YAP1,观察到以上危险变化,同时细胞的能量工厂线粒体功能增强。当用提取自枸杞的枸杞多糖(Lycium barbarum polysaccharides,LBPs)处理这些细胞时,这些癌样行为显著减弱,YAP1 水平下降。换言之,枸杞糖能将这个生长开关拨回较低水平。
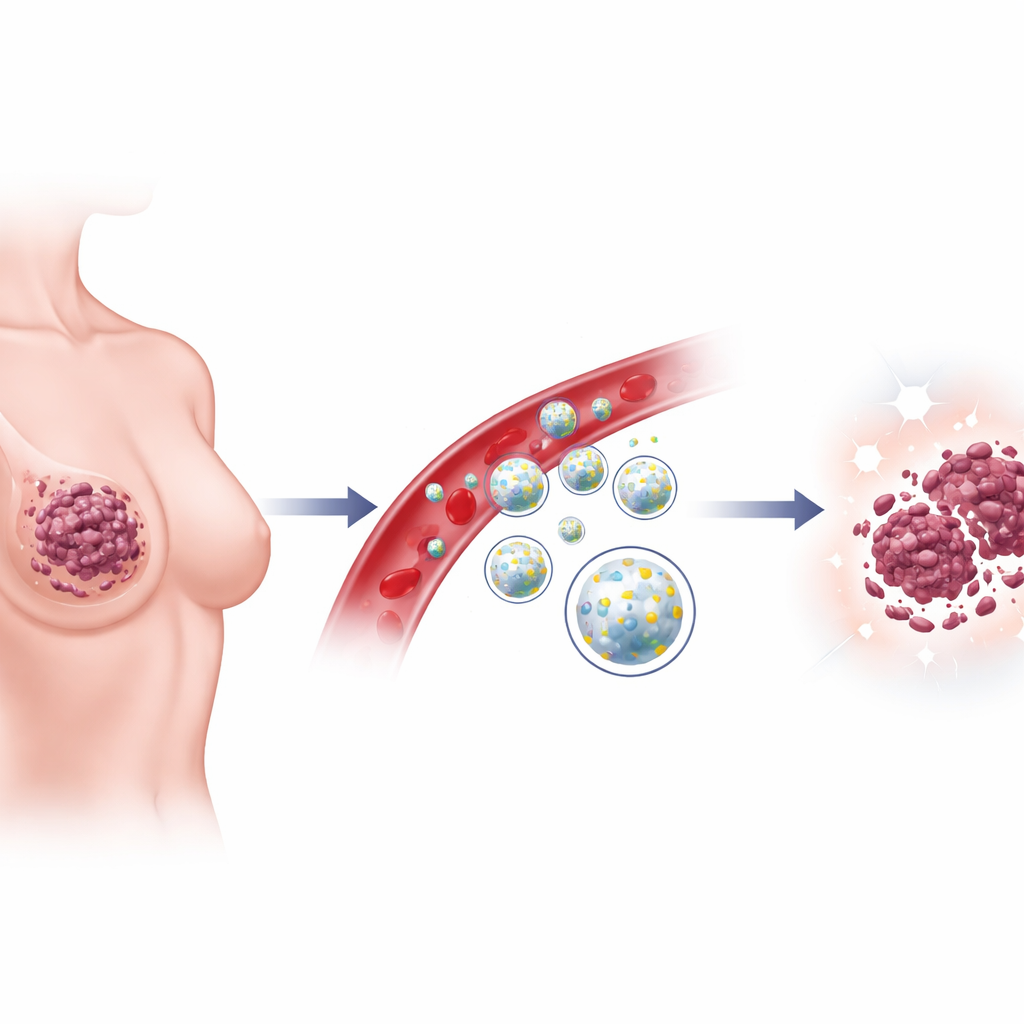
将癌细胞推向一种特殊死亡方式
随后研究者转向侵袭性强的乳腺癌细胞。同样,高 YAP1 水平与快速增殖、强抗凋亡能力和强侵袭性并存。LBPs 处理减缓了细胞分裂,削弱了细胞内支架并降低了侵袭性。更重要的是,这些化合物促使癌细胞走向铁死亡——一种由铁和脂质氧化损伤驱动的细胞死亡形式。通常保护细胞免受此类死亡的标志物下降,而有利于铁死亡的信号上升,细胞内铁含量增加。用基因手段降低 YAP1 也产生了类似效果,将这些基因工具与 LBPs 组合使用时作用更明显,这将枸杞化合物的效应紧密关联到这一单一生长开关上。
构建更智能的递送载体
单独的 LBPs 并非理想药物:它们分子量大、亲水、易降解且在体内迁移效率低。为克服这些问题,研究者将其包裹在一种可生物降解的聚合物 PLGA 制成的微小球体中,制备出装载 LBPs 的纳米颗粒(LBPs NPs)。这些颗粒尺寸均一、在液体中稳定,并被乳腺癌细胞容易吞噬,积累在细胞体内。与游离 LBPs 相比,纳米颗粒形式更强地抑制癌细胞生长、破坏其细胞骨架、降低侵袭性并提高程序性细胞死亡的比例。纳米颗粒在降低 YAP1 及其伙伴 TAZ 的同时,还增加了被磷酸化标记为“关闭”状态的 YAP1 变体,作用更显著。
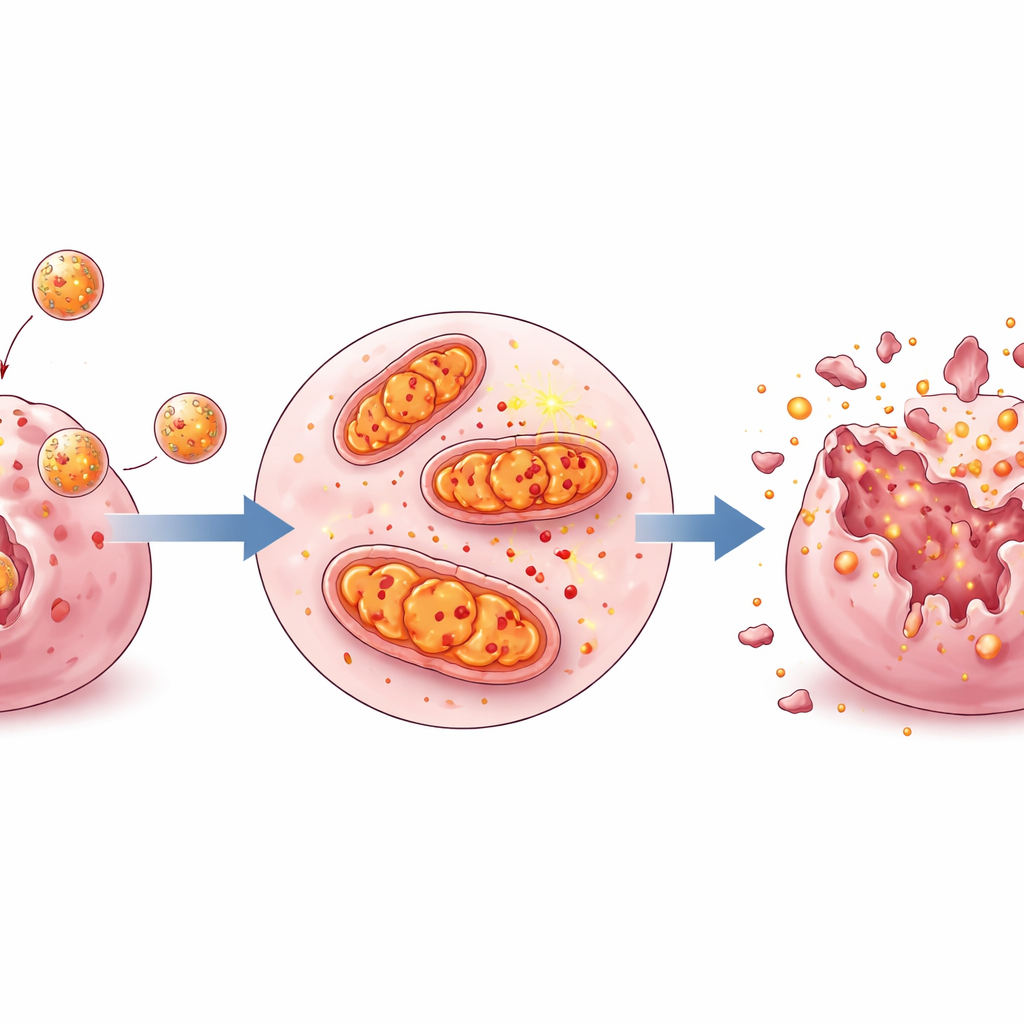
耗尽细胞能量并搅动铁稳态
透视被处理的癌细胞,团队发现 LBPs,尤其是 LBPs NPs,削弱了线粒体功能和能量产生。线粒体膜电位——衡量这些能量工厂功能的关键指标——在处理后下降,细胞产生的 ATP(基本能量货币)减少。与此同时,铁敏感染料与染色显示细胞内铁含量增加,使其更易触发铁死亡。通常保护细胞免受铁驱动损伤的蛋白减少,而促进此类损伤的蛋白增加。当研究者加入已知的铁死亡阻断剂时,这些变化部分被逆转,证实这些纳米颗粒确实在驱动这种特定形式的细胞死亡。
这对未来治疗意味着什么
通俗地讲,该研究表明:经精心工程化的枸杞多糖通过纳米颗粒递送,能够关闭乳腺细胞中的关键生长驱动因子,耗尽癌细胞的能量并将其推向受控的铁依赖性崩溃。该工作在细胞培养皿中完成,而非动物或患者体内,因此它属于早期的概念验证步骤,而非现成的治疗方案。尽管如此,研究指向了一个前景:将天然化合物与智能递送系统配对,以选择性地解除癌细胞的生长机制并激活其内在的自毁程序。
引用: Zhao, F., Yang, S., He, T. et al. LBPs NPs suppress breast cancer progression by inhibiting YAP1 expression to induce ferroptosis and alter energy metabolism. Sci Rep 16, 9257 (2026). https://doi.org/10.1038/s41598-025-34454-w
关键词: 乳腺癌, 纳米颗粒, 枸杞多糖, 铁死亡, Hippo YAP1 通路