Clear Sky Science · zh
在体外成熟牛复合体卵母细胞期间有针对性地稳定低氧诱导因子1-α(HIF1A)可提高囊胚率
为什么调整卵细胞的氧感应很重要
现代养牛育种在很大程度上依赖实验室制备的胚胎,但成功率远非百分之百:只有大约三分之一的卵细胞能达到关键的囊胚阶段,届时才适合移植回母牛。这项研究提出一个看似简单但对动物育种和辅助生殖具有广泛意义的问题:如果我们更贴近卵巢内卵细胞自然经历的低氧环境——通过温和增强一种关键的氧感应蛋白——是否能帮助更多胚胎成功发育?
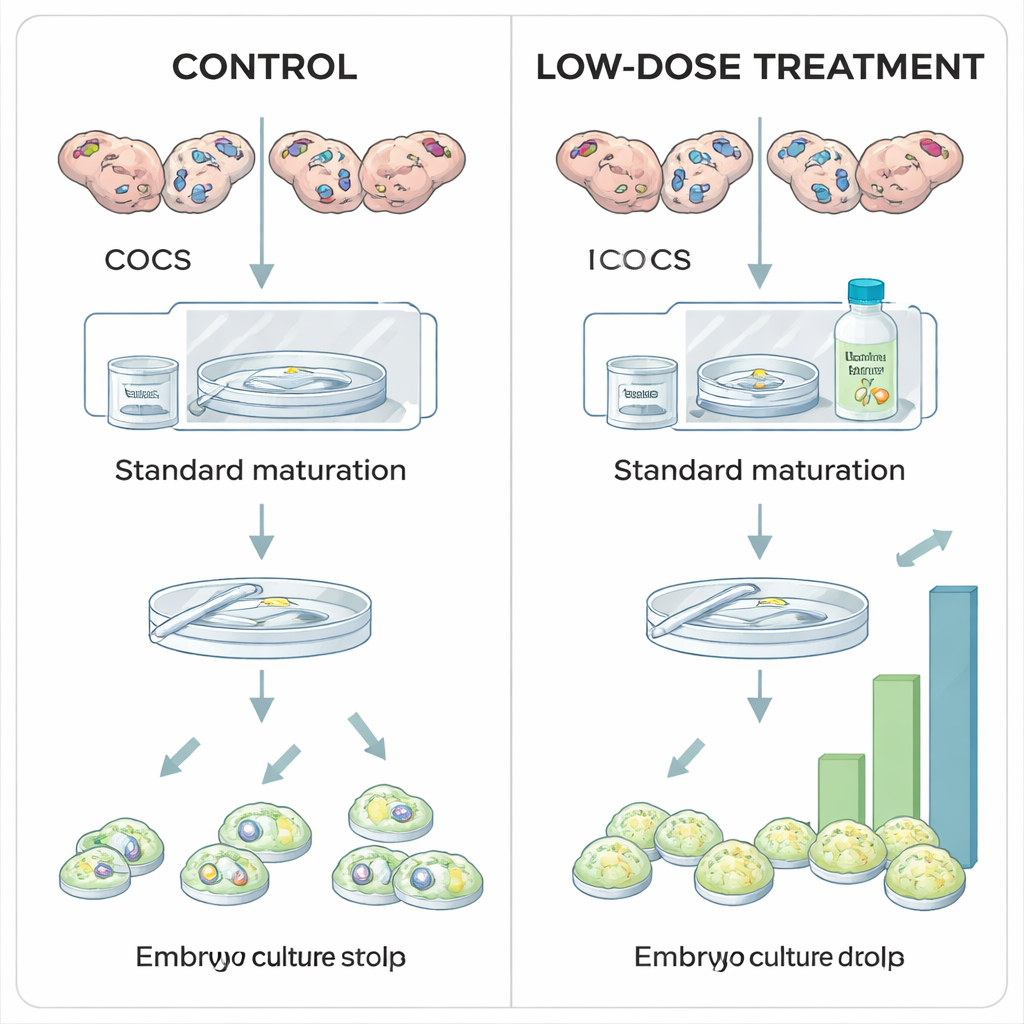
生命始于低氧的微环境
在卵巢内,每个发育中的卵子被一簇被称为冠状细胞的支持细胞包裹,二者共同形成冠状-卵母细胞复合体。尽管随着卵泡生长,卵巢的血液供应增多,但血管并不会直接延伸到卵子周围的最靠近区域。氧气必须通过扩散进入,形成一个包围成熟卵子的轻度低氧(缺氧)口袋。在这一小环境中,细胞内的感应器HIF1A通过调节代谢和激素生成帮助细胞适应。早期研究表明阻断HIF1A会损害卵子成熟并大幅降低胚胎形成,凸显出该蛋白作为卵子能力(即卵子被受精并发育成健康胚胎的能力)的核心协调因子的地位。
用药物微调卵子的氧感应器
研究人员探讨了在牛卵体外成熟期间适度稳定HIF1A是否能提高胚胎产出。在标准的体外方法中,冠状-卵母细胞复合体通常在常压空气氧浓度下成熟,更多出于操作便利而非生物学考虑。本研究将从屠宰场卵巢采集的卵子分组,并在24小时的成熟期内暴露于不同剂量的Roxadustat(已用于人类治疗贫血的药物)。Roxadustat通过抑制一类称为脯氨酰羟化酶(PHDs)的酶发挥作用,这些酶在氧气充足时会标记HIF1A使其被降解。通过抑制PHDs,Roxadustat使HIF1A蛋白在较高氧水平下仍能积累,部分重现卵子在体内感受到的低氧信号。
合适剂量增加囊胚率,剂量过高有害
当团队检查处理后卵子和胚胎的表现时,出现了清晰的模式。低剂量Roxadustat(25微摩尔)并不改变完成成熟的卵子数量或开始分裂的受精卵数量,但显著提高了达到囊胚阶段的比例。换言之,早期步骤未受影响,但更多胚胎成功完成成为囊胚的艰难旅程——这表明适度的HIF1A稳定化改善了卵子的内在质量。相反,最高剂量(100微摩尔)降低了能够完成成熟的卵子百分比;当相同抑制剂在之后的为期八天的胚胎培养期间使用时,高剂量大幅减少了囊胚形成而不改变早期细胞分裂。这些发现表明,在成熟期“恰到好处”的HIF1A活性是有益的,而过多或过长时间的激活则有害。
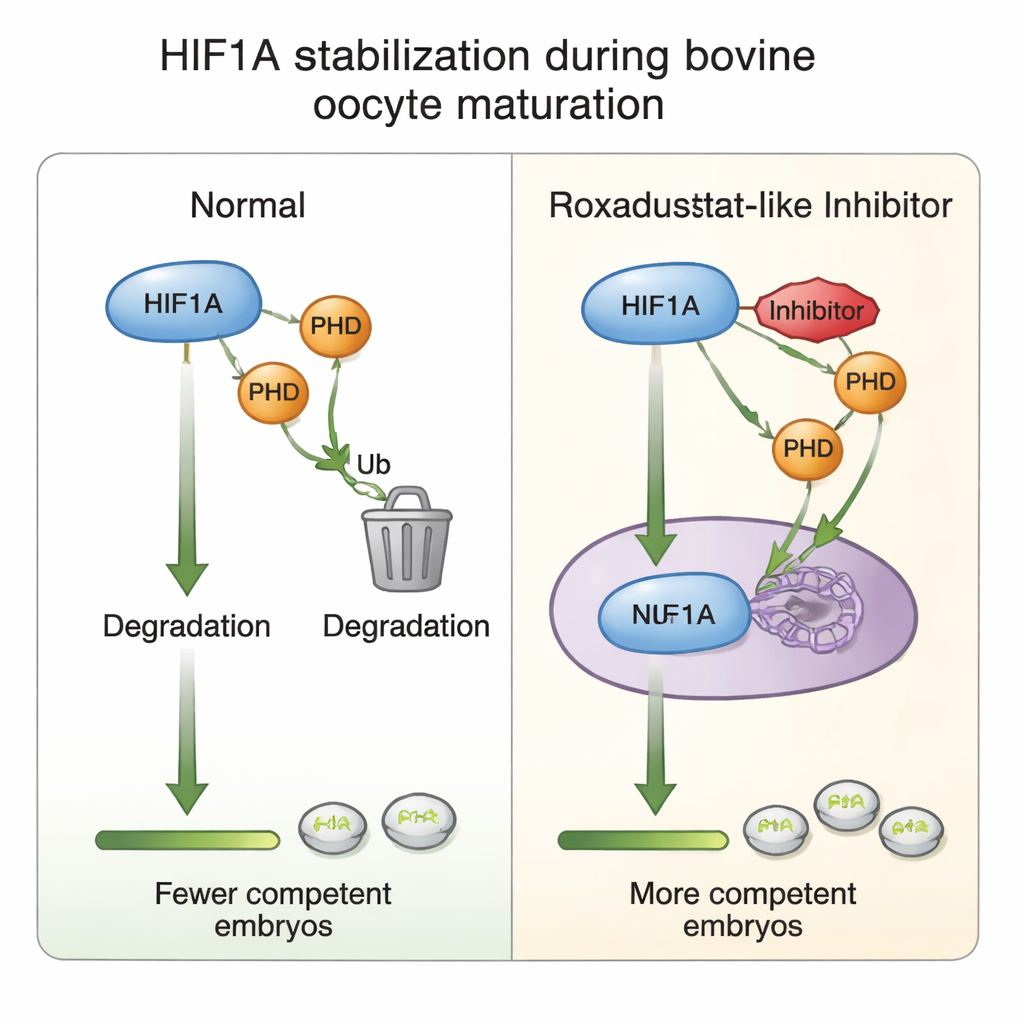
在卵子的支持细胞内部发生了什么
为了弄清这种化学微调如何起作用,作者检测了包围每个卵子的冠状细胞。他们发现总体上成熟过程会提高HIF1A基因的活性,但加入Roxadustat反而使HIF1A信使RNA下降而HIF1A蛋白水平保持稳定——这暗示细胞在蛋白被充分稳定后可能会降低基因产出,这是一种内在的防过度激活制动机制。作为最对氧敏感的PHD酶,PHD2水平对药物的响应而上升,强化了其作为氧感应回路一部分的角色。在更高药物剂量下,细胞增殖标志物以及帮助冠状细胞围绕卵子扩展的粘性基质标志物减少,这与观察到的成熟和胚胎形成下降一致。所有这些支持了这样一个观点:细致平衡的HIF1A活性微调了卵子与冠状细胞之间的对话,从而支撑随后发育的成功。
对动物育种及其他领域的启示
这项工作表明,在体外成熟的短暂窗口内温和稳定卵子的氧感应器可以显著提高并稳定牛的囊胚产出,而不会改变受精或早期裂解。在实际操作上,这可能意味着对育种计划来说,使用一种有针对性的药物而非粗糙地改变氧浓度或使用更具毒性的化学物质,能够带来更可靠的胚胎生产。该研究还强调了对人类生育治疗也具有的更广泛教训:模仿卵巢那种微妙的低氧环境不仅仅是把氧气调高或调低,而是尊重像HIF1A这样的信号分子之间的精细平衡。细致地调整这种平衡,而不是将其推向极端,可能是获得更健康胚胎的关键途径。
引用: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
关键词: 体外胚胎生产, 卵母细胞成熟, 低氧信号传导, HIF1A 稳定化, 牛生殖