Clear Sky Science · zh
借助面向 GPU 集群的高效开源可扩展求解器迈向心脏电生理数字孪生
为什么构建虚拟心脏很重要
医生在治疗心律失常时常常有部分信息缺失:他们可以在体表测量到电信号,但很难直接观察这些信号在心脏深处的传播。本研究介绍了一套强大的新型计算工具,能够详尽地模拟个体心脏的跳动,速度足以探索大量“如果……会怎样”的情形。通过将逼真的心脏解剖与最先进的图形处理器相结合,作者让我们更接近在个体患者心脏的数字副本上进行安全、低成本的虚拟实验。
从简单模型到数字孪生
现代心脏模拟可以表示从单个细胞到整个器官的活动,但要忠实再现电信号在心脏中的传播既在数学上复杂又在计算上耗费巨大。医学的一个关键目标是“心脏数字孪生”:一个模拟特定患者心脏的个性化计算模型,可用于在临床使用前测试药物、器械或起搏策略。为了使这成为可能,运行这些模拟的软件必须既快速又准确,包含重要的解剖结构,并且应以开源方式提供,以便全球研究者能够检查、改进和重用。
捕捉心脏的隐蔽布线
这项工作聚焦于一个名为 monoalg3d 的开源模拟器,该模拟器模拟电信号如何在心肌及其专门的传导网络中传播。该网络被称为浦肯野系统,它将触发心跳的信号从上游传导通路快速传递到分布在心室内表面的众多微小连接点。在每个这样的交界处,一条细小的浦肯野纤维必须激发体积更大的心肌,这会引入自然的延迟,并在某些条件下带来传导阻滞或异常的风险。作者改进了 monoalg3d,使其更真实地表示该布线及其交界,包括浦肯野向心肌传播与心肌反向进入网络之间的非对称性。
将超级计算机与 GPU 打造成心脏实验室
为了快速运行如此精细的模型,团队重新设计了模拟器利用硬件的方式。他们重构了数值核心,使局部细胞动力学和跨心脏的电压扩散都直接在图形处理单元(GPU)上求解——这些设备最初用于图像渲染,但现在广泛用于科学计算。通过为 GPU 库精心组织数据并避免频繁的 CPU 与 GPU 之间传输,他们展示了完全基于 GPU 的配置在标准基准测试上相比传统的仅 CPU 版本可将速度提升近 11 倍。他们还引入了一种新的紧凑输出格式以大幅降低存储需求,并实现了一种消息传递功能,能够在超级计算机上并行启动数百个模拟,每个模拟探索不同的一组生理参数。
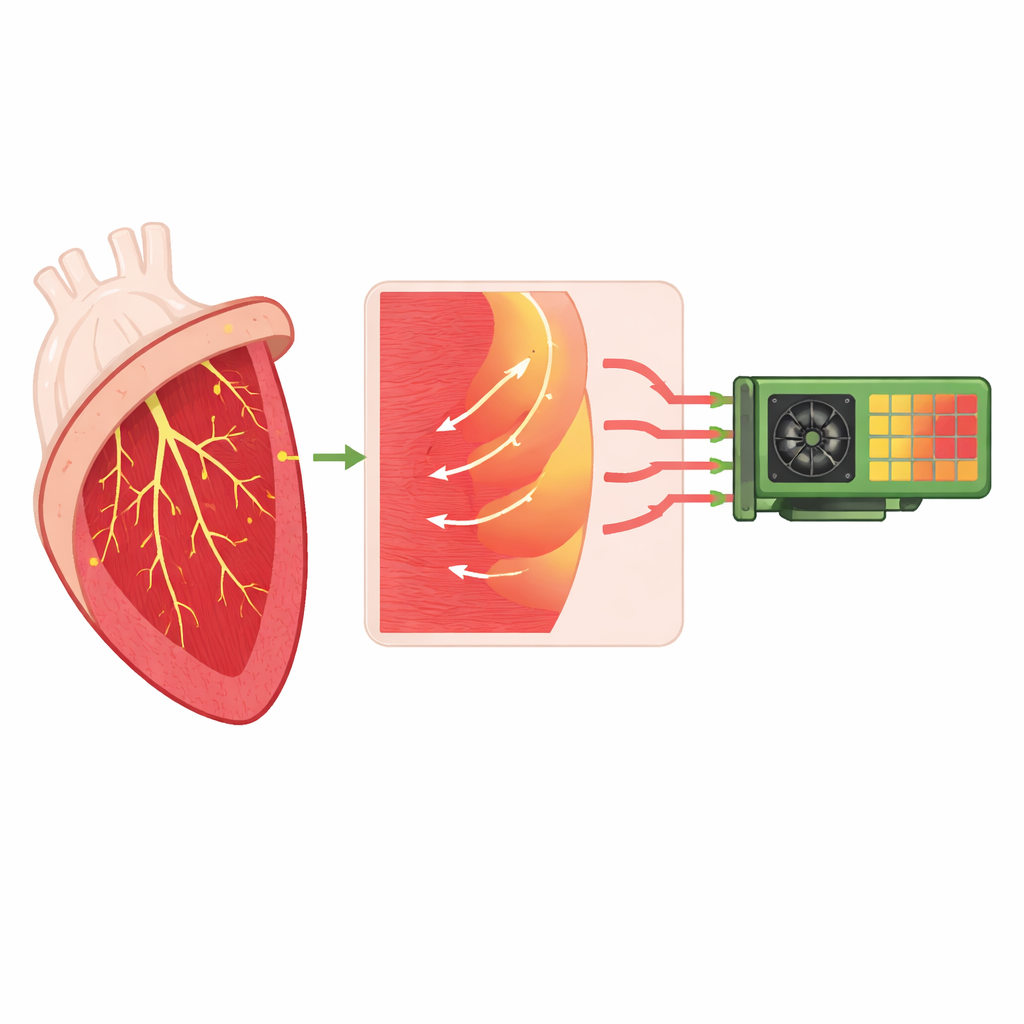
教会虚拟心脏去匹配真实患者
除了原始速度之外,作者还测试了改进的求解器是否能支持真实的患者特异性模拟。利用来自医学成像的人体心脏三维重建,他们附加了一个合成的浦肯野网络并调整关键交界参数:每个连接处的电阻以及每个浦肯野末端激发的相邻心肌区域数量。他们自动遍历这些数值的数百种组合,从主传导束处施加刺激启动模拟,测量每个交界处的小延迟以及胸部上的心电图(ECG)信号。对于高分辨率的心脏网格,他们识别出能够产生生理上合理的激动时间和与真实患者记录高度相关的 ECG 波形的参数组合,同时即便在并发执行 512 次运行时,单次模拟时间仍可控制在数小时内。
许多内部不同但体外相似的心脏
一个有趣的结果是,不同的内部传导配置和交界强度可能产生非常相似的体表 ECG。换言之,几种不同的数字心脏可以同样符合相同的临床数据。作者指出某些浦肯野交界尤其有影响力,在同样拟合良好的模拟中其局部延迟可出现显著差异,而整个心室的激动时序仍保持稳定。这种非唯一性表明,未来的数字孪生框架需要额外的数据或约束——例如更详尽的成像或侵入性测量——来确定给定患者最可能的内部配置。
这对未来医疗意味着什么
总之,本研究提供了一个可自由获取的 GPU 加速模拟器,能够处理细致的心脏解剖、逼真的传导布线,并在现代计算集群上批量运行大量个性化模拟。对非专业读者而言,关键信息是:运行快速且高保真、类似个体患者的虚拟心脏实验(包括心脏内部布线交界处的微小延迟)正变得可行。尽管仍需更多工作以完全个性化这些模型并解决内部不确定性,但此处引入的工具构成了未来基于数字孪生的心脏病学诊断、风险评估与治疗规划的重要基石。
引用: Berg, L.A., Oliveira, R.S., Camps, J. et al. Toward cardiac electrophysiology digital twins with an efficient open source scalable solver on GPU clusters. Sci Rep 16, 9619 (2026). https://doi.org/10.1038/s41598-025-33709-w
关键词: 心脏数字孪生, 心脏电生理模拟, 浦肯野传导系统, GPU 计算, 个性化心脏病学