Clear Sky Science · zh
雄激素使卵泡细胞外基质功能失调并增加小鼠卵巢中的促纤维化基因表达
这对女性健康为何重要
许多患有多囊卵巢综合征(PCOS)的女性面临月经不调和受孕困难,但更隐蔽的变化发生在卵巢的组织结构中。本研究利用小鼠卵巢探讨一种称为雄激素的“男性型”激素如何重塑围绕发育中卵泡的微观支撑框架。该研究有助于解释为何PCOS患者的卵巢常表现出更多结缔组织和更高的僵硬度,以及这种改变的微环境如何干扰正常卵子发育与排卵。
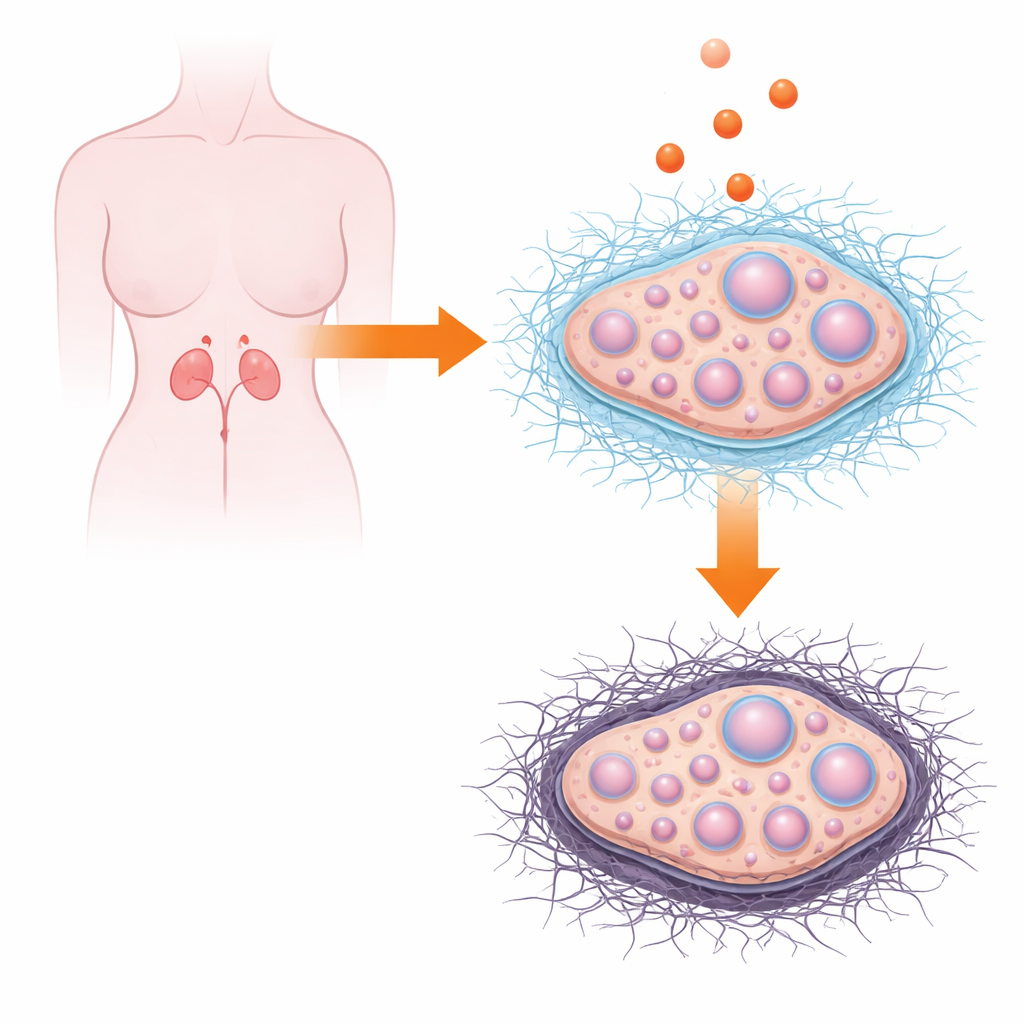
卵巢的隐秘支撑网络
身体的每个器官都建立在复杂的“分子脚手架”之上,即细胞外基质。在卵巢中,这种由蛋白质和多糖构成的网状结构包绕并填充在卵泡之间,卵泡是容纳发育中卵子的微小液囊。基质并非静止:它在每个生理周期中持续改建,使卵泡能够生长、形成液腔并最终释放成熟卵子。既往对PCOS女性的研究表明,她们的卵巢常含有额外的结缔组织并显得更致密,暗示存在瘢痕化或纤维化。作者旨在鉴定小鼠卵巢中与基质相关的基因与通路,并研究当卵泡在体外直接暴露于雄激素时这些基因如何反应。
绘制卵巢中的构建模块
研究者首先列出了一组与结构性基质蛋白、修饰这些蛋白的酶以及帮助细胞感知并响应机械力的分子相关的基因。使用小鼠卵巢,他们确认许多这些基因在不同卵泡阶段、周围间质组织,甚至在卵母细胞中均有活性。在显微镜下,若干关键蛋白(如胶原、层粘连蛋白和一种肌动蛋白形式)在生长卵泡周围形成环状层,而其他蛋白则将细胞与基质连接并有助于纤维交联。这一模式表明卵巢的支撑网络被精细组织以包裹每个卵泡,提示这些环层或周围网状结构的任何破坏都可能改变卵泡的生长方式及其环境的硬度。
雄激素使局面向瘢痕化倾斜
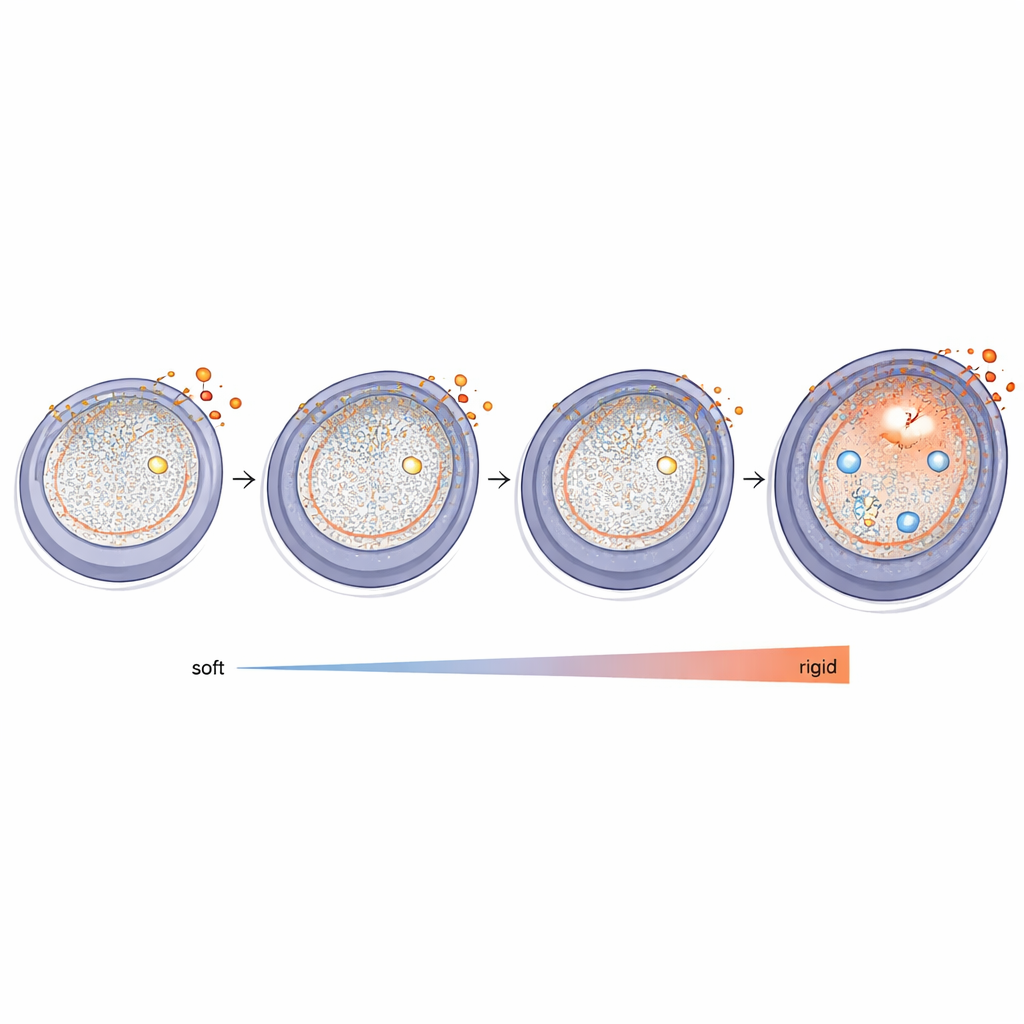
接着,团队分离出早期小鼠卵泡,并在有无强效雄激素二氢睾酮的条件下进行培养。如早期研究所见,暴露于雄激素的卵泡增长更快。但在这种生长加速的背后,其基因活性向更纤维化的方向转变。一天后,许多结构性基质基因的活性下降,尤其是构成卵泡外边界的薄基底膜成分。三天后,某些成分出现反弹或上调,包括弹性蛋白和α-平滑肌肌动蛋白,这些都与僵硬的瘢痕样组织相关。卵泡还增强了能加固胶原纤维或重塑富糖基质的酶类基因表达,这与组织从柔软向更致密、坚韧环境的转变一致。
机械信号变得更为显著
研究还聚焦于随着周围环境变硬,卵泡如何感知并转译机械线索。雄激素处理的卵泡在Hippo通路的若干核心组分上表现出更高活性,该信号网络已知对组织张力有响应并参与限制器官大小。该通路的下游靶点,包括结缔组织生长因子和其他与基质相关的信号,也被上调,表明机械信息已传入细胞核并改变基因程序。与此同时,两个TGF-β家族成员(在许多器官的纤维化反应中是强效驱动因子)也被上调。总的来看,这些变化提示一个反馈回路:雄激素不仅改变基质,还在卵泡细胞内增强促纤维化和机械敏感性信号。
这对PCOS意味着什么
对非专业读者来说,核心信息是过量雄激素可以推动卵泡构建更僵硬、更像瘢痕的包膜,并激活强化这种改变的细胞系统。在高雄激素水平与卵巢纤维化常并存的PCOS背景下,这些发现支持这样一种观点:激素不仅仅是改变血液中的激素水平,它们也在主动重塑卵巢的物理景观。更硬的卵巢环境可能使卵泡难以正常发育与排卵,从而部分解释PCOS相关的不孕问题。理解这些组织层面的改变或能为旨在软化卵巢基质或调节机械信号的治疗开辟新途径,以补充仅针对激素水平的疗法。
引用: Hopkins, T.I.R., Lerner, A., Dunlop, I.E. et al. Androgen dysregulates the follicular extracellular matrix and increases pro-fibrotic gene expression in the mouse ovary. Sci Rep 16, 8974 (2026). https://doi.org/10.1038/s41598-025-32927-6
关键词: 多囊卵巢综合征, 雄激素, 卵巢纤维化, 细胞外基质, 卵泡发育