Clear Sky Science · zh
使用整合的网络药理学与计算方法将天然产物重新用于脊髓小脑性共济失调3型的研究
这项研究为何对患者和家庭重要
脊髓小脑性共济失调3型(SCA3)是一种罕见的遗传性脑病,会逐步剥夺患者的平衡、协调能力和独立生活能力。目前尚无治愈方法,也没有获批能阻止病情进展的药物。本研究探讨是否可以借助强大的计算工具,将已存在于自然界的化合物——许多来自传统医药——智能化“再利用”,以期为新疗法开辟更快且可能更安全的路径。
在自然中寻找有用分子
研究人员聚焦于天然产物:存在于植物及其他生物体中的化学物质,长期以来一直是现代药物的重要来源。他们收集了15种先前在细胞或动物模型中报道能缓解SCA3特征的有前景天然化合物。通过专门的数据库,他们预测了每种化合物可能作用的人体蛋白,并单独汇编了数千个与SCA3相关的基因。通过比较两组数据,研究团队锁定了239个重叠的靶点——既参与疾病过程又可能被这些天然分子影响的蛋白质。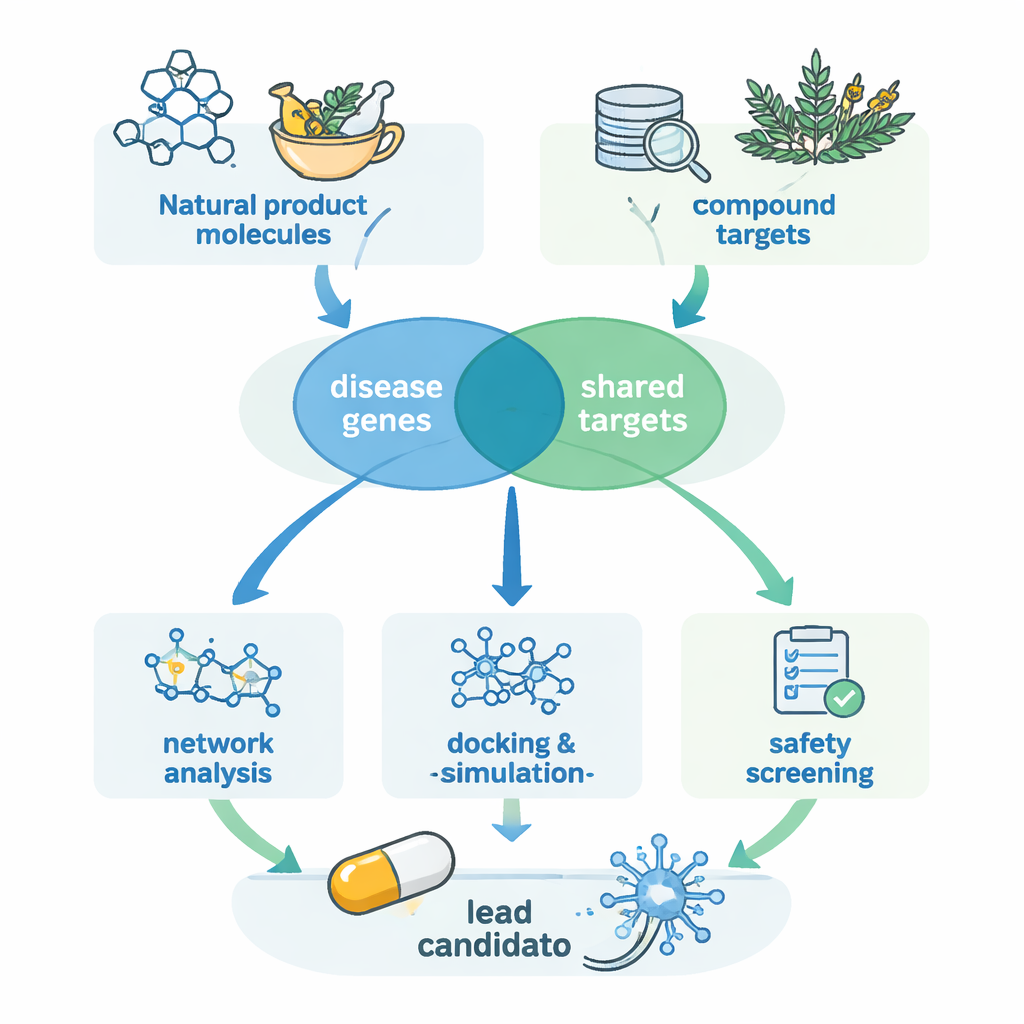
绘制疾病的薄弱环节图谱
接着,团队构建了大型的“相互作用图”,展示这239种蛋白在细胞内如何相互交流。在这些图谱中,有些蛋白就像交通网络中的枢纽,连接着多条路径。其中两个枢纽——AKT1和TP53——尤其突出。研究人员随后分析了哪些细胞通路——一系列相互关联的生化反应——受影响最大。其中,称为MAPK信号传导的通路尤为重要,该通路已被公认为在脑细胞存活、应激反应与退行性变化中起关键作用。许多天然化合物似乎会影响该通路,提示它们可能通过这一共同途径保护SCA3中的神经元。
对藏红花苷进行(虚拟)显微镜下的检视
在所有测试分子中,藏红花苷——一种来自藏红花的明亮橙色色素——在对AKT1和TP53的预测结合能力上最强。为深入了解,团队使用了基于计算的对接方法,将每种化合物的虚拟模型嵌入蛋白的三维结构中,类似于在锁中试钥匙。藏红花苷比一种名为troriluzole的参考实验用药更好地“匹配”了AKT1和TP53,形成了更稳定的接触和更强的相互作用。随后科学家运行了长时间的分子动力学模拟,这些模拟模拟了在水性、类体内环境中原子随时间的运动。模拟显示蛋白–藏红花苷复合体保持稳定,形成了许多氢键并达到低能量、稳态构象——这些特征与强稳的相互作用一致。
这如何有助于保护脑细胞
AKT1和TP53在决定受压的神经元是恢复还是死亡方面发挥作用。在SCA3中,异常的ataxin-3蛋白扰乱了包含这两位关键调节因子的信号网络,使细胞更倾向于损伤和丧失。计算模型表明,藏红花苷可能结合到AKT1中与其活性相关的区域,以及结合到TP53的DNA结合域,从而微妙地改变这些蛋白的行为。早期在其他脑病模型中的实验室研究显示,藏红花苷可降低氧化应激、缓和炎症、稳定线粒体(细胞的能量工厂)并调节细胞死亡通路。综合这些证据,新一轮的模拟支持了这样的观点:藏红花苷可能有助于恢复受SCA3影响神经元中更健康的存活—死亡平衡。
从计算预测到现实疗法
尽管藏红花苷的预测安全性显示出良好前景,且其在模拟中的表现令人鼓舞,但该工作仍停留在计算模型阶段。研究并未在SCA3患者身上直接测试藏红花苷,而是提供了一份详尽的路线图,指出藏红花苷是值得进一步进行实验室和动物研究、并最终进入精心设计的临床试验的强有力候选者。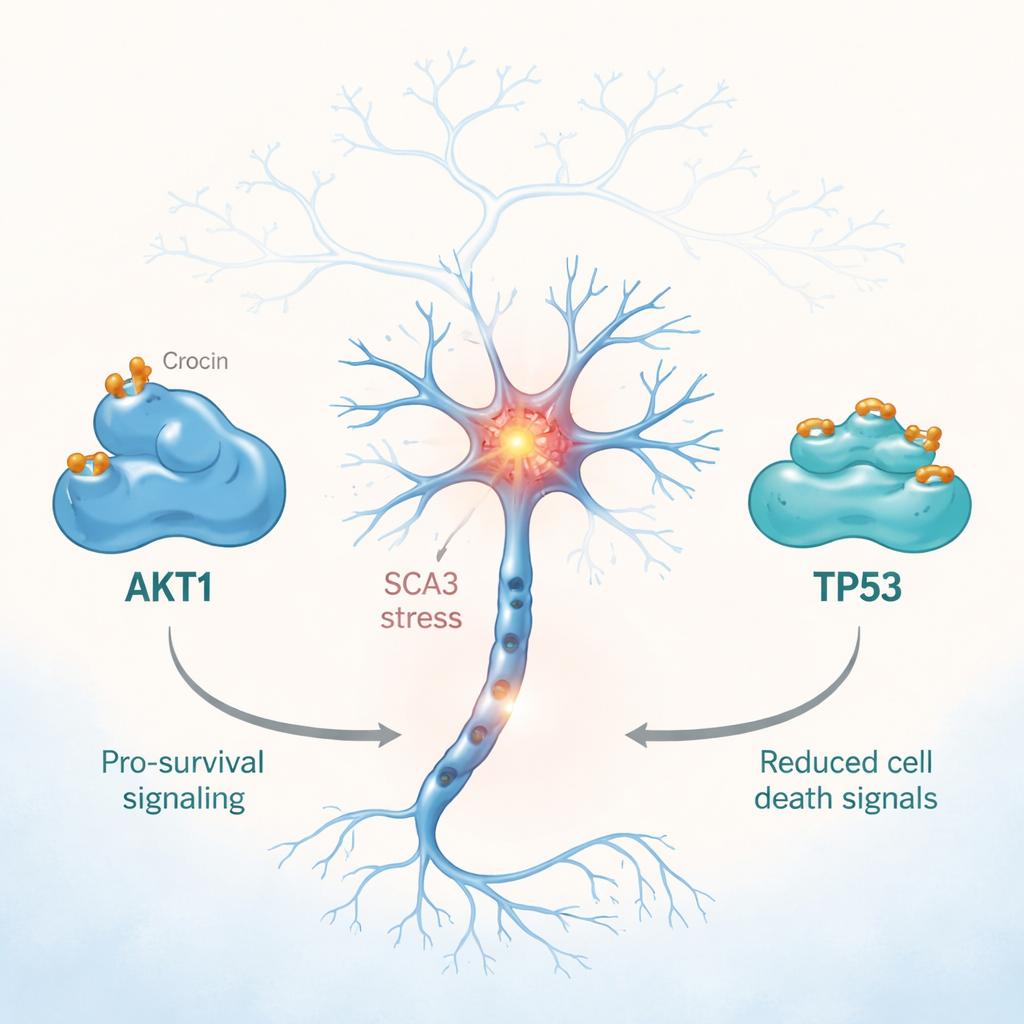
引用: Roney, M., Mohd Hisam, N.S., Uddin, M. et al. Repurposing of natural products for spinocerebellar ataxia type 3 using integrated network pharmacology and in silico approaches. Sci Rep 16, 7332 (2026). https://doi.org/10.1038/s41598-025-30652-8
关键词: 脊髓小脑性共济失调3型, 天然产物, 药物再利用, 藏红花苷, 神经退行性疾病