Clear Sky Science · zh
鉴定与评估与肿瘤焦亡相关的抗原以设计肺癌疫苗候选物
这项研究对肺癌患者的意义
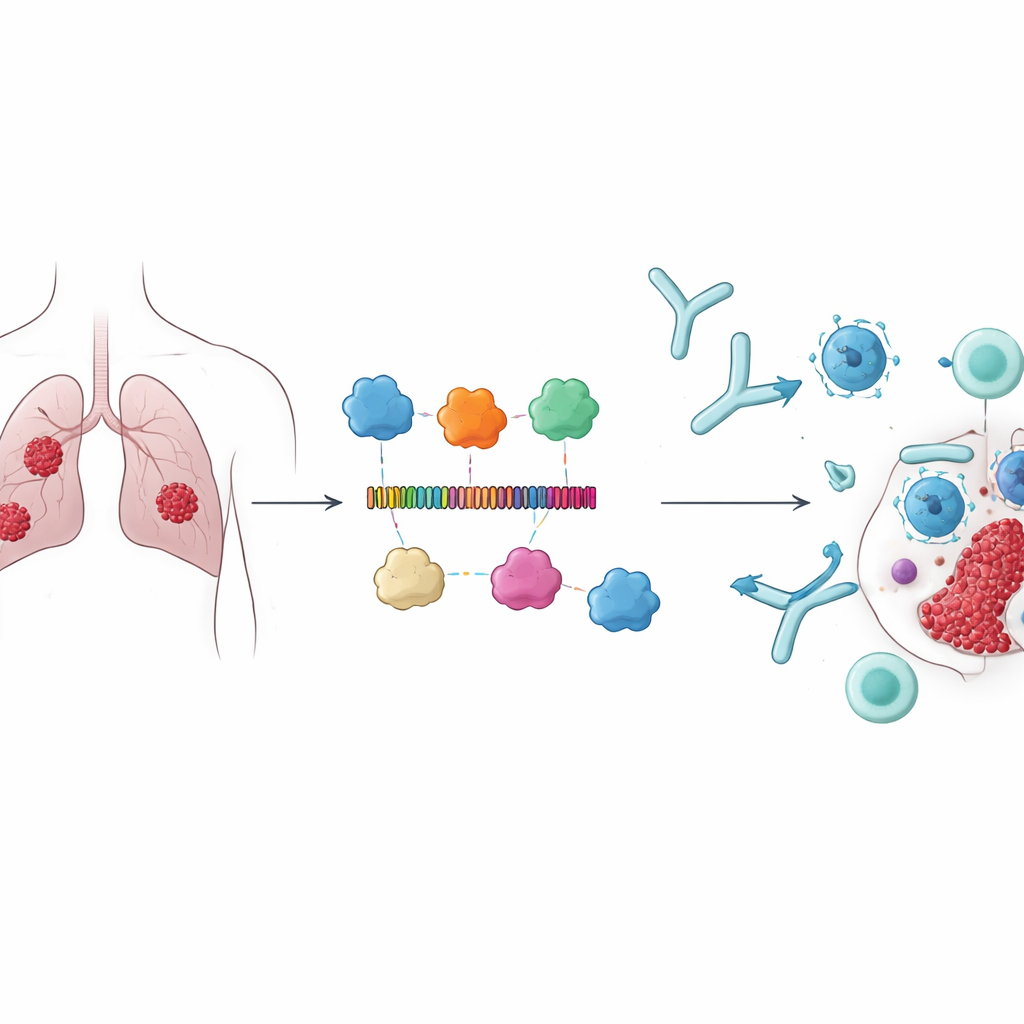
肺癌仍然是全球最致命的癌症,现有治疗——手术、化疗、放疗和免疫疗法——仍使许多患者缺乏长期治愈的选择。本研究探索了一个截然不同的思路:一种治疗性疫苗,目的不是预防感染,而是训练免疫系统更好地识别并攻击肺肿瘤。作者利用先进的计算建模,完全在体外计算环境中构建并测试了一种基于蛋白的疫苗,该疫苗靶向与一种称为焦亡的剧烈肿瘤细胞死亡形式相关的分子,为更精确且持久的肺癌治疗开辟了新途径。
把细胞死亡开关变成癌症靶点
研究者没有聚焦于经典的癌症标志物,而是选择了四种参与焦亡的蛋白:CARD8、NAIP、NLRP1 和 NLRP3。焦亡是一种会以爆发性方式发生并能提醒免疫系统的程序性细胞死亡。这些蛋白在免疫调节中起作用,并与肺腺癌更好的生存率相关,使其成为有吸引力的靶点。团队推断,如果能精确训练免疫系统识别肿瘤细胞上这些蛋白的小片段,可能不仅直接帮助清除癌细胞,还能放大针对肿瘤的更广泛免疫反应。
逐步构建定制疫苗
作者使用免疫信息学工具扫描这四种蛋白,以识别可被T细胞和B细胞识别的短片段或表位。他们从数百个候选中挑选出15个在免疫可识别性上评分较高、并被预测为无毒且不致敏的表位。这些片段随后通过精心选择的分子“间隔”连接为一个长蛋白,以确保每个表位保持可及性。为增强免疫反应,他们增加了三个来自细菌蛋白的已知免疫刺激成分作为佐剂。所得构建体由678个氨基酸残基组成,预测具有稳定、可溶和强抗原性的特性——这些特性对实际疫苗非常重要。
在计算机上测试构型与稳定性
由于疫苗效力高度依赖其三维形状,团队使用多种先进的结构预测程序构建了新蛋白的三维模型。他们反复优化这些模型,并用标准结构学基准检查其质量,最终选定满足真实蛋白几何与稳定性严格标准的版本。他们还绘制出哪些表面区域最容易被抗体识别,并设计了新的内部“桥接”——二硫键,预测可进一步加固和稳定蛋白。为模拟疫苗在体内水性环境中的行为,研究者进行了持续100纳秒(注:文中为100亿分之一秒,即100纳秒)并重复10次的详尽分子动力学模拟。在这些模拟过程中,模型蛋白保持紧凑且结构稳定,表明其在真实条件下能维持预期构型。
模拟免疫系统的反应
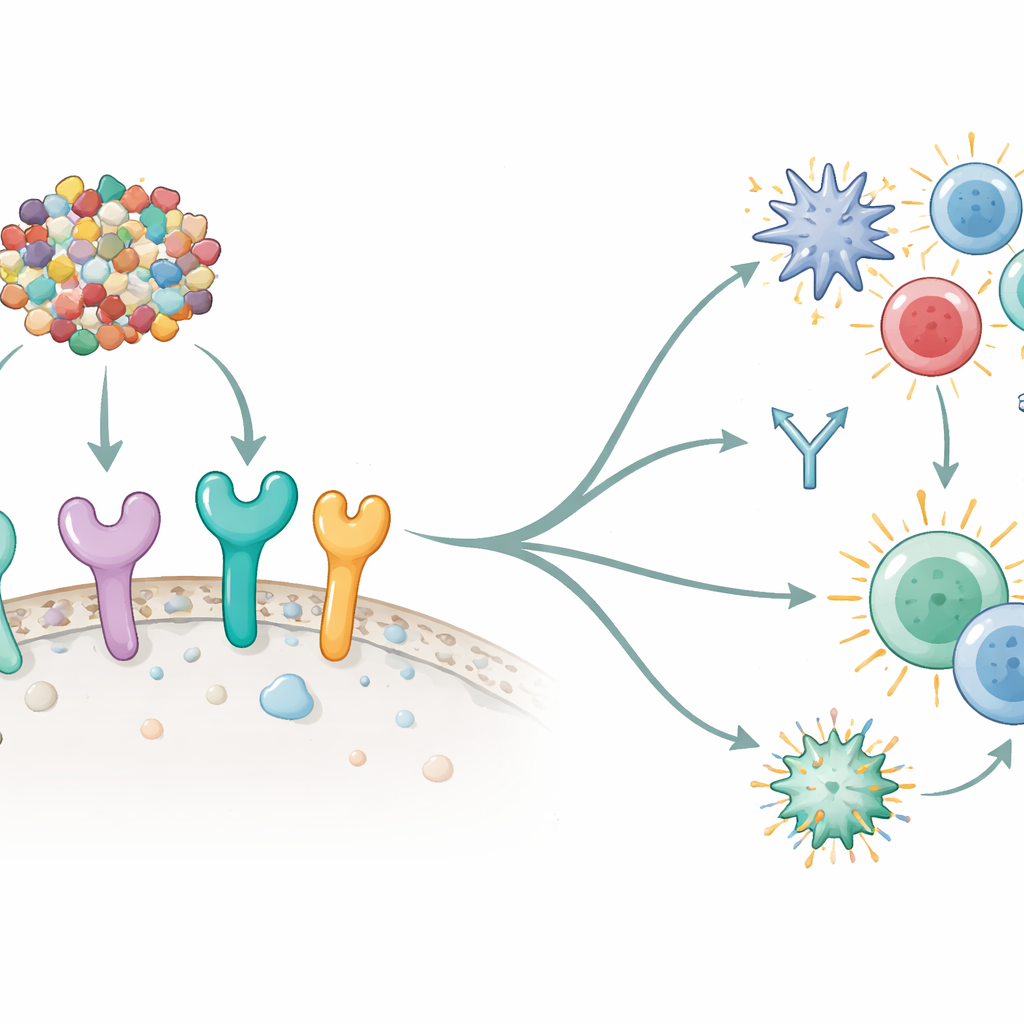
接下来,研究者询问他们的疫苗是否能原则上与免疫系统的关键“报警”传感器——位于免疫细胞表面或细胞内的Toll样受体(TLRs)——进行有效互动。计算对接实验显示疫苗与六种不同人类TLR之间存在强且稳定的相互作用,尤其是已知能启动强大免疫级联反应的TLR5和TLR8。随后他们使用免疫系统建模软件模拟了完整的免疫接种方案。在这些虚拟实验中,三剂疫苗导致模拟抗原迅速清除,出现强烈的抗体波(尤其是IgM和IgG1),并促使长期记忆B细胞和辅助T细胞增加。干扰素-γ和多种白细胞介素等重要信号分子也显著升高,表明先天免疫和适应性免疫两方面都被激活——这正是抗肿瘤保护所需的平衡反应。
为实际生产做准备
为了从概念走向实验室测试,团队评估了该疫苗是否能在常用的细菌表达系统大肠杆菌中高效生产。他们通过优化基因编码(不改变蛋白质本身)来实现适合细菌表达的密码子使用和均衡的DNA化学组成。随后进行了虚拟克隆步骤,将优化后的基因插入用于蛋白表达的标准实验质粒。这些步骤表明,如果进入实验室阶段,该疫苗很可能可按规模制造以供进一步研究。
这对未来癌症护理可能意味着什么
简而言之,这项工作提供了一个经过充分计算验证的肺癌疫苗蓝图,该疫苗靶向与一种高度炎性肿瘤细胞死亡形式相关的蛋白。设计在模拟中显示出安全、稳定并能强烈激活免疫防御,且预测可覆盖广泛的人群。然而它仍是一个数字原型,必须在细胞、动物乃至人体中得到验证。这项研究展示了现代计算工具如何将多年反复试验浓缩为一个集成设计。如果后续实验验证了这些预测,这类疫苗未来有望成为现有治疗的补充,帮助患者自身免疫系统更可靠地识别并攻击肺肿瘤。
引用: Nguyen, T.L., Kim, H. Identification and evaluation of tumor pyroptosis-associated antigens for design a vaccine candidate against lung cancer. Sci Rep 16, 9559 (2026). https://doi.org/10.1038/s41598-024-84792-4
关键词: 肺癌疫苗, 焦亡, 多表位免疫疗法, 计算疫苗设计, 肿瘤免疫反应