Clear Sky Science · zh
覆盖所有组织病理学类别的具链式思维推理的乳腺超声数据集
这项研究为何重要
乳腺癌筛查日益依赖超声检查,尤其针对年轻女性以及乳腺X线摄影可及性较低的地区。然而,即便是用于读取这些影像的最优秀人工智能(AI)工具常常表现得像黑箱,只给出良性或恶性的结论,却不显示其得出结论的过程。本文介绍了BUS-CoT——一个新的、公开可用的乳腺超声数据集,目的不仅是帮助AI识别癌症,更是教会它以类似专科放射科医师处理疑难病例的方式“边想边说”。
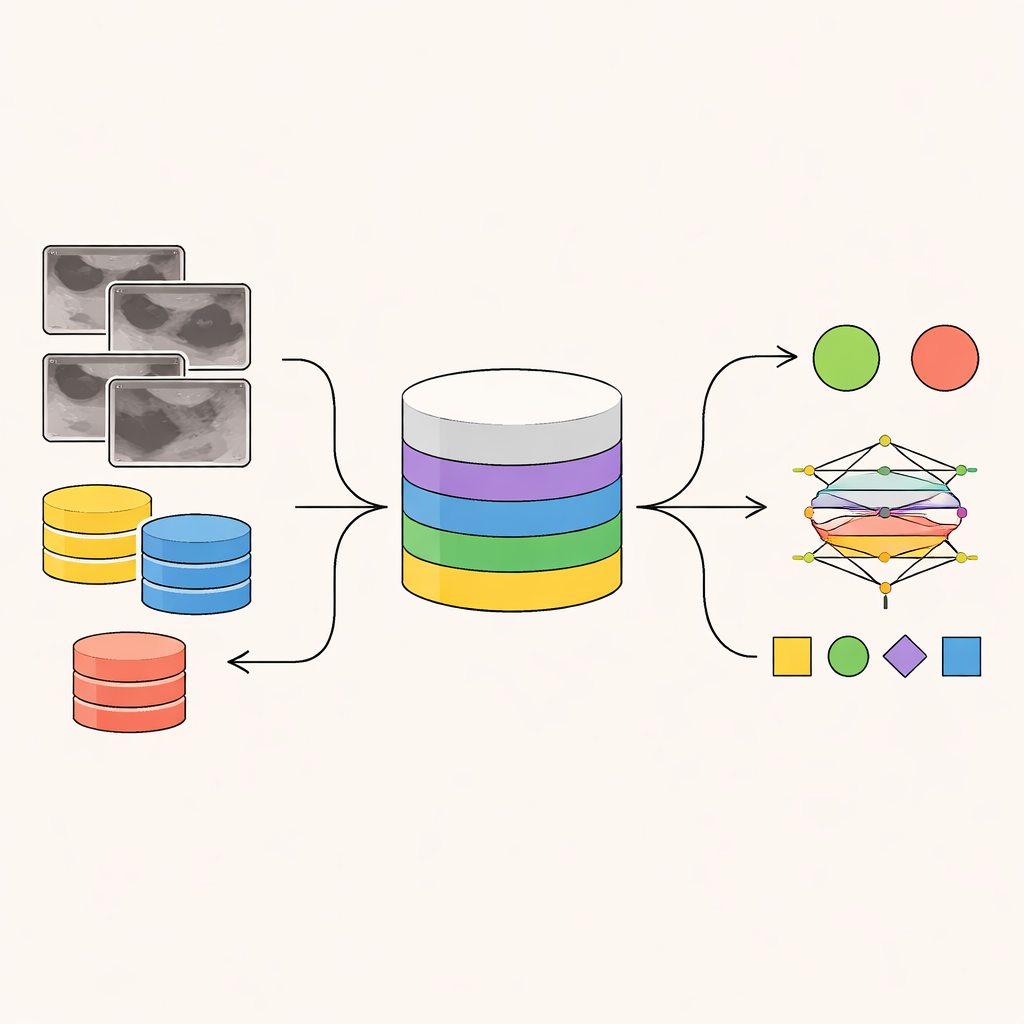
从模糊影像到结构化线索
超声图像噪声多且难以解读,即便对专家来说也不容易。人类专家不会仅凭一瞥就下诊断;他们会寻找一连串可视线索——肿块是卵圆还是不规则、边界是光滑还是有棘突、是否有声影、以及微小亮点是否提示钙化。这些线索随后与标准化规则(例如BI-RADS体系)一起权衡,以评估病变为癌的概率并决定是否需要活检。现有的AI系统通常跳过这种逐步推理,直接从像素到预测,这使得其决策难以信赖,也难以应对不寻常或罕见病例。
一套丰富的真实世界病例集
BUS-CoT通过汇集来自多大洲、不同超声机器类型的刊物、开放数据集和在线病例库的11,439张乳腺超声图像(对应11,850个病变、4,838名患者),来应对这些问题。关键在于,该集合覆盖世界卫生组织定义的全部99种乳腺组织类别,从常见的良性结节如纤维腺瘤到罕见且侵袭性的癌症。这种广泛覆盖解决了早期数据集的一个主要弱点:常常遗漏罕见疾病,从而让AI系统在医生最可能感到棘手的那类病例上准备不足。
教机器沿着推理路径前进
除了原始影像,BUS-CoT还提供了多层次的专家注释。放射科医师首先记录基本观察:是否存在肿块、是否有钙化以及病变位置。随后他们标注详细的视觉特征——形状、边缘、内部回声模式等——在此基础上分配BI-RADS类别,并将这些影像发现与组织样本的确诊病理结果关联。最后,他们把这些结构化信息转换成叙事式的链式思维:简短的逐步解释,将影像所见与特定诊断可能性的原因连接起来。与自动生成的文本不同,这些推理链由有经验的乳腺影像专家撰写并核验,保留了可供模型学习的真实临床逻辑。
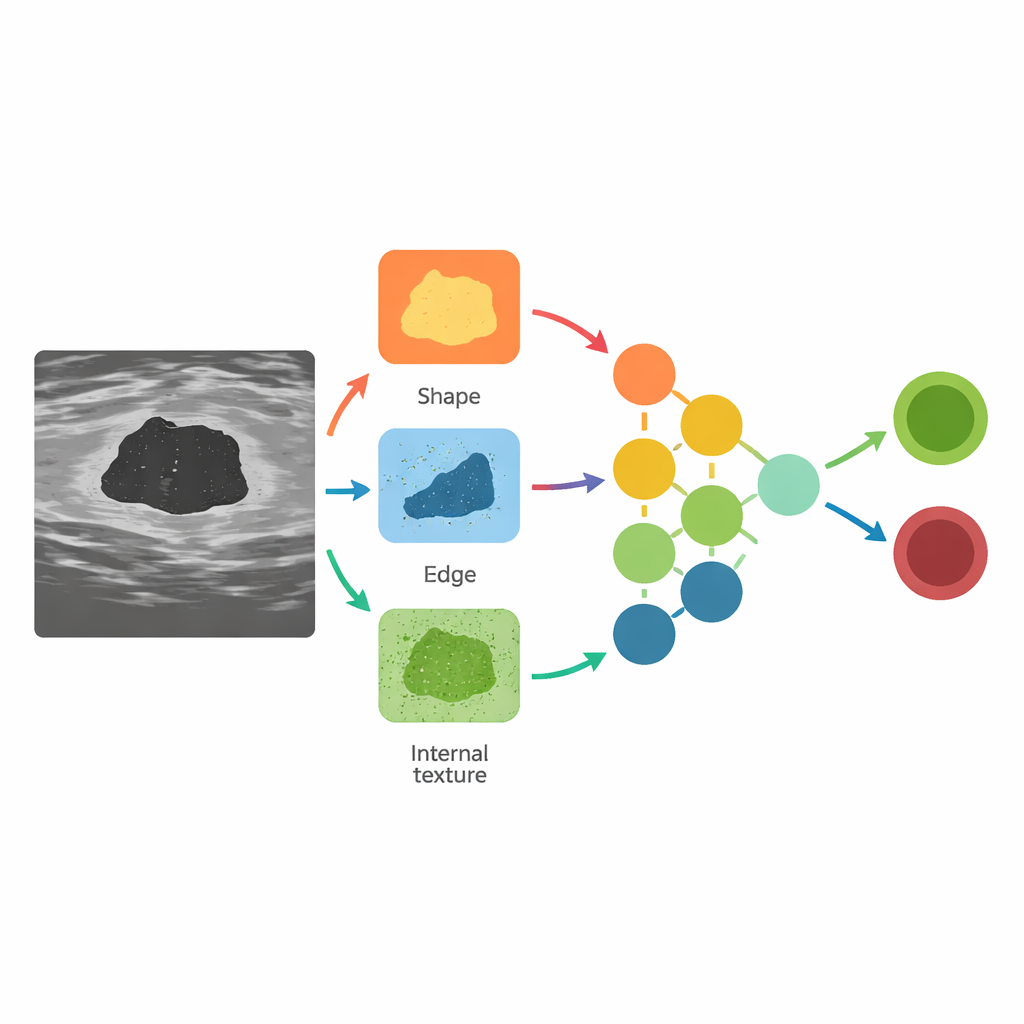
对数据集进行检验
为展示该资源的能力,作者在BUS-CoT上训练了多种现代图像与视觉—语言模型,重点使用了经过精心筛选的5,163张以病变为中心的高质量子集。传统的图像网络学会将病变分类为良性或恶性,而一种先进的视觉—语言模型则被训练为既观察图像又在给出答案前生成一条推理链。当模型被强制以这种结构化方式进行推理时,其准确性有所提高,尤其是在那些良性与恶性外观相似的模糊病例上。换言之,引导模型“逐步走过”放射科医师使用的相同视觉线索,有助于其做出更好、更安全的决策。
这项工作如何影响未来诊疗
对患者和临床医生而言,BUS-CoT的承诺在于开发出不仅能达到人类水平准确性、还能以临床上有意义的方式解释自身结论的AI工具。通过将数千张超声图像与经过详尽记录的推理配对,并覆盖从常见到罕见的全部乳腺组织诊断谱,这个数据集为能够处理棘手边缘病例并为其建议提供理由的AI系统奠定了基础。尽管目前它尚未包含如遗传学或病史等更广泛的临床信息,BUS-CoT仍是朝向更透明、可被信任的基于超声的诊断迈出的重要一步,使机器不再像神秘的预言者,而更像思路可检视并可改进的勤勉初级同事。
引用: Yu, H., Li, Y., Niu, Z. et al. A Chain-of-thought Reasoning Breast Ultrasound Dataset Covering All Histopathology Categories. Sci Data 13, 370 (2026). https://doi.org/10.1038/s41597-026-06702-9
关键词: 乳腺超声, 医学影像人工智能, 可解释人工智能, 乳腺癌诊断, 临床数据集