Clear Sky Science · zh
散发性髓样甲状腺癌的全面转录组概况
为什么这种罕见甲状腺癌很重要
髓样甲状腺癌是一种罕见的甲状腺癌类型,行为比大多数甲状腺肿瘤更具侵袭性,且常在已较晚期时才被发现。由于发病率低,医生和研究人员一直缺乏足够的数据来理解为何有些肿瘤生长和转移更快,或为何有些患者对治疗反应更好。本研究通过对72例肿瘤中数千个基因的广泛基因组范围活性进行深入分析,填补了这方面的空白,创造了迄今为止对该疾病最完整的分子快照之一。
洞察肿瘤细胞内部
研究者并未仅关注 DNA 突变,而是检查了肿瘤的“转录组”——癌细胞中由活跃基因产生的全部 RNA 信息。这些 RNA 信息像细胞活动的实时状态报告。通过对新鲜冷冻肿瘤样本进行 RNA 测序,团队能够看到哪些基因被上调、哪些被下调,以及基因信息如何被拼接在一起。这种方法有助于揭示经典遗传检测可能遗漏的隐蔽模式,例如基因调控或组合方式的变化。
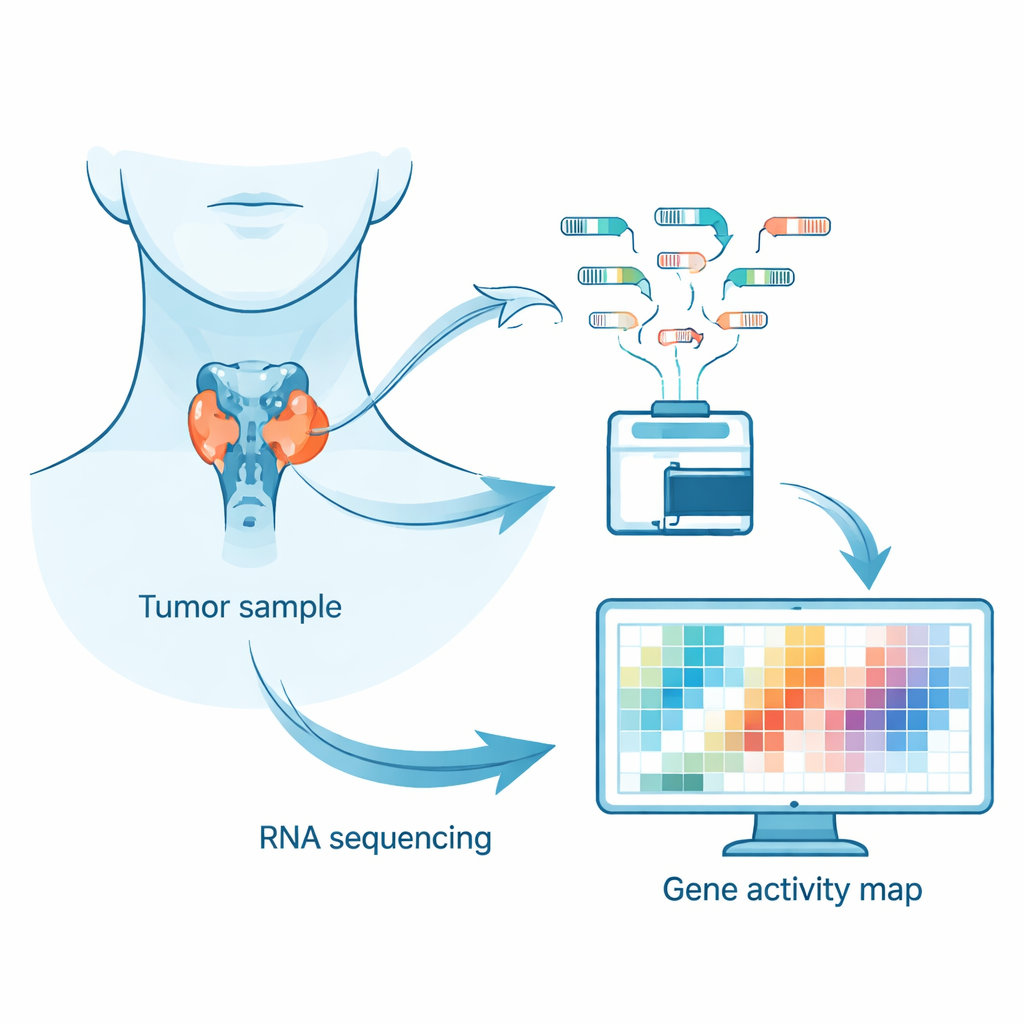
研究对象与测量内容
团队分析了来自72名散发性(非家族性)髓样甲状腺癌患者的肿瘤样本。受试者中女性略多一半,手术时的中位年龄为61岁。约58%的肿瘤携带称为 RET 的基因变异,约24%存在 RAS 家族基因的突变,这两类基因都是该癌种的已知驱动因子。研究者首先通过检测关键标志物(如在此类癌症中升高的降钙素,以及属于正常甲状腺细胞并保持低水平的甲状腺球蛋白)来确认肿瘤样本质量高且较少受正常甲状腺组织或免疫细胞的污染。随后他们使用成熟的计算工具将 RNA 读数比对到人类基因组、计数基因活性,并在临床与遗传组之间搜索差异。
基因活性与分期及突变的关联
当研究者比较早期(I–II 期)与更晚期(III–IV 期)肿瘤时,发现有760个基因的活性水平在两组间显著不同。这表明基因表达模式包含有关癌症进展程度的重要线索。他们还将携带 RET 或 RAS 突变的肿瘤与两者均无突变的肿瘤进行对比,发现超过1200个基因活性发生改变。另一项分析聚焦于携带特定 RET 变异 M918T 的肿瘤——该变异长期以来与更差的预后相关。在这些肿瘤中,与 RET 正常的癌症相比,有529个基因的活性不同,且 RET 基因本身表达更高,强调了这一单一变异如何显著重塑细胞行为。
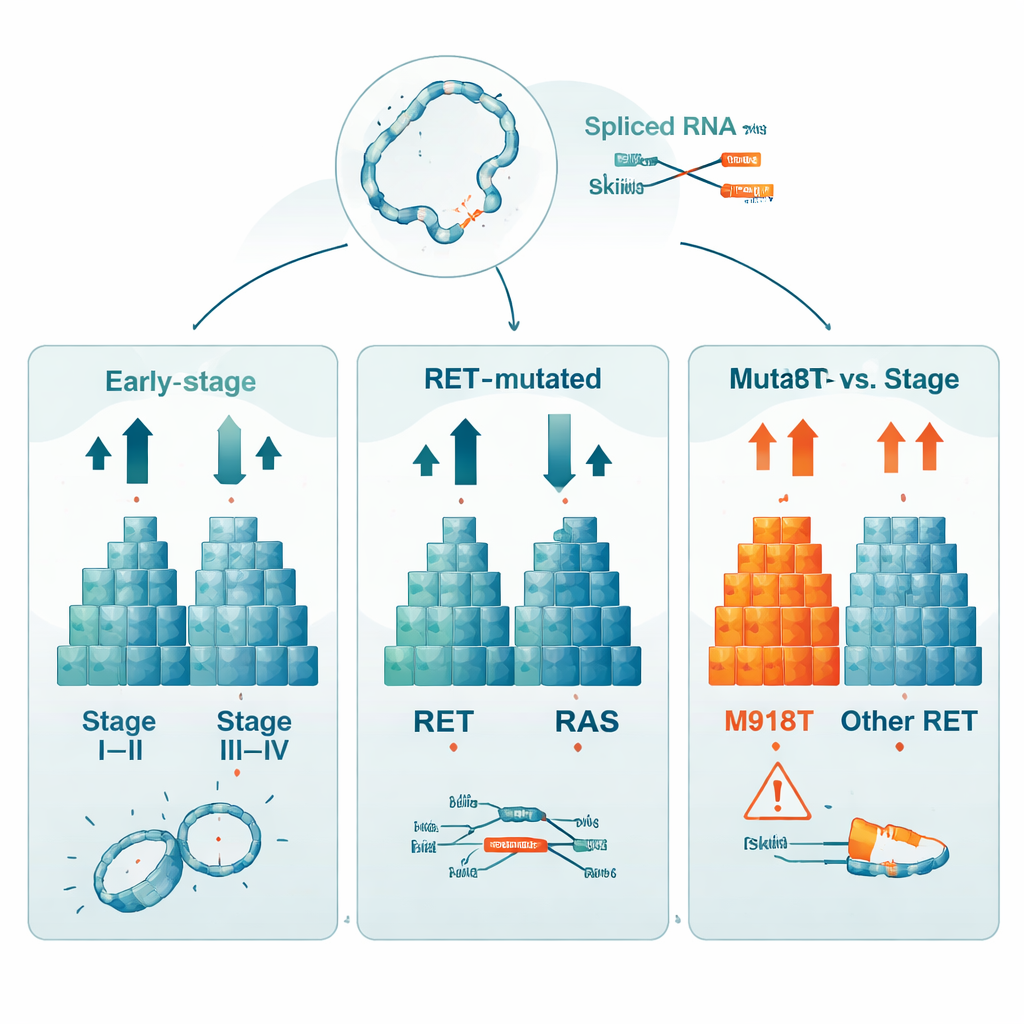
隐匿的重排与信息改写
除了基因的简单开关式变化外,该研究还寻找更深层次的 RNA 干扰形式。团队检测到59种不同的基因融合转录本,即不同基因片段在 RNA 水平上异常连接在一起。大多数融合事件很少见,且最频繁的一种可能是技术性伪像,但这份目录表明可以从这些数据系统性挖掘此类重排。研究者还绘制了数千个可变剪接事件,即基因信息的片段被跳过、替换或保留。尽管按分期、突变类型或 M918T 状态进行的各项临床比较显示这些可变剪接总体数量相似,但具体事件大多不同,这提示肿瘤细胞有多种、部分独立的方式来重接其基因信息。
该资源为患者与科学家提供了什么
对患者而言,这项工作尚未直接转化为新的药物或检测方法,但它奠定了必要的基础。作者将所有处理过的 RNA 测序数据公开,使其他科学家能够深入挖掘以发现新的预测预后生物标志物、改进髓样甲状腺癌的分类,或发现可被未来疗法(包括新一代选择性 RET 抑制剂)针对的脆弱点。简而言之,本研究提供了许多真实病例中肿瘤基因的详细“活性地图”,为研究人员理解为何这种罕见癌症在不同人之间表现差异大以及未来如何更精确地个体化治疗,提供了重要工具。
引用: Palumbo, D., Melone, V., Palo, L. et al. Comprehensive Transcriptome Profiling of Sporadic Medullary Thyroid Carcinomas. Sci Data 13, 234 (2026). https://doi.org/10.1038/s41597-026-06550-7
关键词: 髓样甲状腺癌, 癌症基因组学, RNA 测序, RET 突变, 个体化肿瘤学