Clear Sky Science · zh
维生素B2代谢促进FSP1稳定以防止铁死亡
一种常见维生素如何帮助细胞在生与死之间做出决定
我们的细胞不断在生存与自我毁灭之间走钢丝。一种引人注目的细胞死亡形式称为铁死亡,因为它能够选择性杀死对其他治疗耐受的癌细胞。该研究揭示了一种日常营养素——维生素B2(核黄素)——通过稳定一种关键的保护性蛋白,悄然改变了这种平衡。了解饮食、细胞代谢与癌细胞死亡之间这一隐秘联系,可能有助于研究人员设计更智能的疗法并完善未来的营养建议。
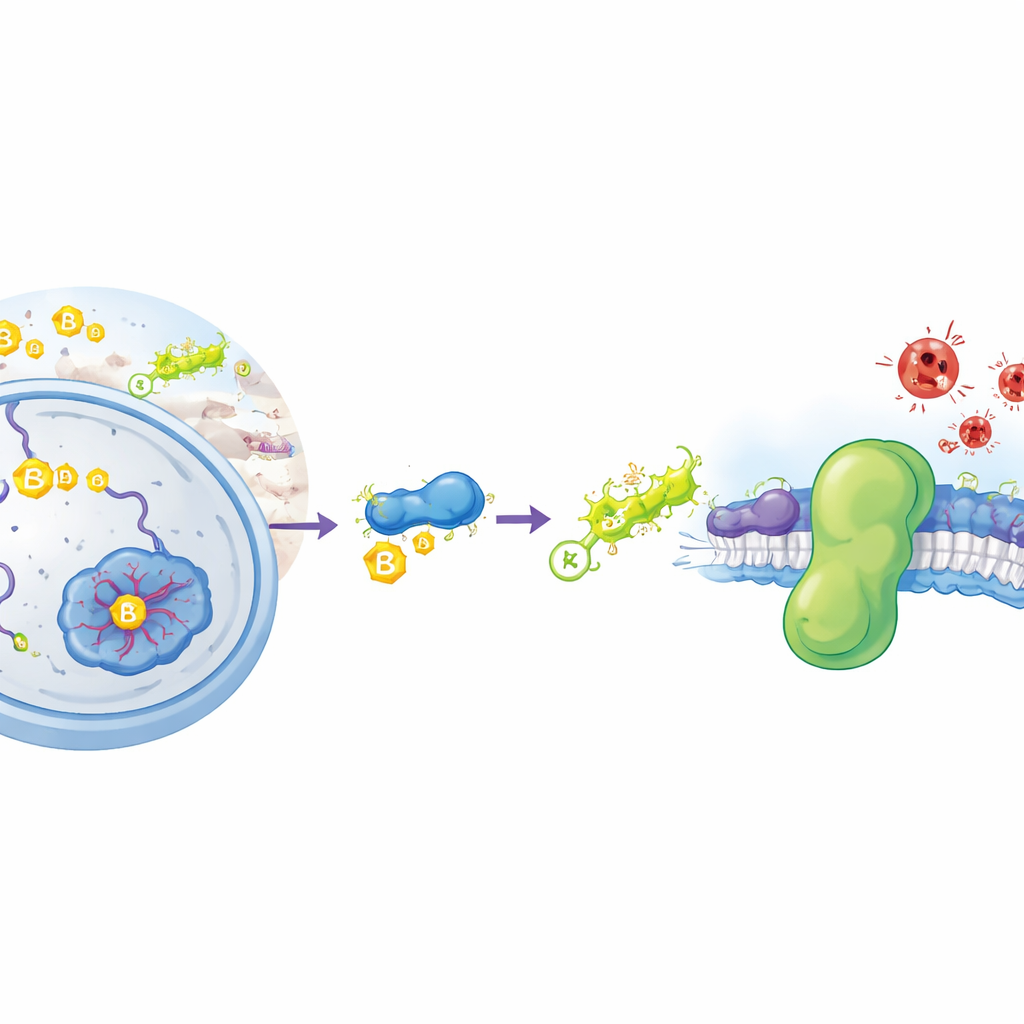
细胞内的一种特殊“生锈”
铁死亡是一种由化学过程驱动的细胞死亡,类似于金属生锈:细胞膜中脂质的失控氧化。当这些脂质被破坏时,膜失去完整性,细胞破裂。我们的细胞通常部署若干防御机制来阻止这种情况发生。主要屏障之一是酶GPX4,它利用小分子谷胱甘肽来解毒有害的脂质过氧化物。另一条平行防线是名为FSP1的蛋白,它位于细胞膜上,利用小型类脂分子截留破坏性的自由基,阻止其扩散。癌细胞常常上调FSP1以逃避铁死亡,使该蛋白成为抗癌新药的主要靶点。然而直到现在,科学家们尚不清楚细胞如何控制FSP1的生成量及其生存时间。
为这一阻死因子构建细胞内的“燃料表”
为发现FSP1的隐性调控者,研究者首先将人类骨癌细胞改造为携带荧光报告系统。他们在天然FSP1蛋白上标记了绿色荧光信号,并配套了一个蓝色信号用以报告细胞产生的FSP1信息RNA的多少。这一巧妙设计使他们能区分基因活性(蓝)变化与蛋白稳定性(绿)变化。在该双色系统就位后,他们用CRISPR–Cas9系统系统性扰动几乎每个基因,然后对FSP1水平高或低的细胞进行分选。通过比较每组中富集的导向RNA,他们绘制出数百个在基因调控或蛋白周转水平上促进或降低FSP1的基因图谱。
维生素B2的隐秘任务:制造一个稳定的把手
最显著的命中项中包括两种酶:核黄素激酶(RFK)和FAD合成酶(FLAD1),它们将维生素B2转化为一种名为FAD的辅因子。FSP1是一个黄素蛋白,通常紧密结合FAD以执行其化学反应。当RFK或FLAD1被去除,或当细胞在缺乏维生素B2的培养基中生长时,尽管FSP1的基因活性保持相近,其蛋白水平仍显著下降。研究团队证明,当GPX4被阻断时,这种损失使细胞对铁死亡更为敏感。重要的是,维生素B2本身并非典型抗氧化剂:在敏感的体外测定中,它未能像维生素E那样阻止脂质氧化。相反,将FAD(及部分其前体FMN)补回缺乏的细胞可恢复FSP1水平和对铁死亡的抗性,而如果处理酶缺失,仅补充额外的维生素B2无济于事。
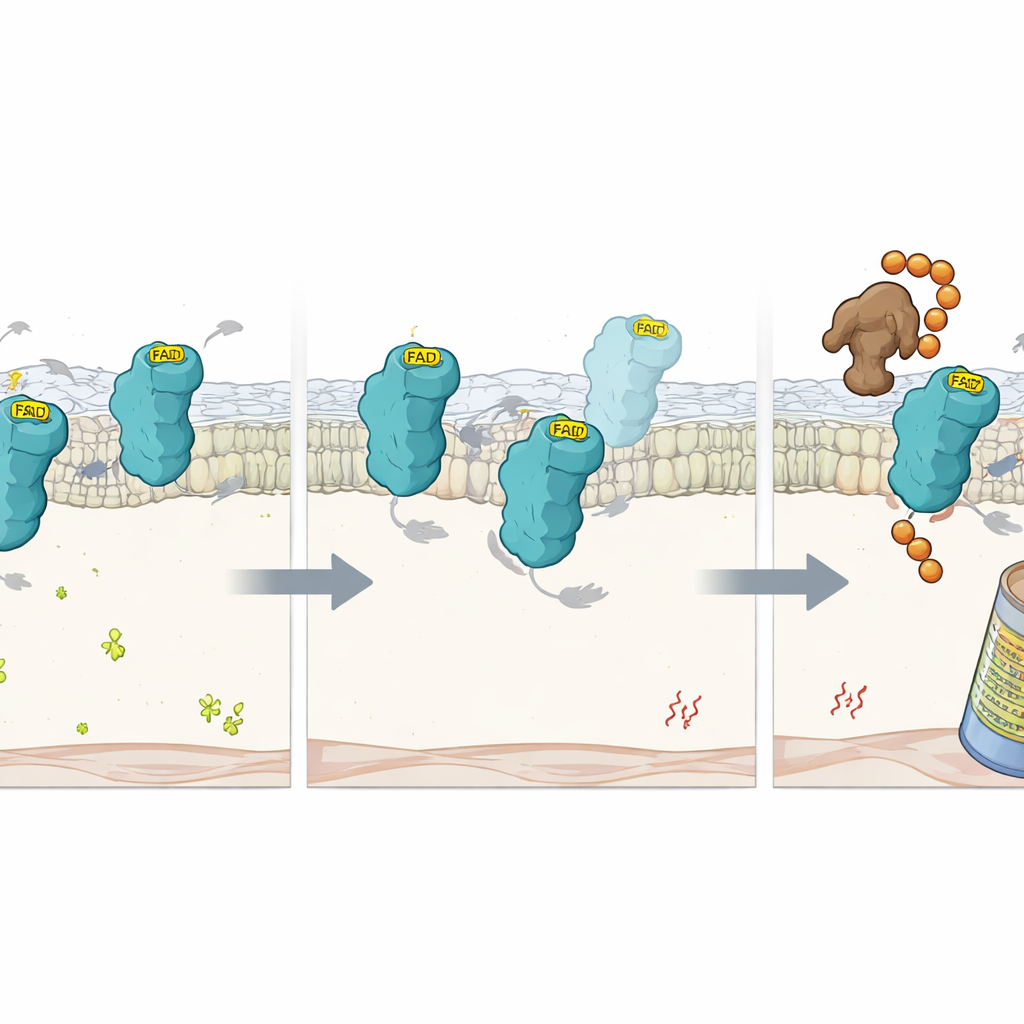
当辅因子缺失时会发生什么
为进一步深入,科学家研究了在FSP1中破坏其结合FAD能力的精确突变体。这些突变蛋白仍大体折叠成正常形状,但丧失了FAD及其催化活性。在细胞内,这些变体比正常FSP1衰减得更快,除非蛋白酶体——细胞的蛋白粉碎机器——被阻断。这提示FAD结合本身像一个稳定的把手,保护FSP1不被标记为缺陷蛋白。采用另一项在低FAD条件下的聚焦CRISPR筛选,团队鉴定出一种名为RNF8的E3连接酶为识别无FAD FSP1的关键因子。当RFK被删除时,RNF8在空缺辅因子的FSP1上连接泛素链,将其目标化交由蛋白酶体降解。去除RNF8可在FAD贫乏的细胞中减慢FSP1的周转,尽管在没有辅因子的情况下它无法恢复FSP1丧失的保护功能。
从分子回路到癌症治疗构想
将这些片段组合起来,作者提出了一个简单但有力的模型:维生素B2经RFK和FLAD1转化为FAD后,结合FSP1,对其生化活性和寿命均至关重要。当维生素B2供应或其加工出现问题时,新合成的FSP1无法获得FAD,会被RNF8标记并迅速被蛋白酶体拆解,使细胞更容易遭受铁死亡损伤。癌症数据表明,RFK表达较高的肿瘤对诱导铁死亡的药物更具抗性,突显了该通路的现实相关性。对非专业读者而言,核心信息是:一种熟悉的维生素远不止作为简单抗氧化剂存在——它决定了一种强效抗死亡蛋白是坚守防线还是被清除。通过调节维生素B2代谢或FSP1的稳定性,未来的治疗或能更好地利用铁死亡来消除癌细胞,同时尽量保护健康组织。
引用: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
关键词: 铁死亡, 维生素B2, FSP1, 癌细胞死亡, 细胞代谢