Clear Sky Science · zh
抗噬菌体 retron Eco2 的结构与机制
细菌如何利用内置“自毁”机制抵抗病毒
感染细菌的病毒,称为噬菌体,随处可见——从海洋到我们自身的肠道。该研究揭示了存在于部分细菌体内的微小遗传装置 Eco2 retron 如何帮助它们在噬菌体攻击中存活。通过解析 Eco2 的三维结构及其激活方式,工作阐明了一种新的紧急防御机制:在检测到感染时,细胞有意关闭自身的蛋白质合成,从而阻止病毒扩散。
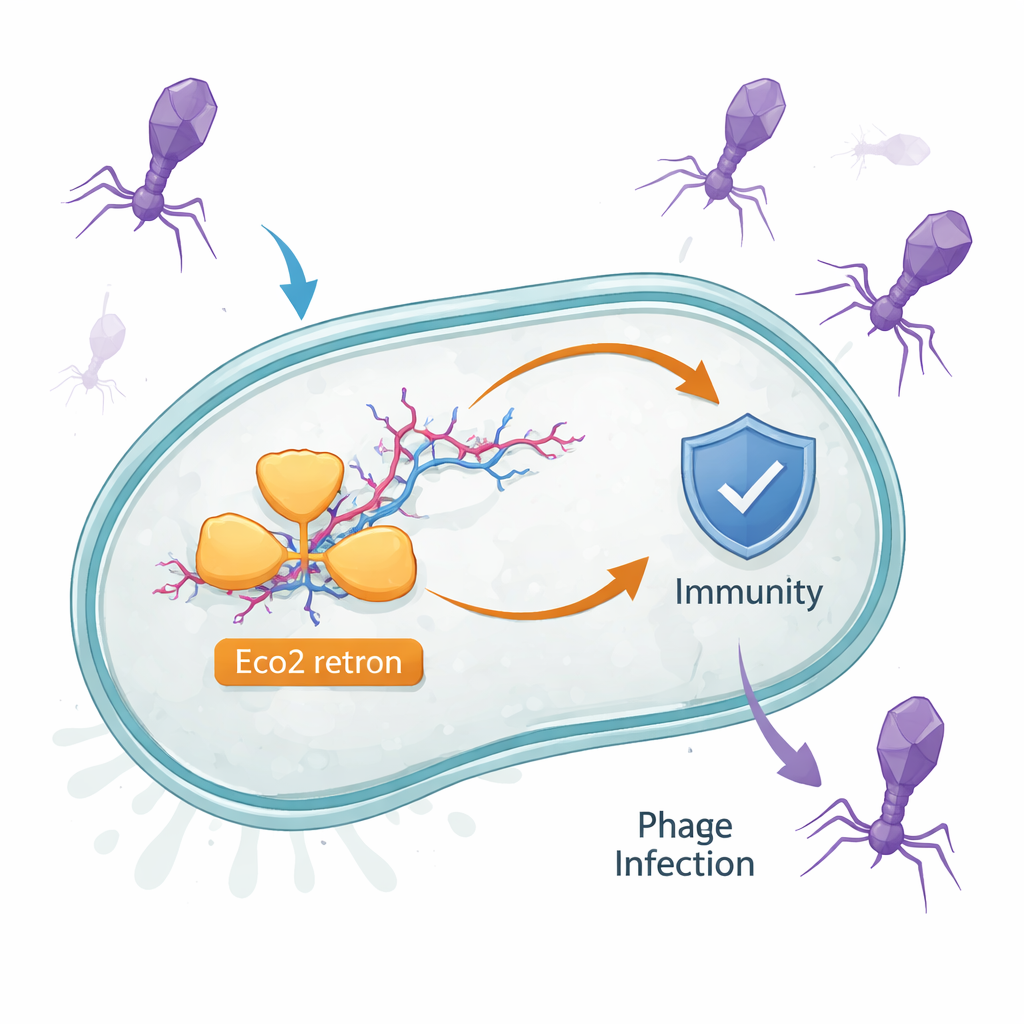
细菌细胞中的隐秘 DNA–RNA 装置
细菌携带许多只在感染期间启动的小型防御系统。Eco2 就是其中之一。它存在于埃希氏菌(Escherichia coli)中,由一个既能将 RNA 逆转录成 DNA 又能切割核酸的单一蛋白质构成。该蛋白与一种奇特分子 msDNA 协同工作,msDNA 是 RNA 与单链 DNA 的杂交体,呈分支状如小叉枝。此前的线索表明像 Eco2 的 retron 具有抗噬菌体作用,但单一蛋白与其 msDNA 伙伴如何感知感染并作出反应尚不清楚。
对多种病毒的广泛防护
研究人员首先询问 Eco2 对多种噬菌体的保护效果。通过用大量多样的病毒挑战携带 Eco2 的细胞,他们发现 Eco2 能阻挡许多噬菌体科,但并非全部。当一些噬菌体设法突围时,其基因组显示出编码病毒 DNA 切割酶(尤其名为 DenB 的一种)基因的突变。这一模式表明 Eco2 由特定的病毒核酸酶触发:当这些酶因突变失活时,病毒就能绕过该防御。
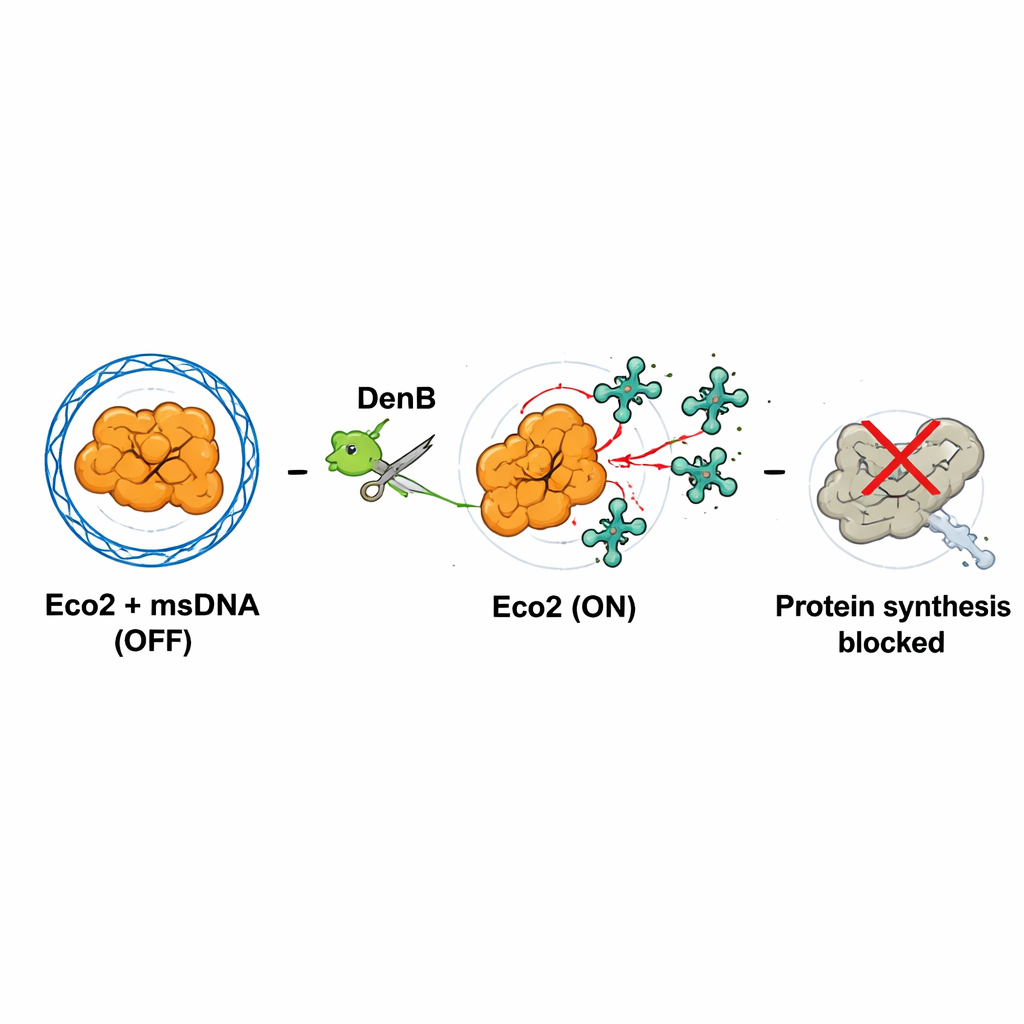
三臂分子护盾
为了观察 Eco2 的构造,团队使用低温电子显微镜将该复合体以近原子分辨率可视化。Eco2 并非单打独斗:三个 Eco2 蛋白组装成一个三臂状、如手里剑般的结构。分支的 msDNA 穿过并缠绕在这三种蛋白之间,将它们系在一起。这样,msDNA 在中心形成一个三向连接,并物理上“笼罩”住 Eco2 的核酸酶部分,阻断其切割位点。氢-氘交换实验(用于跟踪不同区域的柔性)显示,msDNA 的结合使该复合体变得更僵硬、更稳定。在这种静止状态下,Eco2 实际上被锁定在关闭(OFF)位置。
病毒攻击触发系统开启
激活的关键在于 msDNA 的破坏。通常帮助噬菌体处理 DNA 的病毒酶 DenB,也会切割笼罩 Eco2 的 msDNA。作者使用纯化的 DenB 与标准的 DNA 切割酶模拟了这一过程,观察到一旦 msDNA 被切开,Eco2 的核酸酶位点就会暴露并重排为活性构型。该“开启状态”的高分辨率结构显示,核酸酶口袋中的一个关键氨基酸移动到可恰当结合镁离子的位置,而镁离子对剪切 RNA 至关重要。因此,病毒的核酸酶活性——本意是重塑宿主 DNA——无意间扳动了 Eco2 的安全销,使其被激活。
切割细胞自身的 tRNA 以阻止病毒
被激活的 Eco2 切割什么?通过细胞外体系、放射性标记和真实感染期间的 RNA 测序,研究团队发现 Eco2 主要在转运 RNA(tRNA)上切割——tRNA 是将氨基酸送入核糖体的适配分子。Eco2 在 tRNA 的尾端附近进行切口,尤其偏好含有较多胞嘧啶的位点。当大量 tRNA 被破坏时,细胞的核糖体无法有效合成蛋白质。在 DenB 与活性 Eco2 共存的情况下,绿色荧光蛋白的产生急剧下降,细菌和噬菌体的 RNA 都被剪切。这种关闭很可能代表一种“中止感染”策略:被感染的细菌细胞牺牲自身生长,以阻止病毒成功复制和传播。
这一发现为何超越细菌本身的重要性
这项工作展示了一个最小化 retron 如何感知病毒酶、从不活跃形式翻转为活性状态,并通过靶向 tRNA 削弱蛋白质合成。对非专业读者而言,核心观点是:细菌有时并非通过精确打击来击败病毒,而是在恰当时机切断自身细胞机器的电源。除加深我们对微生物免疫的理解外,Eco2 及其 msDNA 支架的详细结构为工程师们希望将 retron 重新用于基因组编辑和合成生物学的应用提供了蓝图。
引用: Jasnauskaitė, M., Juozapaitis, J., Liegutė, T. et al. Structure and mechanism of antiphage retron Eco2. Nat Struct Mol Biol 33, 330–340 (2026). https://doi.org/10.1038/s41594-026-01754-2
关键词: 噬菌体免疫, retron Eco2, 细菌抗病毒防御, tRNA 裂解, msDNA