Clear Sky Science · zh
蓝藻环节转录的机制与重构
即便是细菌也需要体内时钟的原因
从人类到微小的微生物,所有生物都会计时。这些内在时钟帮助生物预见日出与日落,安排采食、修复和生长等活动。本文探讨了一种简单的光合细菌——延长拟南芥蓝藻(Synechococcus elongatus)——如何依靠蛋白质驱动的时钟,以惊人的精确度在24小时周期内开启与关闭基因表达。通过在试管中重建这一时间系统,研究者揭示了一个精简的生物钟版本,可能为生物技术与合成生物学带来新的工具与启示。
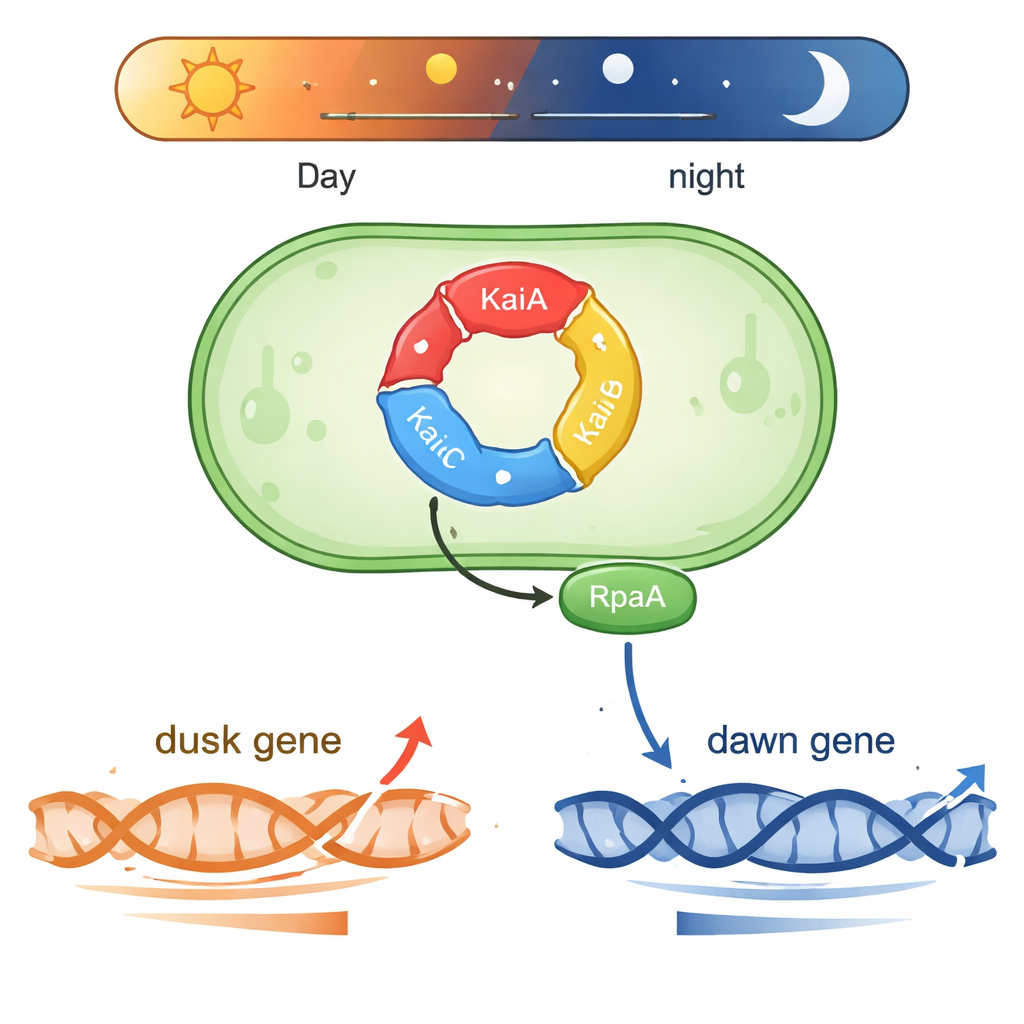
靠化学运行的小型时钟
Synechococcus生存在有光的水体中,需要预判每天的光照变化。其核心是由KaiA、KaiB和KaiC三部分组成的蛋白质机器。这些蛋白通过在大约24小时重复一次的循环中相互传递磷酸基,形成一个生化“齿轮传动”,即使置于细胞外也能保持计时。另有两种蛋白SasA和CikA能读取KaiC的磷酸化状态,并以此控制另一种蛋白RpaA。当RpaA被磷酸化时,它会结合DNA,充当数百个基因的主控开关,这些基因在恒光条件下会分别在主观“黎明”或“黄昏”时段出现峰值。
同一蛋白调控两类相反时间的基因
昼夜节律生物学中的一个难题是:同一个输出因子RpaA如何协调在不同时间达到峰值的基因。作者将注意力集中在两个代表性的DNA调控区(启动子)上:kaiBC,其活性在黄昏最强;以及purF,在黎明达到峰值。在用纯化的蓝藻RNA聚合酶和RpaA进行的受控反应中,他们展示了被磷酸化的RpaA一方面增强kaiBC启动子的转录,同时又抑制purF启动子的转录。精细的足迹图谱实验精确绘制出RpaA在每段DNA上的结合位点,揭示出其相对于标准启动子元件的位置决定了它是作为加速器还是刹车发挥作用。
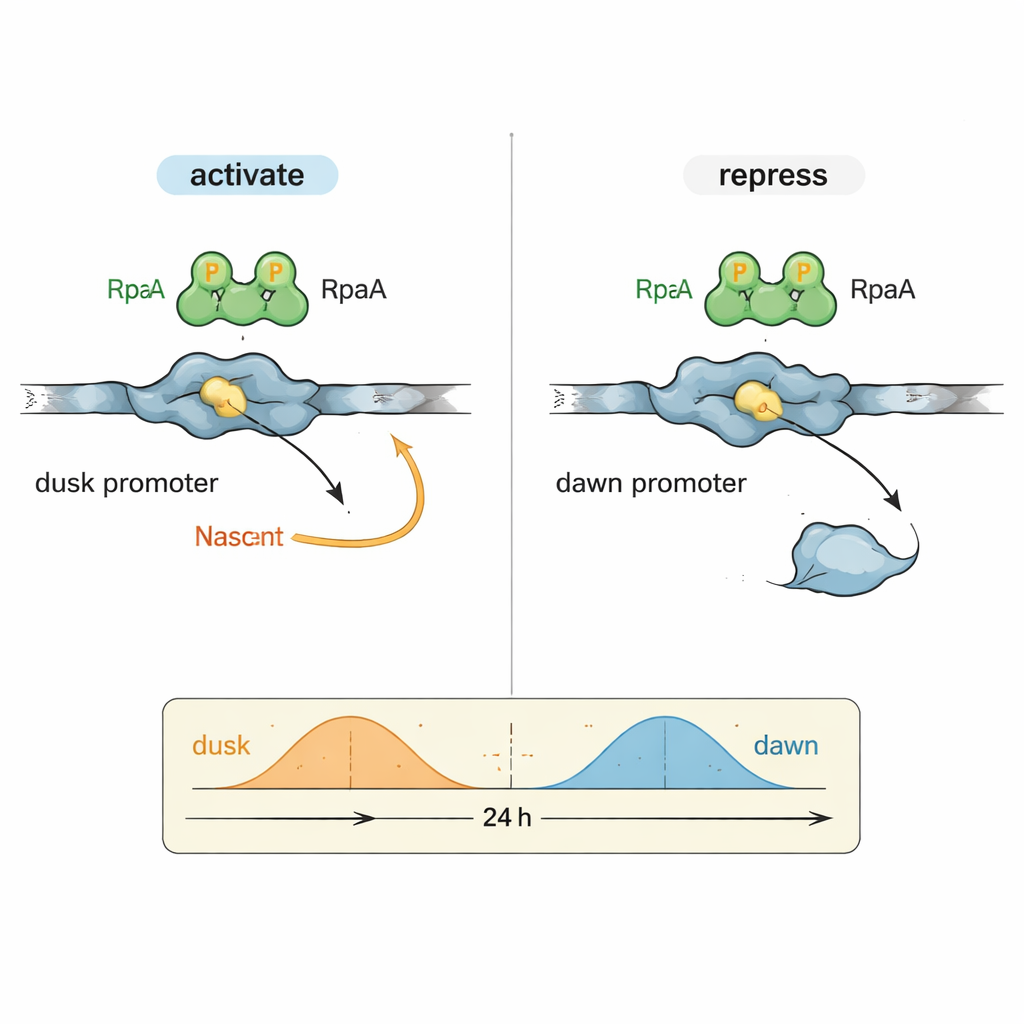
以原子级细节观测时钟的开关
为了解释这种双重行为的分子基础,团队利用高分辨率低温电子显微镜捕捉了RpaA与kaiBC启动子以及RNA聚合酶复合体的结构。图像显示RpaA以不对称二聚体的形式抓握DNA,并接触酶的两个关键部位:α亚基的尾部和通常识别启动子序列的σ因子的一段区域。这些接触使DNA弯曲,并帮助将RNA聚合酶定位到稍微重新定义的转录起始位点。精心设计的突变削弱任一接触点都会在体外及活细胞中降低或消除kaiBC的激活,证实了物理招募RNA聚合酶是黄昏相基因激活的基础。
从零开始构建一个由时钟驱动的基因
由于本源蓝藻RNA聚合酶复杂且难以在数日内保持活性,研究者转而使用实验室中广泛使用的更简单的T7噬菌体聚合酶。RpaA无法招募这种无关的酶,但仍可通过占据DNA来阻断它。团队设计了一个合成DNA模板,其中T7启动子驱动一个荧光RNA“Broccoli”报告基因,并在下游放置了一个RpaA结合位点。当他们在单一优化缓冲液中将该模板与KaiA–KaiB–KaiC时钟、CikA激酶/磷酸酶、RpaA和T7聚合酶组合时,观察到转录速率以大约24小时为周期起伏。通过改变ATP与ADP的比例可重置该节律,且在一定温度范围内周期几乎不变——这些都是典型的真实昼夜节律时钟特征。
从简单时钟到工程化计时
该研究表明,仅凭六种蛋白就足以将化学节律器与节律性基因读出连接起来:三种Kai时钟蛋白、CikA、RpaA和一种RNA聚合酶。通过改变RpaA在DNA上的位置,同一分子可以使某些基因在黄昏达到峰值,而另一些在黎明达峰,从而帮助解释在蓝藻中观察到的复杂基因活动波动。由于基于抑制的设计在像T7这样的外源聚合酶中也能起作用,因此有可能把这个最简时钟模块移植到其他微生物或无细胞体系中,使科学家能够为研究、工业生产或未来治疗应用编程日常节律性基因开关。
引用: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
关键词: 昼夜节律钟, 蓝藻, 转录调控, RpaA, 合成生物学