Clear Sky Science · zh
大规模分发阿奇霉素与肠道及鼻咽抗生素耐药性:一项集群随机试验
为何给许多孩子一片药很重要
在西非的部分地区,阿奇霉素这一抗生素已被用于大规模运动中,以减少幼童因感染死亡的数量。该策略有效——但也带来一个严重担忧:我们是否在儿童体内悄悄培育出更强壮、对药物耐受的微生物?这项在尼日尔数百个村庄开展的研究,深入采样儿童的肠道和鼻腔,观察反复的社区范围用药如何重塑他们隐蔽的微生物世界及其抗生素耐药性。
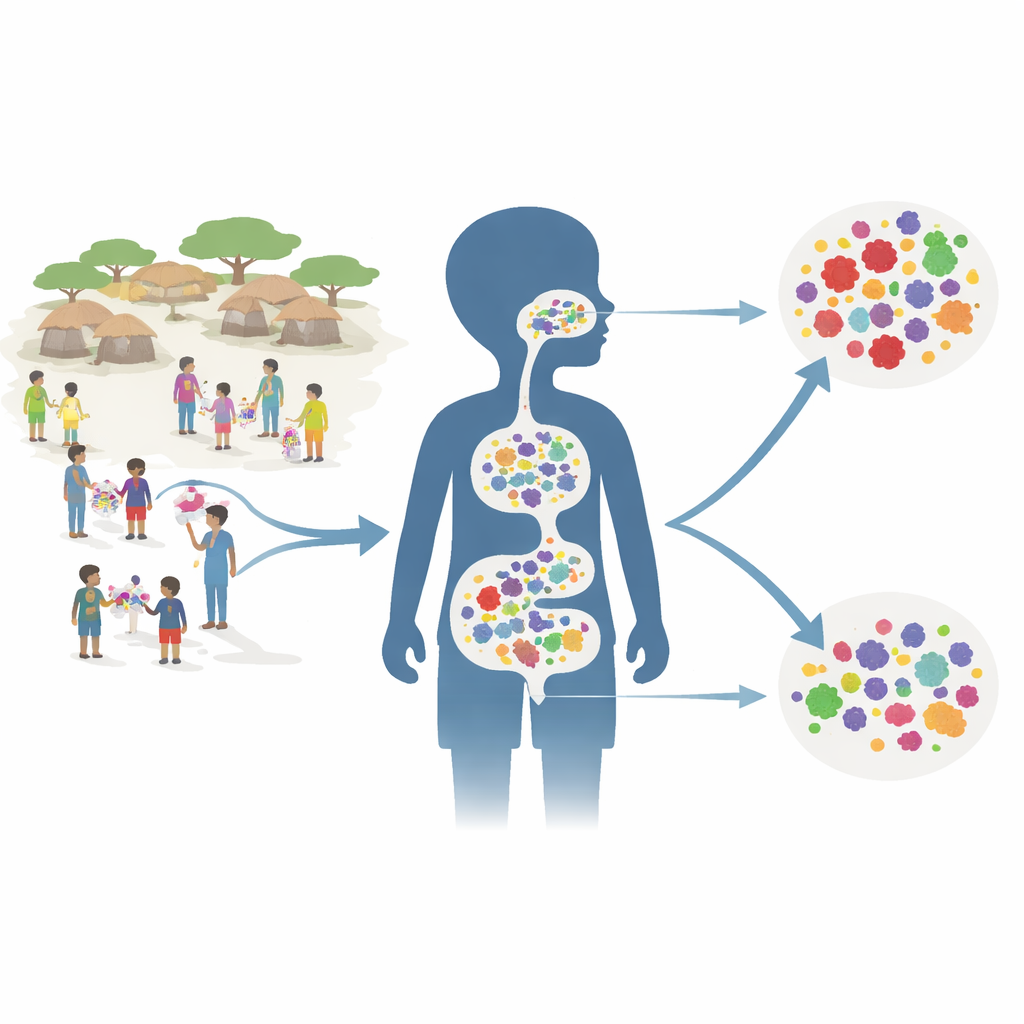
检验一项社区性用药计划
研究者将工作嵌入到一项名为 AVENIR 的大型试验中,该试验已显示每六个月向1至59个月儿童群体发放阿奇霉素,可降低该年龄段的死亡率。为耐药性研究,他们在150个随机挑选的村庄中取样。每个村庄属于三组之一:所有幼儿都接受阿奇霉素;仅0–11个月婴儿接受阿奇霉素,年长的幼儿和学龄前儿童服安慰剂;或所有儿童均服安慰剂。项目开展两年——在第四轮治疗后六个月——团队从每个村约30名儿童采集了直肠拭子和深部鼻拭子。
窥探肠道与鼻腔
研究人员未在培养皿中培养病原体,而是将每个村庄的样本汇合并采用现代DNA测序技术。这样他们能够目录化存在哪些细菌并计数显示对不同抗生素家族耐药的基因标记。他们特别关注大环内酯类——阿奇霉素所属的药物家族——同时也扫描对其他常用抗生素类型(如类似于青霉素的药物)的耐药基因。之所以检查肠道和鼻咽(鼻后上咽部),是因为两处都是耐药基因可能积累并潜在传播的重要储库。
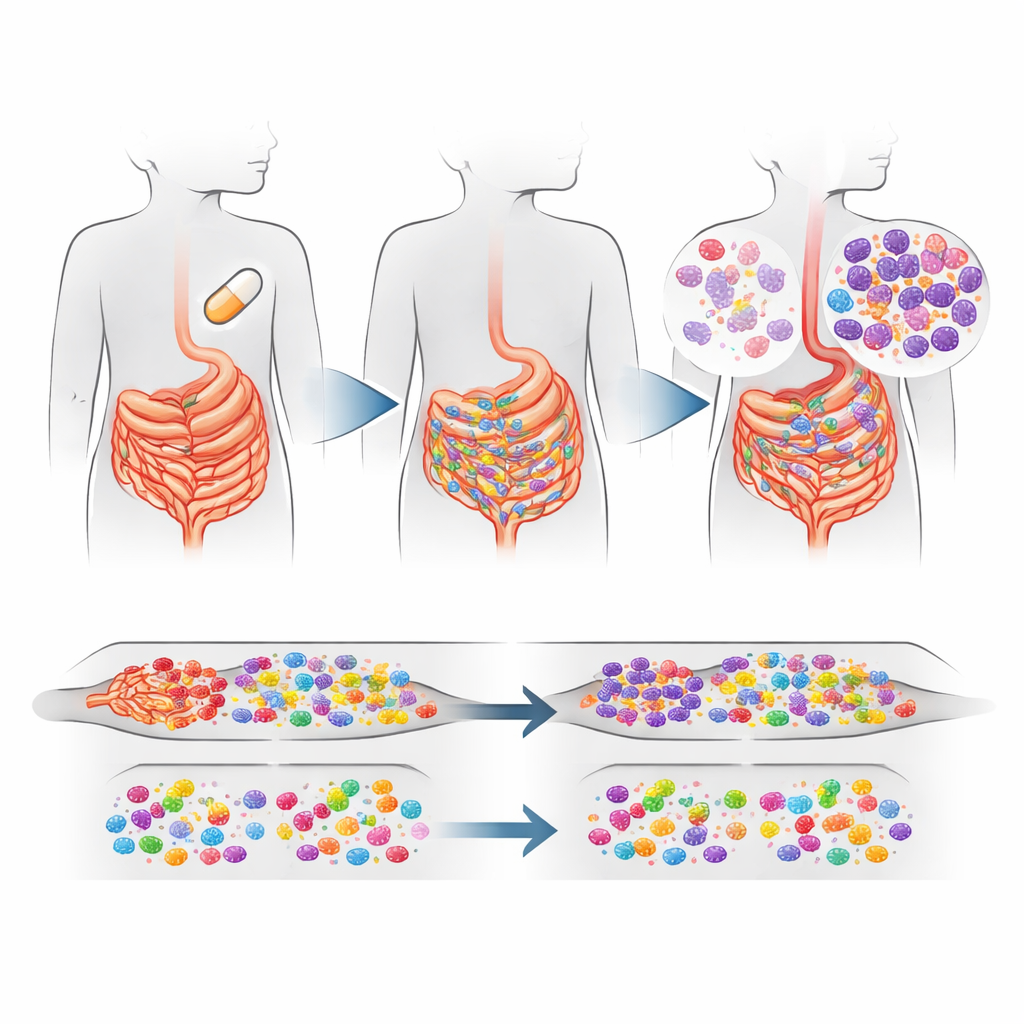
儿童肠道内部发生的变化
最明显的信号来自肠道。那些对所有儿童给予阿奇霉素的村庄,其肠道细菌中大环内酯类耐药基因总体上有温和但统计学上可靠的增加——大约高出16%,与安慰剂村庄相比。这一上升主要由一种名为 ermF 的耐药基因驱动,该基因帮助细菌抵御大环内酯类药物。该基因常见于诸如拟杆菌属(Bacteroides)和普氏菌属(Prevotella)等常见肠道细菌,这些细菌通常在肠道中无害共存,但有时也会致病。有趣的是,对其他主要抗生素家族的耐药基因并未增加,肠道细菌的总体构成和多样性在各治疗组间大体相似,尽管某些特定物种的丰度出现了升降。
鼻腔内保持相对稳定
相比之下,鼻腔的情况更为平静。研究未在鼻咽中发现不同处理组之间大环内酯类耐药基因存在明确且统计学上稳健的差异,也没有证据表明其他抗生素类别的耐药性在此处被选择性放大。典型的鼻腔常驻菌——如莫拉菌属(Moraxella)、嗜血杆菌属(Haemophilus)和链球菌属(Streptococcus)——仍然占主导。一些与口腔牙龈疾病相关的细菌在接受阿奇霉素的社区中变得更常见,其中部分也可能携带耐药基因,但鼻腔的总体耐药负荷并未像肠道那样发生明显变化。
在当下的收益与未来风险之间权衡
综合来看,研究结果表明,在社区中向所有幼儿发放阿奇霉素可以挽救生命,但也会推动肠道细菌对该药物家族的耐药性增加,主要是通过像 ermF 这样的特定耐药基因扩增驱动。研究在两年观察窗口内未见向其他抗生素类型的耐药蔓延,也未见鼻腔储库有强烈变化,但作者警告称,耐药肠道细菌及其基因可能随时间和人群传播扩散。他们主张,任何旨在减少儿童死亡的广泛抗生素计划都应内置谨慎的长期耐药性监测,以便卫生决策者在立即减少儿童死亡的好处与逐步、较隐蔽的增强耐药微生物的代价之间持续权衡。
引用: Doan, T., Yan, D., Arzika, A.M. et al. Mass azithromycin distribution and antibiotic resistance in the gut and nasopharynx: a cluster-randomized trial. Nat Med 32, 859–868 (2026). https://doi.org/10.1038/s41591-026-04217-9
关键词: 阿奇霉素, 儿童死亡率, 抗生素耐药性, 肠道微生物组, 大规模药物分发