Clear Sky Science · zh
对肿瘤抗原的体液性 IgG1 反应支撑免疫检查点抑制疗法的临床结局
这对癌症患者为何重要
免疫疗法通过动员机体自身防御来攻击肿瘤,已改变癌症治疗格局,但只有部分患者能受益。大多数研究关注的是一种免疫战士——T 细胞——但本研究揭示,另一类产抗体的 B 细胞也能决定疗效成败。研究显示,一种特定的抗体反应——称为 IgG1——与更好结局相关,这一结果指向了新的方法来预测谁会从免疫疗法中获益,以及如何让更多患者受益。
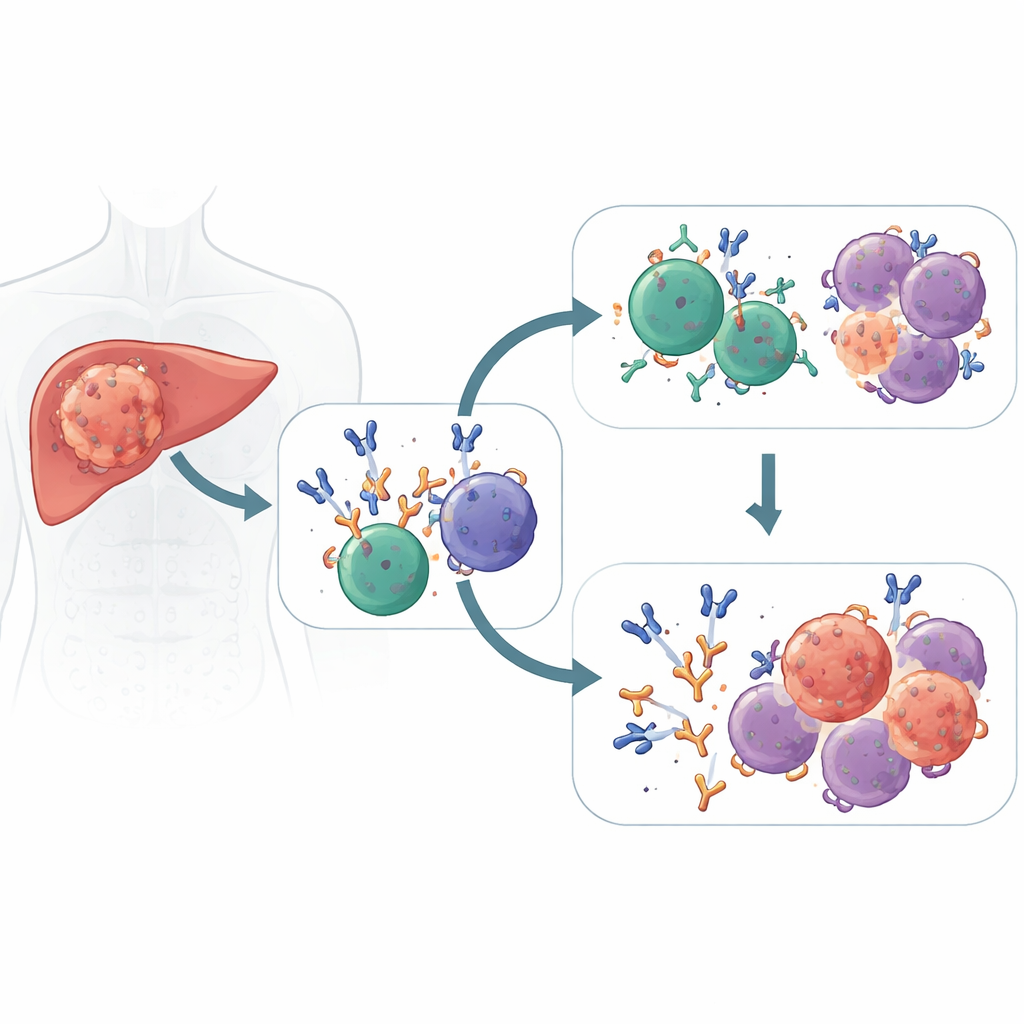
两条防线协同作战
现代药物称为免疫检查点抑制剂,能松开 T 细胞的“刹车”,使其识别并杀死癌细胞。研究者在接受术前此类药物的肝癌患者中发现,疗效良好的患者并不单靠 T 细胞。他们的肿瘤中也充斥着浆细胞——成熟的 B 细胞,像迷你抗体工厂一样——产生以肿瘤为靶的优势性 IgG1 抗体浪潮。相反,肿瘤未显著缩小的患者肿瘤内有更多处于静止或功能异常的 B 细胞,而这些特化的浆细胞更少。
沿着抗体足迹追踪全身
为了解这些有益浆细胞的来源,团队将单细胞测序与对每个 B 细胞所携带独特抗体“条码”的精细追踪相结合。他们发现,疗效良好的患者在肿瘤与邻近淋巴结中都有扩增的、密切相关的 IgG1 产生细胞群——淋巴结是免疫系统的指挥中心。同样的克隆签名在治疗前就已出现,治疗后进一步扩增,表明检查点抑制放大了既有的、对肿瘤有反应的 B 细胞克隆,而不是完全新生出这些克隆。这提示训练有素的抗体产生细胞在淋巴结与肿瘤部位之间存在协调循环。
抗体如何重塑肿瘤微环境
显微成像与空间基因图谱显示,在应答者体内,浆细胞并非停留在肿瘤边缘——它们深入肿瘤内部,伴随杀伤性 T 细胞与有利的巨噬细胞。这些区域富含促进 B 细胞激活与抗体生成的信号,形成了为攻击优化的免疫“社区”。相比之下,未应答者在纤维化的基质口袋中积累记忆样 B 细胞与调节性免疫细胞,抑制了有效反应。在多个独立患者队列和不同免疫治疗组合中,向 IgG1 产生浆细胞倾斜始终与更好的肿瘤控制和较慢的疾病进展相关联。
识别肿瘤特异性标志的抗体
由于浆细胞会将抗体分泌到血液中,研究者进一步询问这些分子能否在血液样本中检测到。在许多应答者中,他们发现针对所谓癌-睾丸抗原的高水平 IgG1 抗体——例如通常在正常组织缺失但在肿瘤中重新出现的 NY-ESO-1。具有这些抗体的患者也更可能对相同靶点表现出强烈的 T 细胞活性,这暗示抗体有助于将肿瘤片段呈递给细胞免疫分支。来自黑色素瘤和肺癌的大规模生存数据集证实,具有强烈 IgG1 特征的肿瘤更易对检查点药物产生反应,而主要以标准化疗为主的肿瘤则未显示出此类关联。
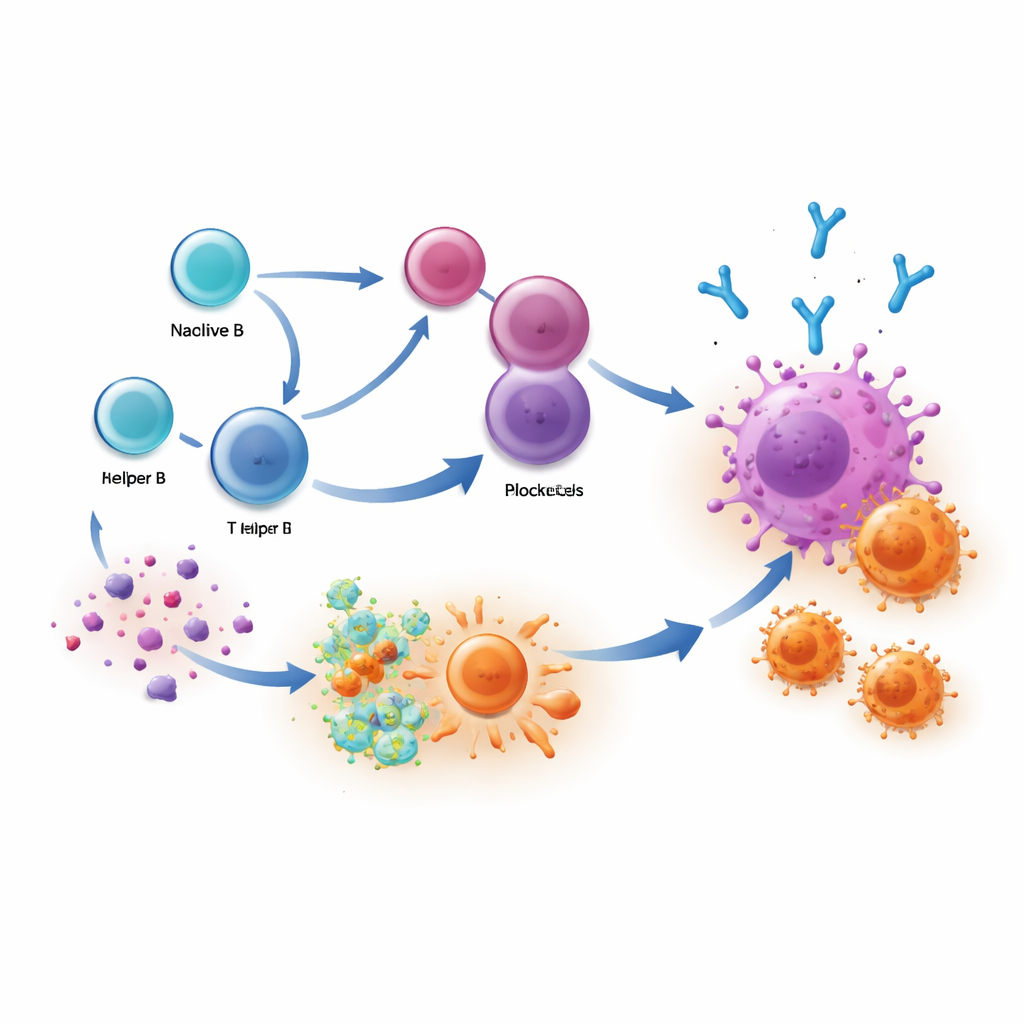
这对未来治疗的意义
简言之,当免疫系统发起双管齐下的攻击时,患者获益最大:来自浆细胞的 IgG1 抗体为癌细胞做标签,T 细胞则进行清除。该研究表明,检查点疗法可增强这些抗体反应,尤其是在治疗前就存在有益的 B 细胞克隆时。测量富含 IgG1 的浆细胞或在血液与肿瘤样本中检测这些抗体,可能帮助医生识别潜在应答者并监测疗效。长远来看,旨在引导 B 细胞产生更多这种精确、趋向肿瘤的 IgG1 抗体的疫苗或药物,或可放大免疫疗法的益处,使更多癌症患者获得持久反应。
引用: Gonzalez-Kozlova, E., Sweeney, R., Figueiredo, I. et al. Humoral IgG1 responses to tumor antigens underpin clinical outcomes in immune checkpoint blockade. Nat Med 32, 978–991 (2026). https://doi.org/10.1038/s41591-025-04177-6
关键词: 癌症免疫疗法, B 细胞, IgG1 抗体, 免疫检查点抑制, 肝细胞癌