Clear Sky Science · zh
针对GPRC5D的T细胞接合剂在多发性骨髓瘤中的多模态抗原逃逸
当癌症智胜精准免疫疗法时
强效的新型免疫药物正在改变多发性骨髓瘤的治疗,这是一种对大多数患者仍无法治愈的血液恶性肿瘤。这类疗法通过将机体自身的T细胞重新导向去识别并摧毁表面带有特定“标志”的肿瘤细胞来发挥作用。一个有前景的标志是名为GPRC5D的分子。然而,与许多靶向疗法一样,肿瘤可以演化并规避治疗。本研究以不同寻常的细致程度揭示了骨髓瘤细胞如何改变或隐藏GPRC5D标志,以逃避高度有效的T细胞接合药物。
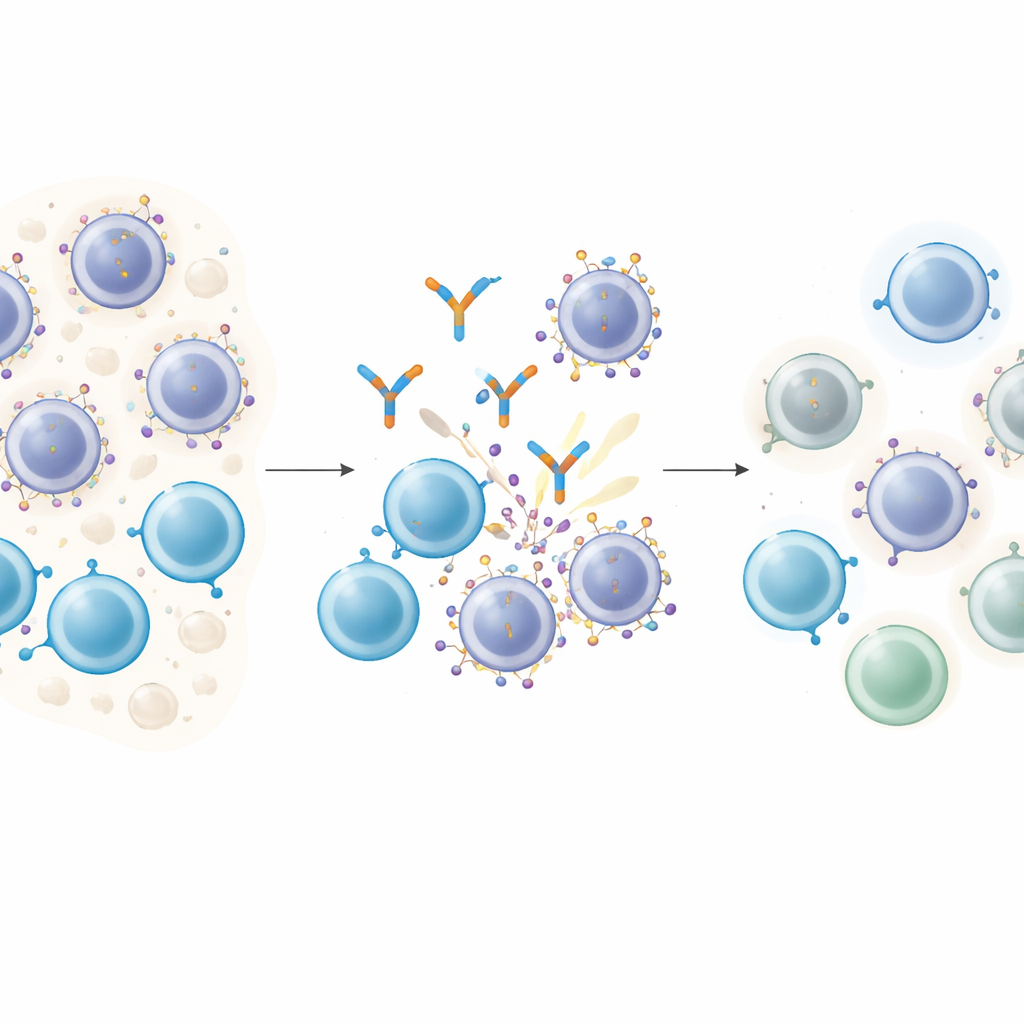
智能药物如何锁定癌细胞
T细胞接合抗体作用如同分子媒人:一端抓住T细胞,另一端连接到癌细胞表面的靶分子,将两者拉到直接接触,使T细胞能够杀死目标。在多发性骨髓瘤中,GPRC5D是一个有吸引力的靶点,因为它在恶性浆细胞上丰度高,而在大多数正常组织中稀少。接受针对GPRC5D的药物talquetamab治疗的患者常出现深度缓解。然而,几乎所有患者最终都会复发,这提出了一个关键问题:癌细胞是否在改变这些药物依赖的靶点?
实时追踪肿瘤演化
研究人员随访了21名接受talquetamab治疗的难治性骨髓瘤患者。他们在部分患者治疗前和癌症复发时采集了骨髓样本,并结合多层次的DNA、RNA和染色质分析来检查肿瘤细胞。这种超细致的观察发现,在约三分之二复发患者中,癌细胞以多种方式改变了GPRC5D,足以削弱或阻断药物效果。显著的是,若干不同的耐药亚克隆——肿瘤的基因上不同分支——常在同一患者体内共存,表明朝向逃逸的演化可同时沿多条路径进行。
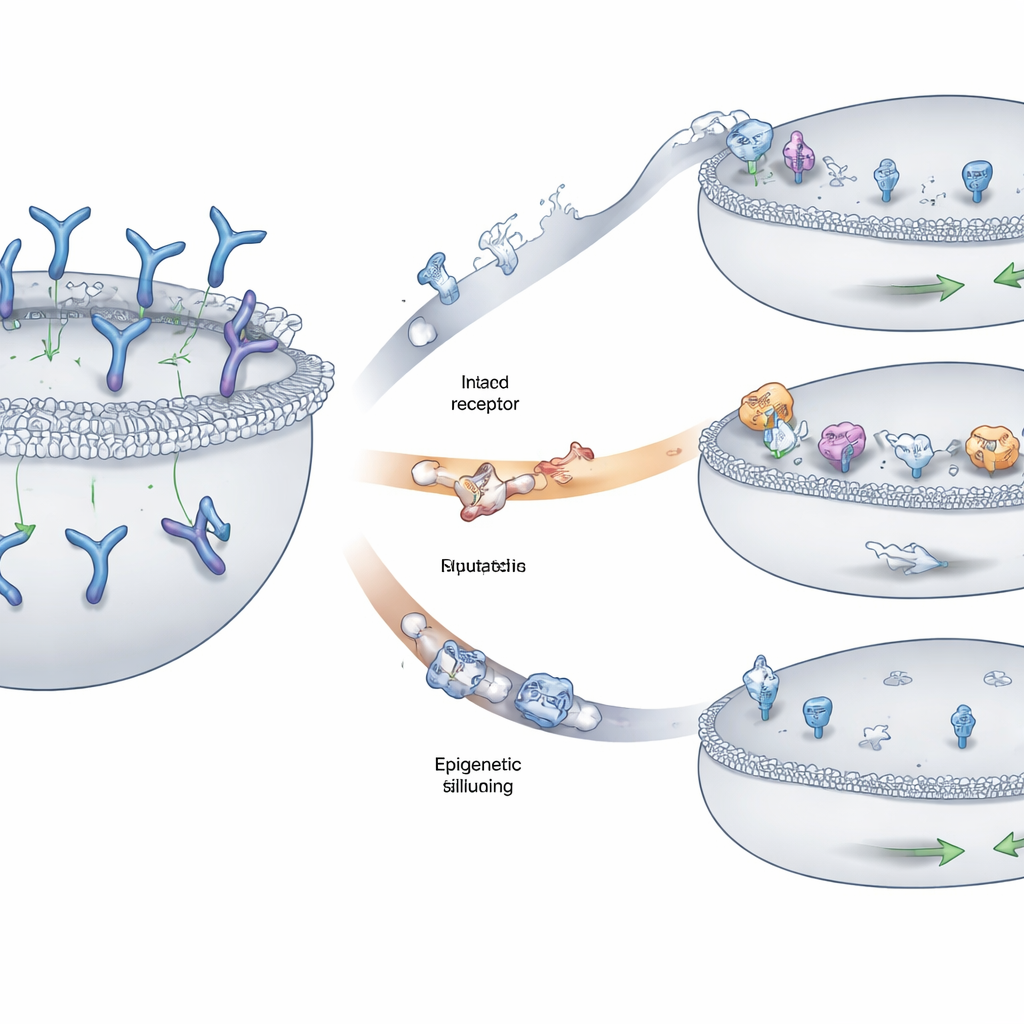
肿瘤隐藏靶点的三种主要方式
研究组发现了骨髓瘤细胞逃避识别的三种反复出现的模式。在一些患者中,携带GPRC5D基因的染色体片段在两套拷贝上被删除,完全抹除细胞表面的标志。另一些患者则出现较小的改变——单个碱基置换或微小的插入/缺失——扭曲了GPRC5D蛋白的关键区域。许多这些改变破坏了蛋白质从细胞内部正确运输到外膜所需的部分,导致GPRC5D滞留在细胞内的隔室,而非展示在药物可见的位置。第三条路径涉及表观遗传沉默:围绕GPRC5D的DNA被紧密包装并带有化学标记,使该基因几乎不被读取,尽管其底层序列大体完好。使用这种策略的肿瘤细胞几乎不产生GPRC5D。
当标志仍在但“锁”不再匹配
并非所有的逃逸途径都将GPRC5D从细胞表面移除。在某些情况下,蛋白在常规实验检测下看起来正常,但已不再像钥匙与锁那样适配药物。研究团队在实验室细胞系中重建了来自患者的特定突变,并测试了不同GPRC5D靶向抗体对这些细胞的结合与杀伤能力。一种突变微妙地改变了talquetamab握住受体的精确位点,大幅降低了该药的结合能力和诱导细胞死亡的效果,尽管受体在常规染色中仍可见。有趣的是,一种以双位点结合受体的另一款GPRC5D靶向药对几种此类突变仍然有效,强调了药物设计(例如采用多价或多表位结合)如何影响耐药克隆能否存活。
超出靶点:免疫攻击的其他限制
尽管大多数复发显示出某种形式的GPRC5D丢失或改变,但少数患者在靶点本身未见明显变化的情况下复发。在这些病例中,问题似乎出在T细胞:它们在实验室测试中表现出更差的功能和较低的杀伤能力,提示长期持续暴露于接合剂疗法可能导致免疫系统疲劳。研究还发现,一种特定的骨髓瘤遗传亚型(涉及称为t(11;14)的染色体易位)天然使GPRC5D基因处于更“封闭”的染色质状态,基础表达更低。这提示某些患者可能天然更易出现较差反应,因为他们的肿瘤起始时标志物水平就偏低。
这对患者与未来治疗意味着什么
对于患者和临床医生来说,这项工作解释了为何即便是高效的GPRC5D靶向疗法仍然无法根治:骨髓瘤细胞可以删除、重排、误导运输或关闭这些药物依赖的标志,而且它们常在多条路径上同时实现这些变化。研究结果表明,监测肿瘤DNA而不仅仅是测定蛋白水平,对检测常规实验可能遗漏的新兴逃逸突变将至关重要。研究还指向下一代策略——例如在多个位点更强力结合GPRC5D的药物、同时打击多个靶点的组合疗法,或能重新开启被沉默基因的药物——以领先于肿瘤演化。本质上,这项研究绘制了骨髓瘤的逃逸路线图,使未来的疗法能够设计以阻断这些路径,从而使基于T细胞的治疗更长久地保持有效。
引用: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
关键词: 多发性骨髓瘤, T细胞接合剂, GPRC5D, 抗原逃逸, 癌症免疫疗法