Clear Sky Science · zh
发现与开发一种用于治疗结核病且毒性降低的新型恶唑烷酮
对抗顽固杀手的新希望
结核病(TB)仍然是全球最致命的传染病之一,每年造成超过一百万人死亡。治疗通常持续数月,有些结核分枝杆菌菌株已对多种药物产生耐药性,使治愈变得更加困难。本研究描述了一种新的试验性抗生素,称为MK-7762,旨在对抗结核具有强效活性,同时避免限制旧药利奈唑胺使用的一些严重副作用。如果在人类中成功,MK-7762可能有助于缩短疗程并将现代结核疗法推广到更多患者。
为何当今有效的结核药物难以广泛使用
利奈唑胺属于称为恶唑烷酮的一类抗生素,对高度耐药的结核患者来说是一项突破。与其他新药联合使用时,它已帮助将曾被判定无望的病例转为可治愈,并已改变世界卫生组织的治疗指南。但利奈唑胺也会损害人体自身细胞,特别是骨髓和神经,因为它干扰了人细胞“能量工厂”线粒体中的微小蛋白质制造机器。这些副作用——如贫血、神经疼痛和视力问题——使得利奈唑胺通常保留给病情最严重、别无选择的患者,而不是广泛用于对标准药物仍敏感的结核患者。
设计更聪明的结核抗生素
研究团队着手开发一种保留利奈唑胺优点——对结核具有强效活性——同时大幅降低其损害人类细胞倾向的药物。他们合成并测试了约2800种化学变体,寻找那些能有效杀灭结核分枝杆菌但对线粒体蛋白质合成影响很小的分子。一种有希望的化合物MK-7762从这次详尽的筛选中脱颖而出。在实验室测试中,它抑制结核生长的效力优于利奈唑胺,但对线粒体功能的干扰明显较弱,这表明血液和神经毒性风险可能更低。
该药物如何选择性攻击结核而保全我们自身细胞
为了解MK-7762为何更具选择性,科学家们使用高分辨率冷冻电子显微镜观察药物如何位于结核菌蛋白质合成机器——核糖体内。他们发现MK-7762嵌入于分枝杆菌核糖体的一个口袋中,药物上的特定化学基团与细菌RNA的一个构件形成了稳定的键。在人类线粒体中,对应的RNA片段取向不同,实际上与药物的这一部分发生排斥,使结合远不如在细菌中有利。这一微妙的结构差异有助解释MK-7762如何在抑制结核菌蛋白质合成的同时在很大程度上避免影响人类细胞中的同类机器。
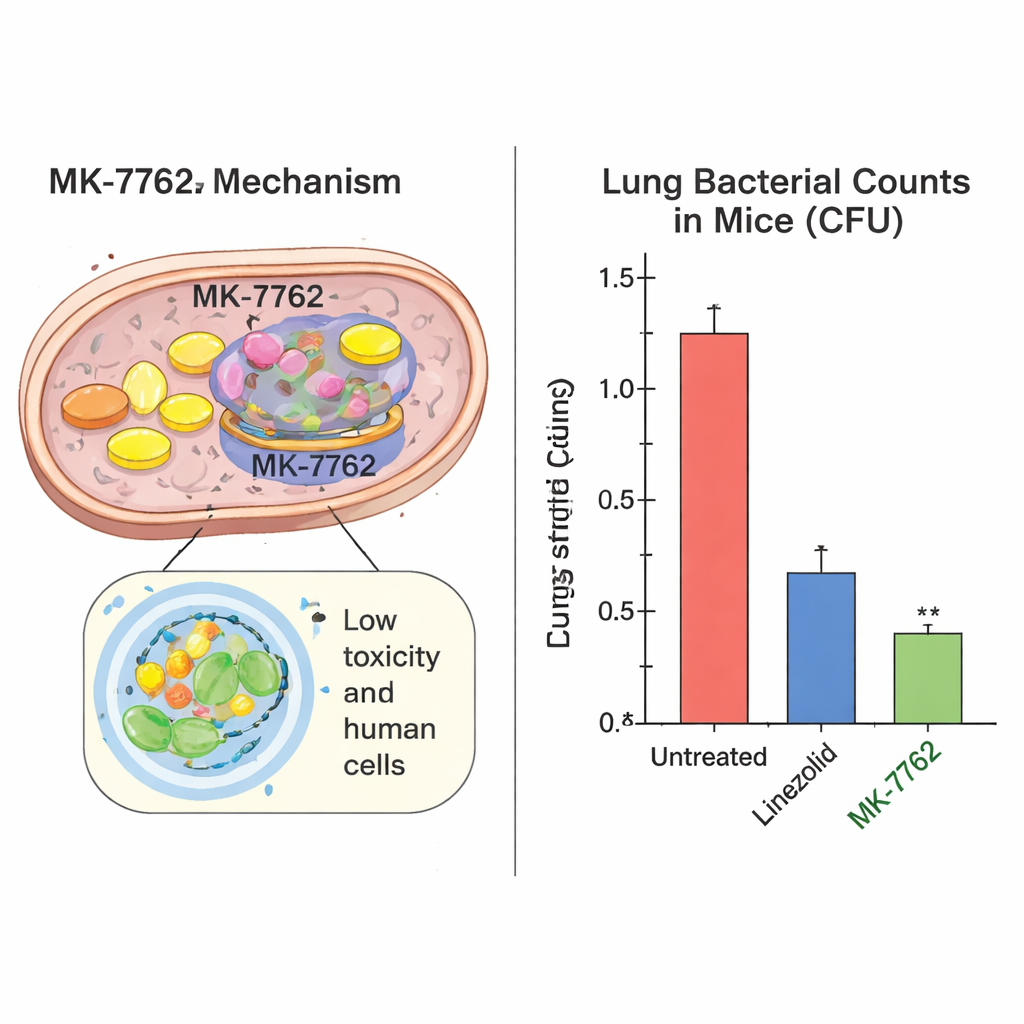
动物研究中效力与安全性的证据
团队随后在结核感染的小鼠中测试了MK-7762。在急性(早期)感染模型中,MK-7762一次每日给药显著降低肺部细菌数量——最多约10万倍——在相似或更低剂量下与利奈唑胺相当或更优。在慢性(长期)感染模型中,MK-7762的表现至少不逊于利奈唑胺。关键是,该药能到达结核常隐匿的、难以穿透的“奶酪样”肺病灶,并在这些部位达到高于抑制大多数临床结核菌株所需水平的浓度,持续数小时。在大鼠和犬的研究中,MK-7762显示出较大的安全窗:动物耐受的暴露量远高于按预期人类每日100毫克剂量时的水平,仅出现轻微且可逆的血象变化,且在四个月给药期间未见明确的骨髓或器官损伤迹象。
这对未来结核治疗意味着什么
综合来看,这些结果表明MK-7762将利奈唑胺的优点与更温和的安全特性结合起来。它对多种敏感和耐药结核菌株仍然有效,在体内的药代动力学特性应允许方便的一次每日给药,并且似乎不太可能引起限制利奈唑胺使用的线粒体相关副作用。尽管仍需通过人体试验来确认其益处并发现任何新的风险,MK-7762提出了一种更安全的恶唑烷酮有可能成为更短疗程、全口服治疗组合的一部分,适用于几乎所有形式的结核——而不仅仅是最耐药的病例。
引用: Crowley, B.M., Boshoff, H.I., Boving, A. et al. Discovery and development of a new oxazolidinone with reduced toxicity for the treatment of tuberculosis. Nat Med 32, 553–560 (2026). https://doi.org/10.1038/s41591-025-04164-x
关键词: 结核病, 抗生素, 耐药性, 利奈唑胺, MK-7762