Clear Sky Science · zh
Repotrectinib治疗NTRK融合阳性晚期实体瘤:1/2期临床试验
来自一种靶向口服药的新希望
癌症治疗越来越像精密工具而非粗糙的利器。本研究评估了repotrectinib,这是一种针对肿瘤携带稀有基因改变——即NTRK融合——患者的靶向口服药。尽管这些融合在实体瘤中少于1/100的发生率,但它们可出现在包括肺、甲状腺和软组织在内的多种器官,并常对专门设计的药物产生显著反应。问题在于早期药物最终会失效。本试验提出了一个简单但意义重大的问题:下一代更聪明的药物能否在更长时间内控制癌症,即便在其他靶向疗法失效之后?
稀有但强大的癌症开关
某些癌症由称为NTRK1、NTRK2和NTRK3基因的融合驱动。这些融合像肿瘤细胞中持续开启的生长开关。阻断由此产生的TRK蛋白的一代药物已帮助许多患者,但随着时间推移,癌细胞常通过在药物结合位点获得新突变来逃避药物。repotrectinib被设计得更小、更紧凑,因此即使在这些变化发生后仍能进入结合口袋。国际TRIDENT‑1试验在成人晚期携带NTRK融合的实体瘤患者中测试了该药物,包括既从未接受过TRK抑制剂的患者,也包括癌症已耐受一到两种早期TRK抑制剂的患者。
试验设计
该研究在全球多中心招募了144例NTRK融合阳性的实体瘤患者;其中120例构成了主要疗效评估人群。肿瘤类型至少涵盖18种,最常见的是非小细胞肺癌、甲状腺癌、涎腺肿瘤和软组织肉瘤。所有患者均为局部晚期或转移性疾病,许多人已接受多种其他治疗,包括化疗、免疫疗法或早期TRK抑制剂。患者按每日口服给药,剂量方案基于早期研究确定。研究者跟踪肿瘤缩小的患者比例、反应持续时间、无进展生存时间以及药物的耐受性。
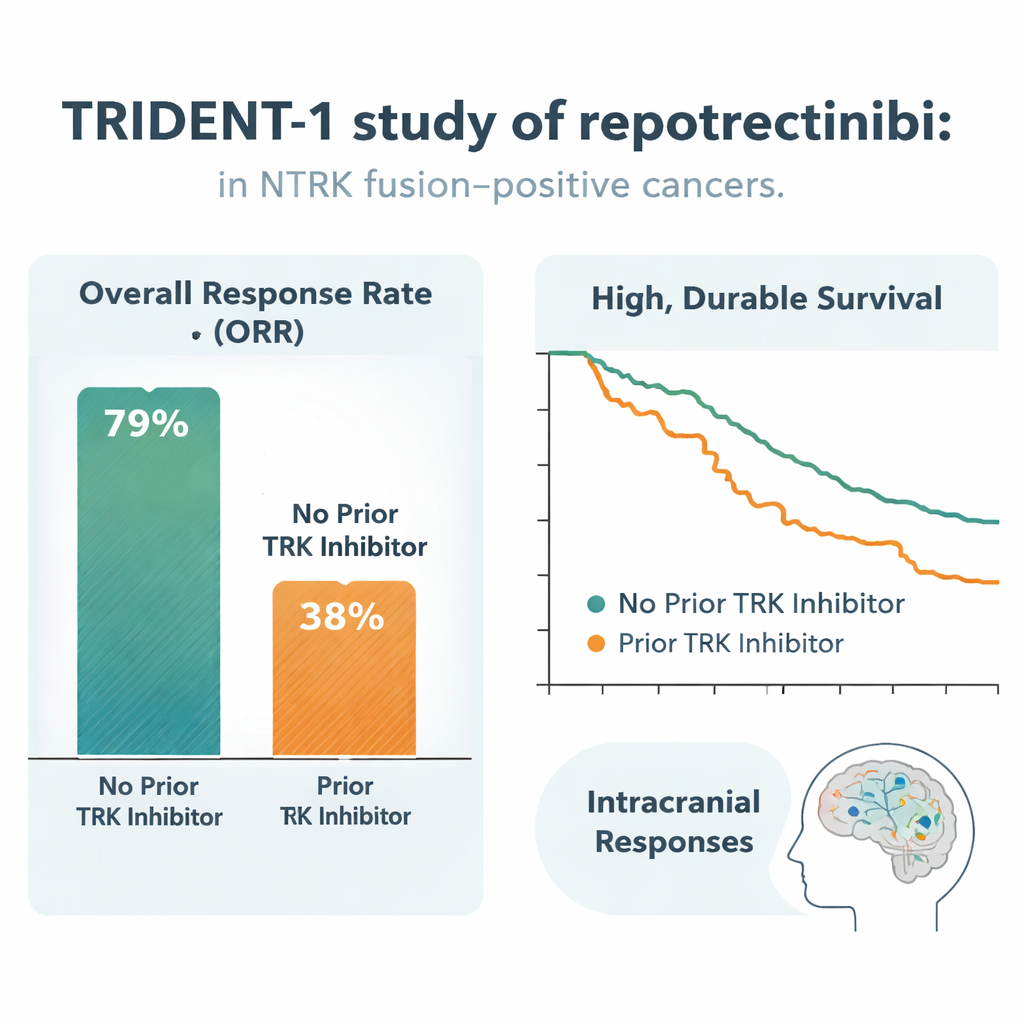
强劲且持久的反应
在51例未接受过TRK抑制剂的患者中,59%出现足以计为客观缓解的肿瘤缩小,16%在影像学上肿瘤消失。反应通常出现迅速——约两个月内——且持续时间显著:两年后,估计85%的应答者仍在受益,全组约60%尚未出现疾病进展。即便在69例已接受过其他TRK药物并病情进展的较多预处理患者中,48%对repotrectinib有反应,典型应答持续约10个月,约四分之一患者在一年时仍无进展。重要的是,这种获益跨越多种肿瘤类型,与涉及哪个NTRK基因或融合伴侣关系不大。
应对耐药和脑内疾病
TRK药物的一大挑战是所谓的溶剂前突变,这些是发生在药物结合口袋中特定改变,会阻断早期药物。在本次试验中,近一半的既往接受治疗患者在基线时携带此类突变。即便在这个难治的亚组中,53%在使用repotrectinib后出现有意义的肿瘤缩小,证实该药能克服至少部分耐药形式。大脑是癌症常常潜伏的地点,也是研究重点。在基线时有可测量脑转移的患者中,未经治疗组的3人中有2人、既往治疗组的6人中有4人的脑部肿瘤出现缩小,且常维持数月。对于起始时无脑转移的患者,随访期间绝大多数仍无新发脑病灶。
副作用及其对患者的意义
在本研究及相关人群中,超过500名使用repotrectinib的受试者中最常见的不良反应为头晕、味觉改变和发麻感,多数为轻中度。更严重的治疗相关问题如贫血或肌酶升高较少见,约有4%的患者因副作用停药。总体生活质量指标在多数参与者随多次治疗周期保持稳定或有所改善。综合来看,结果表明repotrectinib能够为NTRK融合阳性癌症提供持久控制——包括那些已对早期TRK药物耐药及已扩散至脑的病例——同时总体可耐受。对于这些罕见但具有侵袭性的肿瘤患者,研究支持repotrectinib成为精准癌症治疗日益扩展工具箱中的一项重要新选择。
引用: Besse, B., Lin, J.J., Bazhenova, L. et al. Repotrectinib in NTRK fusion–positive advanced solid tumors: a phase 1/2 trial. Nat Med 32, 682–689 (2026). https://doi.org/10.1038/s41591-025-04079-7
关键词: 靶向癌症治疗, NTRK融合, repotrectinib, TRK抑制剂耐药, 脑转移