Clear Sky Science · zh
Flt3L介导的肿瘤cDC1扩增通过在淋巴结中激发干样CD8+ T细胞增强免疫治疗
帮助免疫系统记住如何抗击癌症
为什么有些人的肿瘤在现代免疫治疗下迅速消退,而另一些人几乎没有受益?本研究深入免疫系统内部寻求答案。研究者表明,通过增强肿瘤中一类特定的哨兵细胞,他们可以在邻近的淋巴结中培育出一池长期存在的“干样”杀伤性T细胞。这些细胞反过来使常规的检查点抑制药物,特别是抗‑CTLA‑4治疗,更加有效且疗效持续更久。
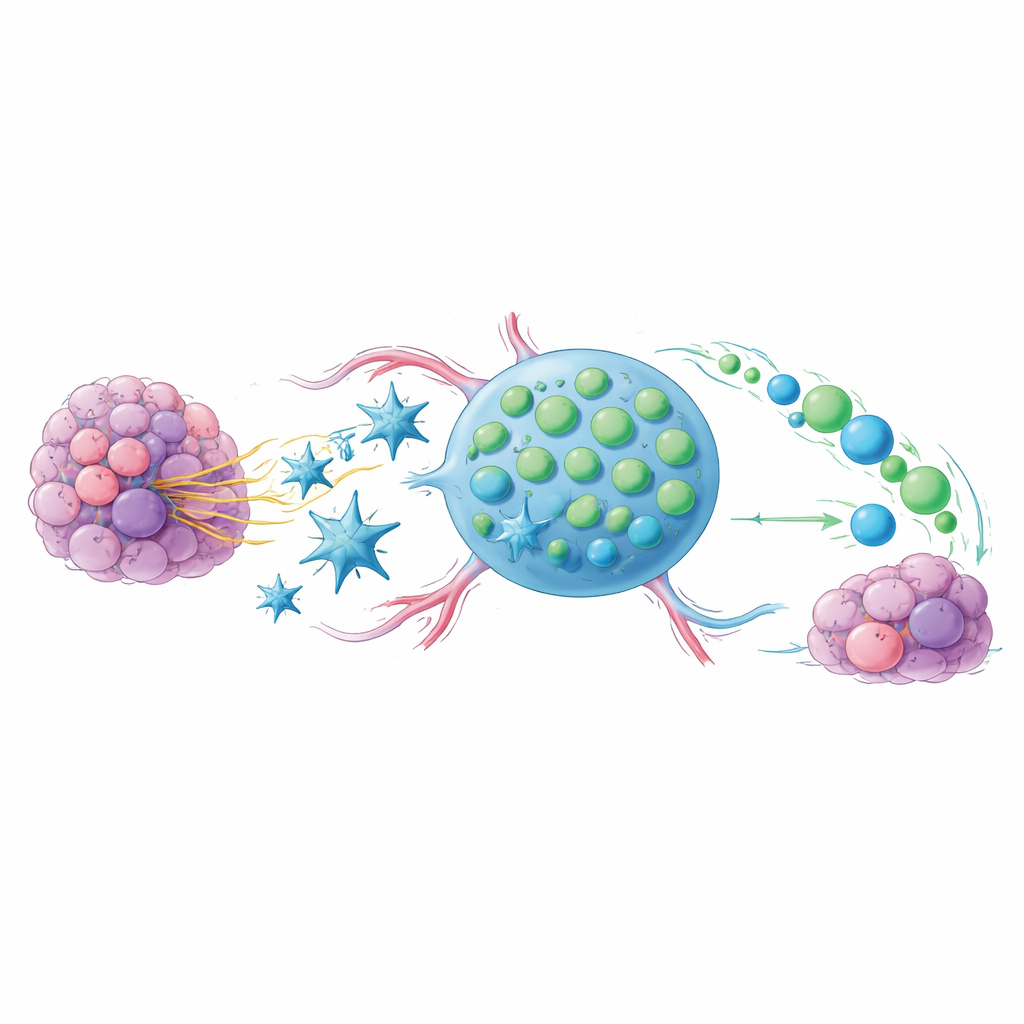
疲惫的抗肿瘤细胞之困
抗‑PD‑1和抗‑CTLA‑4等检查点药物能释放免疫细胞对抗癌症,但只有一部分患者从中获益。一个线索来自于CD8 T细胞的状态,这类细胞是清除受感染或癌变细胞的主要刺客。当这些T细胞被长期高强度推动时,会进入一种耗竭状态,停止有效增殖。然而,有一小部分细胞保持较为年轻的干样特性:它们容易分裂、产生新的战斗细胞,并且与接受检查点治疗的良好反应密切相关。本研究的核心问题是如何促使肿瘤及其微环境偏向产生这些干样细胞,而非那些已耗竭的同类。
为肿瘤的哨兵细胞注入能量
研究团队聚焦于常规1型树突状细胞(cDC1),这是一类罕见但功能强大的免疫哨兵,擅长将肿瘤片段呈递给T细胞。他们使用一种生长信号Flt3配体(Flt3L)在小鼠肿瘤内扩增这类细胞,方法是使癌细胞分泌Flt3L或直接作为药物给药。单细胞RNA测序显示,富含Flt3L的肿瘤包含更多的树突状细胞和淋巴细胞以及更少的肿瘤细胞。在树突状细胞群内,有三类不同亚群扩增,其中一类高度成熟并准备迁移到淋巴结,在那里T细胞首次接受训练。与此同时,肿瘤内的CD8 T细胞从终末耗竭表型转向更具干样或记忆样的状态。
在淋巴结中建立干样T细胞储备
通过追踪肿瘤特异性T细胞并使用遗传学工具,研究者表明Flt3L治疗增强了一群在表面具有与干样潜能和细胞活跃分裂相关标志的CD8 T细胞。这些细胞依赖于表达XCR1的树突状细胞以及由CCR7引导的树突状细胞从肿瘤向引流淋巴结迁移。当树突状细胞被清除或其迁移被阻断时,干样T细胞库就会缩小。阻断淋巴细胞从淋巴结外流也有类似效果,切断了向肿瘤输送更新T细胞的来源。分子谱分析显示,这一过程依赖转录因子Myb,并且有利于识别肿瘤靶点强度相对较低的T细胞——这一类群日益被认为对持久的肿瘤控制十分重要。
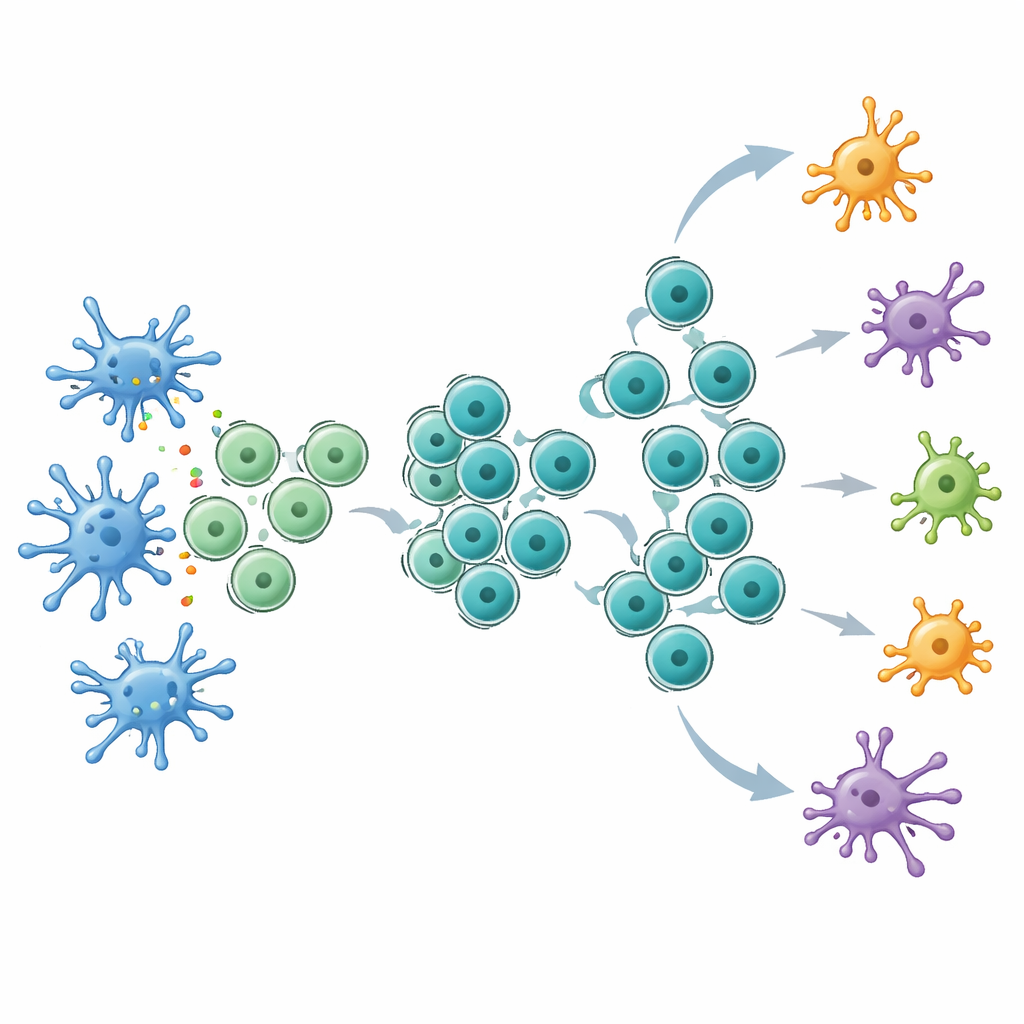
让检查点治疗更有效
有了这一扩增的干样T细胞储备,接受治疗的小鼠对检查点抑制的反应显著改善,尤其是对抗‑CTLA‑4治疗。接受Flt3L处理的动物肿瘤缩小更多、存活期延长,血液和淋巴结中也有更多肿瘤特异性T细胞。在肿瘤内,Flt3L增加了干样CD8细胞,而随后施用CTLA‑4阻断则促使这些细胞成熟为能够产生大量关键抗肿瘤分子的强效效应细胞。T细胞受体测序显示,联合疗法拓宽了扩增克隆的范围,包括许多次主导克隆,提示对癌症的攻击更加多样化。详细的单细胞分析发现了一类独特的CD8 T细胞簇,其特征是表达免疫信使IL‑21的受体,处于干样与耗竭状态之间,并与早期和晚期群体共享T细胞受体。阻断IL‑21信号会削弱Flt3L与抗‑CTLA‑4联合治疗的益处。
这对未来癌症治疗的意义
对非专业读者而言,这项工作的要点是,成功的免疫治疗不仅需要更强地激活免疫系统,还需要拥有合适类型的细胞来被激活。研究表明,通过Flt3L供给并引导树突状细胞,可以在邻近淋巴结中储备一池可再生的干样杀伤性T细胞。当随后使用如抗‑CTLA‑4等检查点药物时,便可动用这一储备,产生更多、更具多样性且更能控制肿瘤的新一波战斗细胞。对人类癌症数据库的分析表明,与该通路相关的基因特征也能预测患者更好的结局。总体而言,这些发现指向一种组合治疗策略:先用像Flt3L这样的药物构建合适的免疫细胞“种源”,然后用检查点抑制药释放它,以实现更强、更持久的癌症控制。
引用: Lai, J., Chan, C.W., Armitage, J.D. et al. Flt3L-mediated tumor cDC1 expansion enhances immunotherapy by priming stem-like CD8+ T cells in lymph nodes. Nat Immunol 27, 530–542 (2026). https://doi.org/10.1038/s41590-026-02419-4
关键词: 癌症免疫治疗, 树突状细胞, 干样CD8 T细胞, 检查点抑制, Flt3配体