Clear Sky Science · zh
CD38 赋予局部抗原特异性调节性 T 细胞对压力的耐受性,以控制区域性中枢神经系统炎症
为何守护大脑的免疫细胞重要
许多自身免疫性脑疾病,如多发性硬化,表现得像隐隐燃烧的火:最初的炎症狂潮平息后,损伤可能在数年后再次爆发。本研究提出了一个看似简单但影响深远的问题:在中枢神经系统(CNS)的一次发作后,是什么维持了和平——又是什么让局势重新转向疾病?作者聚焦于一小群在炎症后定居于脑与脊髓的免疫细胞——调节性 T 细胞,揭示了单一表面分子如何装备它们以在恶劣环境中生存并防止复发。
留下来的免疫维持者
研究人员使用模拟多发性硬化某些方面的小鼠模型,追踪不同类型的 T 细胞,在疾病上升到高峰并进入恢复期时观察其变化。随着症状好转,驱动炎症的常规辅助性 T 细胞数量减少,而通常抑制免疫反应的调节性 T 细胞则留在 CNS 中。它们在局部 T 细胞群体中的相对占比实际上增加,并聚集在脑脊液空间周围和覆盖脑的保护膜等特定利基中。通过标记流入细胞的来源,团队显示在恢复后,很少有新的调节性 T 细胞从淋巴结迁入。相反,CNS 内的这类细胞群主要在本地维持自身,暗示存在长期驻留的“维和”力量。 
能耐受压力的利基守护者
炎症后的 CNS 对这些守护者来说远非舒适。在主要的疾病浪潮过去后,调节性 T 细胞强烈依赖的生长信号白细胞介素-2(IL-2)水平下降,因为大多数常规 T 细胞已经退缩。与此同时,组织中富含代谢分子 NAD+,它在被特定酶修饰时会触发细胞死亡或削弱关键表面受体。通过对单个调节性 T 细胞进行基因标记与追踪,作者将“稳定”保持其身份的细胞与失去典型 Foxp3 程序的“不稳定”细胞区分开来。稳定细胞表现出更强的 IL-2 信号签名和更高水平的 IL-2 受体,表明在这种受压环境中感知稀少 IL-2 的能力对生存至关重要。
来自脑内的局部复发控制
为检验这些驻留调节性 T 细胞是否确实对长期疾病控制重要,研究人员通过直接将毒素注入脑脊液,选择性地清除 CNS 中的调节性 T 细胞,同时保留体内大部分系统性调节性 T 细胞。数日内,正在恢复的小鼠出现严重复发并再次瘫痪。相比之下,只在体内清除调节性 T 细胞而保留 CNS 内的细胞并未引发复发。此次复发涉及已驻留于 CNS 的效应性 T 细胞的快速再激活与扩增,即便阻断了它们从血液的新增募集。该结果表明,控制残留的侵袭性细胞依赖的是局部的调节性 T 细胞,而非循环的调节性细胞。
一种酶如何保护调节性细胞
深入研究中,作者寻找区分耐压 CNS 调节性 T 细胞的分子。关键角色浮现:CD38——一种位于细胞表面的酶,可分解细胞外 NAD+。在发炎的 CNS 中,调节性 T 细胞显著上调 CD38,而常规 T 细胞并未显示同样明显的变化。当团队将缺失 CD38 的髓鞘反应性调节性 T 细胞转入小鼠时,这些细胞虽然能到达 CNS,但无法像正常细胞那样控制疾病。在混合嵌合动物中,仅当驻留的调节性 T 细胞缺乏 CD38 时,移除具有 CD38 的那部分细胞就足以诱发复发,显示 CD38 以细胞内在(cell-intrinsic)的方式促进有效控制。
保护生命线信号
机制实验揭示了 CD38 如何赋予这种韧性。CNS 中高水平的 NAD+ 可为酶 ARTC2.2 催化的表面蛋白化学修饰提供底物。一个敏感的靶点是 IL-2 受体的高亲和亚基,调节性 T 细胞在识别脑抗原时尤其高表达该亚基。在暴露于 NAD+ 的 CD38 缺失调节性 T 细胞中,大多数 IL-2 受体被修饰,导致下游信使 STAT5 的激活减弱和对 IL-2 的反应性下降。相比之下,表达 CD38 的细胞能在局部降低周围的 NAD+,限制这种有害修饰并维持强烈的 IL-2 信号。在活体小鼠中,将 NAD+ 注入脑内通过该通路选择性地杀死了大多数调节性 T 细胞,而相对保留了常规 T 细胞,这强调了在缺乏该保护性酶时该利基的脆弱性。 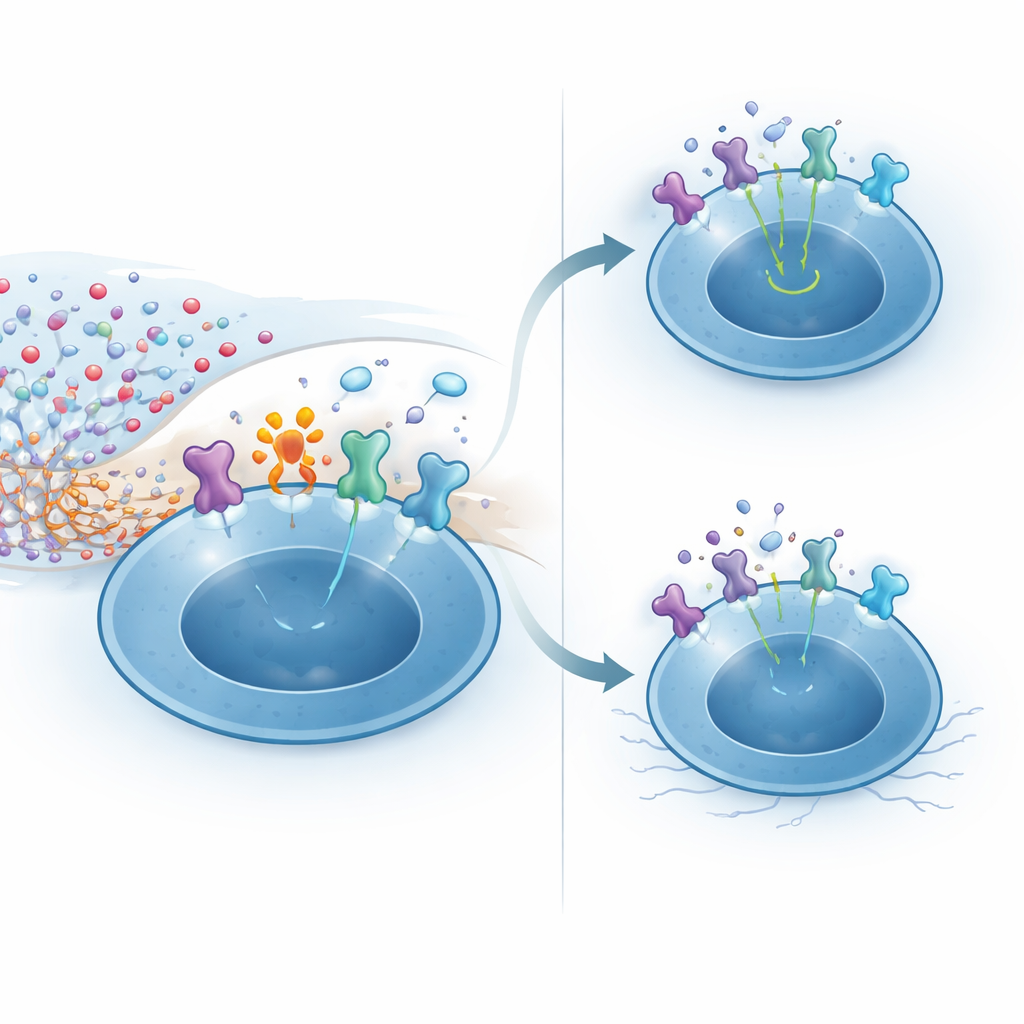
对慢性脑自身免疫的意义
这项工作描绘了慢性 CNS 自身免疫为一种分区化的战斗图景:少量残存的侵袭性 T 细胞栖息在脑和脊髓中,被同样专业化的局部调节性 T 细胞所制约。这些守护者之所以“耐受压力”,是因为 CD38 使它们能在高 NAD+ 水平下生存并持续感知微量 IL-2,从而保持其身份和抑制功能。对非专业读者而言,关键结论是:像多发性硬化这样的疾病的长期控制可能较少依赖循环免疫系统,而更多依赖于培育和保护这些驻留在脑内的维和细胞——可能通过针对能增强调节性 T 细胞 CD38 功能或 IL-2 敏感性的通路来实现。
引用: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
关键词: 调节性 T 细胞, 多发性硬化, 中枢神经系统炎症, CD38 酶, 免疫耐受