Clear Sky Science · zh
一个变构位点将激活、调节与抑制融为一体的 TRPM5
一个微小门控元如何塑造味觉与代谢
我们喜爱的食物以及身体处理糖分的方式,都依赖于细胞内那些微观的“门控”蛋白质。其中一个名为 TRPM5 的通道,既帮助我们感知甜、苦和鲜味,也参与胰腺释放胰岛素。本研究揭示了 TRPM5 上的一个小口袋如何充当主控旋钮——可开启通道、调节其敏感性,甚至将其关闭——这些见解可能为将来治疗糖尿病、肥胖和肠道疾病提供方向。
味觉与血糖调节的交汇通路
TRPM5 位于舌头的味细胞膜上、肠道的分泌激素细胞和胰腺分泌胰岛素的细胞中。当这些细胞内的钙浓度升高时,TRPM5 打开允许带正电的离子流动,短暂改变细胞膜电位。在味蕾中,这个电信号告诉大脑舌上有甜、苦或鲜味。在胰腺中,它有助于微调餐后胰岛素的脉冲释放。TRPM5 功能受损的动物和人会出现胰岛素分泌与血糖控制问题,这提示以 TRPM5 为靶点的药物或许能用于治疗代谢性疾病。然而直到最近,研究者仍缺乏精确的工具来开启或关闭该通道。
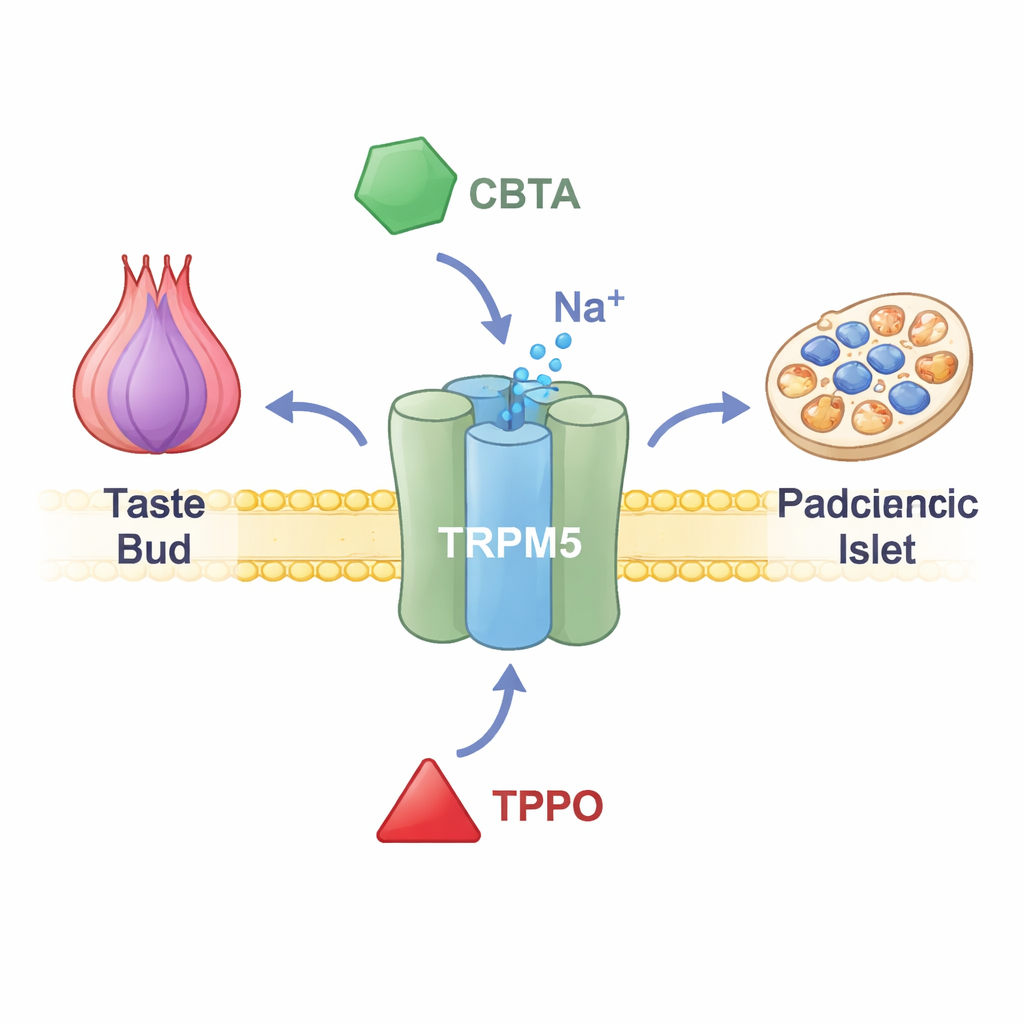
一种能极大激活通道的新化学钥匙
研究人员把注意力集中在一种合成化合物 CBTA 上,先前已知它能刺激 TRPM5,但机制不清。通过对表达 TRPM5 的细胞进行电学记录,他们展示了在几乎没有钙的情况下 CBTA 也能打开通道,证明它是真正的激活剂,而不仅仅是加强钙的作用。在存在微量钙——通常不足以激活 TRPM5 的水平时,CBTA 与钙协同作用,产生的电流远大于单独作用的效应。这表明 CBTA 显著提高了 TRPM5 的敏感性,使接近静息的钙水平足以将通道完全打开。
由冷冻电镜揭示的隐蔽控制口袋
为了解其原子层面的作用机制,团队使用冷冻电子显微镜获取了不同条件下 TRPM5 的三维快照。他们发现 CBTA 嵌入在通道一个电压感受区域上部先前未被注意到的空腔内,正位于钙通常结合位点之上。这个由一簇氨基酸形成的空腔充当精确的停靠位点。当科学家突变了构成该口袋的关键残基后,CBTA 无法再激活 TRPM5,尽管钙仍可作用,证实了这一小口袋对于该药物功能是必需的。值得注意的是,CBTA 结合会轻微重排蛋白附近区域,使得钙更容易占据其常见位置,从而解释了电学测量中观察到的显著协同效应。
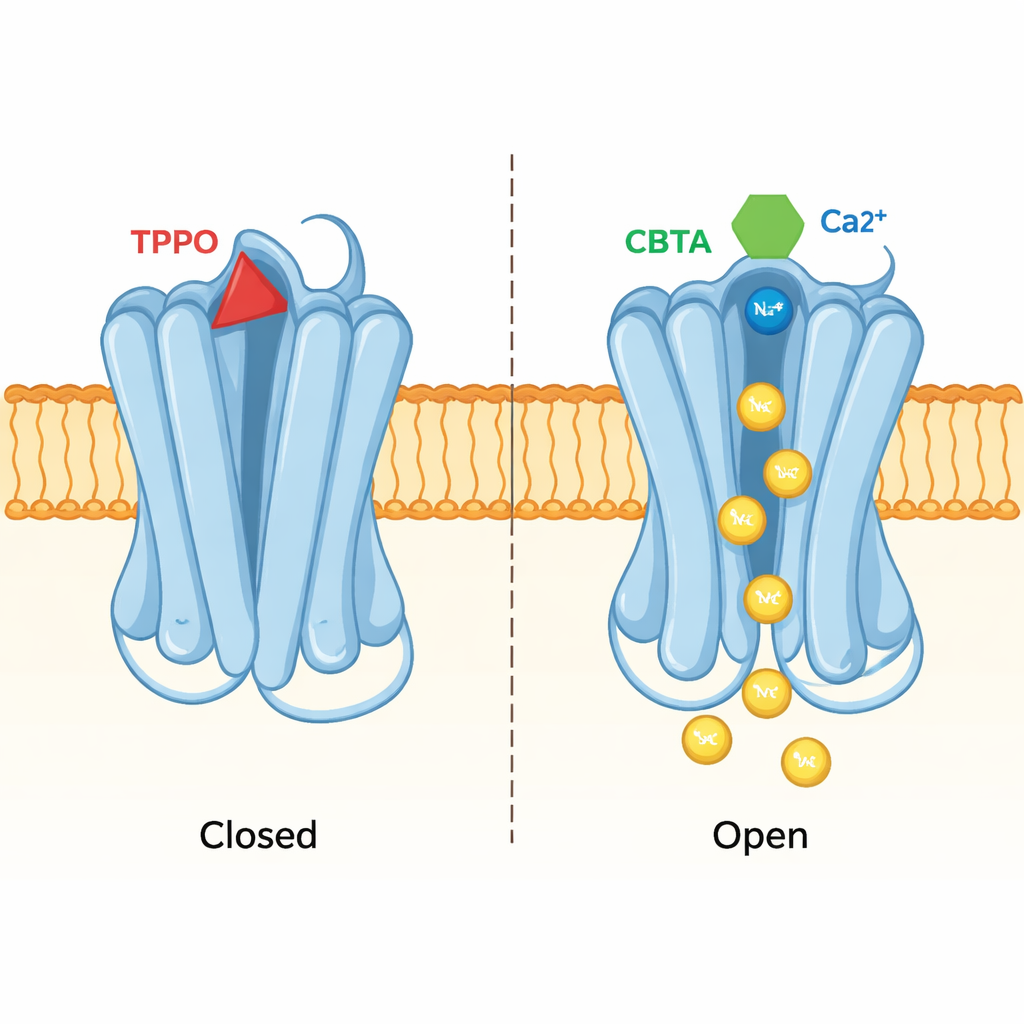
同一口袋导致两种相反结果
相同的结构学方法还揭示了抑制剂 TPPO 如何利用完全相同的口袋产生相反的效果。当 TPPO 结合时,TRPM5 上的钙位点仍被占据,但通道的中央孔保持收紧,离子无法通过。对比 TPPO 结合态与 CBTA 结合态的结构显示,它们不同的分子形状推动邻近蛋白片段朝相反方向运动。CBTA 促使的构象变化传播至孔道并打开它;而 TPPO 则破坏了该口袋与孔道之间的通信,保持闸门关闭。本质上,这个口袋可以充当加速器或刹车,取决于哪个分子停靠于此。
改写通道的内部连线
研究还表明,这个控制口袋可以接管通常由细胞内部另一个钙结合区域执行的任务。在那些使常规内部钙位点失能的突变通道中,单独的钙无法开启 TRPM5。然而 CBTA 仍能激活这些突变体,并重塑一个连接通道内外关键结构元件的构象。在另一类破坏钙结合与孔道开启之间连通性的突变体中,加入 CBTA 恢复了正常行为。这些结果表明,新识别的位点能改道或修复不同通道域间的通信,作为蛋白内部长程信号传递的灵活枢纽。
对未来药物开发的重要意义
对非专业读者而言,核心信息是:研究者发现了 TRPM5 上一个单一、对药物敏感的口袋,能够整合激活、精细调节与关闭。像 CBTA 这样的小分子激活剂既能模拟钙的作用,又能大幅提高通道敏感性,而另一个化合物 TPPO 可以通过同一停靠位点将通道钳制关闭。这一关于 TRPM5 调控的统一图景为设计能在特定组织中增强或抑制其活性的定制分子打开了大门,潜在应用涵盖改善味觉相关疗法、肠道动力药物以及开发管理血糖和代谢疾病的新策略。
引用: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
关键词: TRPM5 通道, 味觉感知, 胰岛素分泌, 离子通道门控, 变构调节