Clear Sky Science · zh
CDK4/6 抑制减缓化疗诱导的 TP53 突变克隆性造血扩增
为什么保护造血系统在癌症治疗中很重要
癌症化疗可能挽救生命,但它也会严重损伤产生新血细胞的骨髓。在一些人中,这种损害会无意中促使罕见的、事先存在的突变血液干细胞扩张,日后可能发展为侵袭性血癌。本研究提出了一个令人期待的问题:我们能否用一种短暂的“暂停键”药物使血液干细胞在化疗期间得到保护,从而减缓这些高风险突变克隆的扩张,同时不削弱对实体瘤的化疗效果?
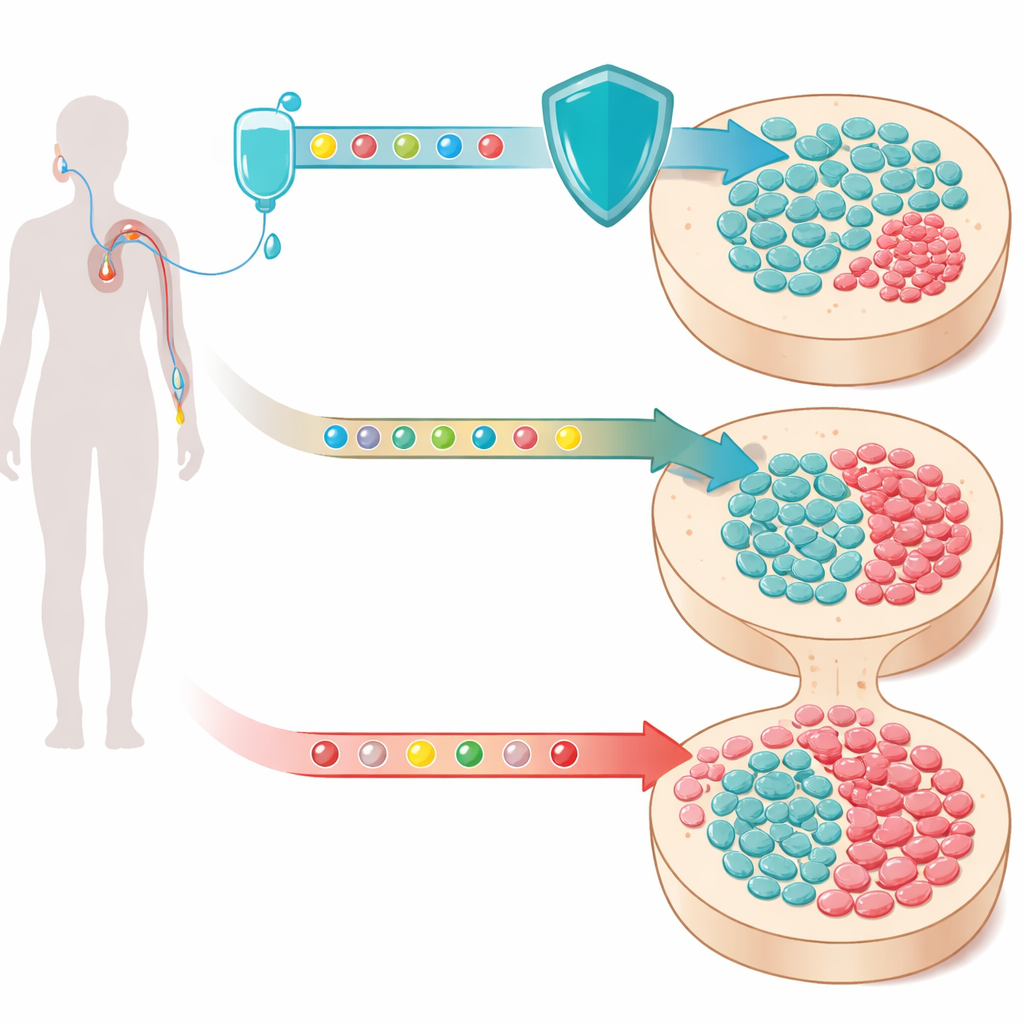
血液中隐藏的克隆
随着年龄增长,我们的造血干细胞会逐渐积累 DNA 变化。大多数发生改变的细胞保持无害,但有少数获得生长优势并开始形成小的克隆——一群基因组成相同的细胞——在血液中循环。这种现象称为克隆性造血,在老年人中出人意料地常见。当受影响的基因是 TP53 或其他 DNA 损伤反应基因时,这些克隆尤其令人担忧:它们能在常规细胞被应激杀死时存活,并与治疗相关的髓系肿瘤密切相关,这是一类通常致命的血癌,可能在化疗数年后出现。
在化疗期间按下干细胞的“暂停键”
研究者关注于阻断 CDK4/6 的药物,CDK4/6 是推动细胞分裂的关键引擎。其中一种药物三拉西利(trilaciclib)已获批用于在接受某些肺癌治疗的患者中减少血细胞减少。短暂在化疗前给予它,可以把骨髓中的干细胞和祖细胞推入静息状态。研究团队推测,如果在化疗来袭时健康和 TP53 突变的干细胞都不太活跃,突变细胞将失去其通常的生存优势,因为在 DNA 损伤性药物最致命的时刻,被“抓到”分裂的细胞——无论正常还是突变——都会更少。
来自临床试验和动物模型的证据
为了在真实患者中检验这一想法,团队分析了四项随机临床试验中的血液样本,这些试验对象为接受小细胞肺癌、转移性结直肠癌和三阴性乳腺癌化疗的患者。在每项试验中,患者被随机分配接受标准化疗并同时给予三拉西利或安慰剂。研究者在治疗开始时及多个疗程后对血细胞进行了超深度 DNA 测序,追踪已知突变克隆随时间的变化。在所有试验中,携带 DNA 损伤反应突变的克隆——尤其是 TP53 和 PPM1D 突变——在化疗期间扩增,但在接受三拉西利的患者中增长速度明显更慢。平均来看,这些高风险克隆的增长率大约减少了三分之一,而其他更常见的与年龄相关的基因突变基本不受影响。
放大看保护机制如何发挥作用
由于患者随访时间仍然相对较短,研究组转向小鼠模型以揭示 CDK4/6 阻断在治疗期间如何重塑骨髓。他们构建了血液系统中含有一小部分 Trp53 突变干细胞的小鼠,模拟人类的克隆性造血。当这些小鼠单独接受铂类化疗时,突变细胞在血液和骨髓中迅速胜过正常细胞。但当在每次化疗前短暂给予三拉西利或另一种 CDK4/6 抑制剂帕博昔利(palbociclib)时,这种突变占优势的现象几乎完全被阻断。详细的单细胞 RNA 测序显示,CDK4/6 抑制使干细胞和祖细胞进入更安静、增殖性更低的状态,降低了一种有利于长期存在的突变细胞的“干性”基因程序,使细胞分化更偏向淋巴系而非髓系,并选择性地在 Trp53 突变干细胞中触发细胞死亡路径,同时保留正常细胞。
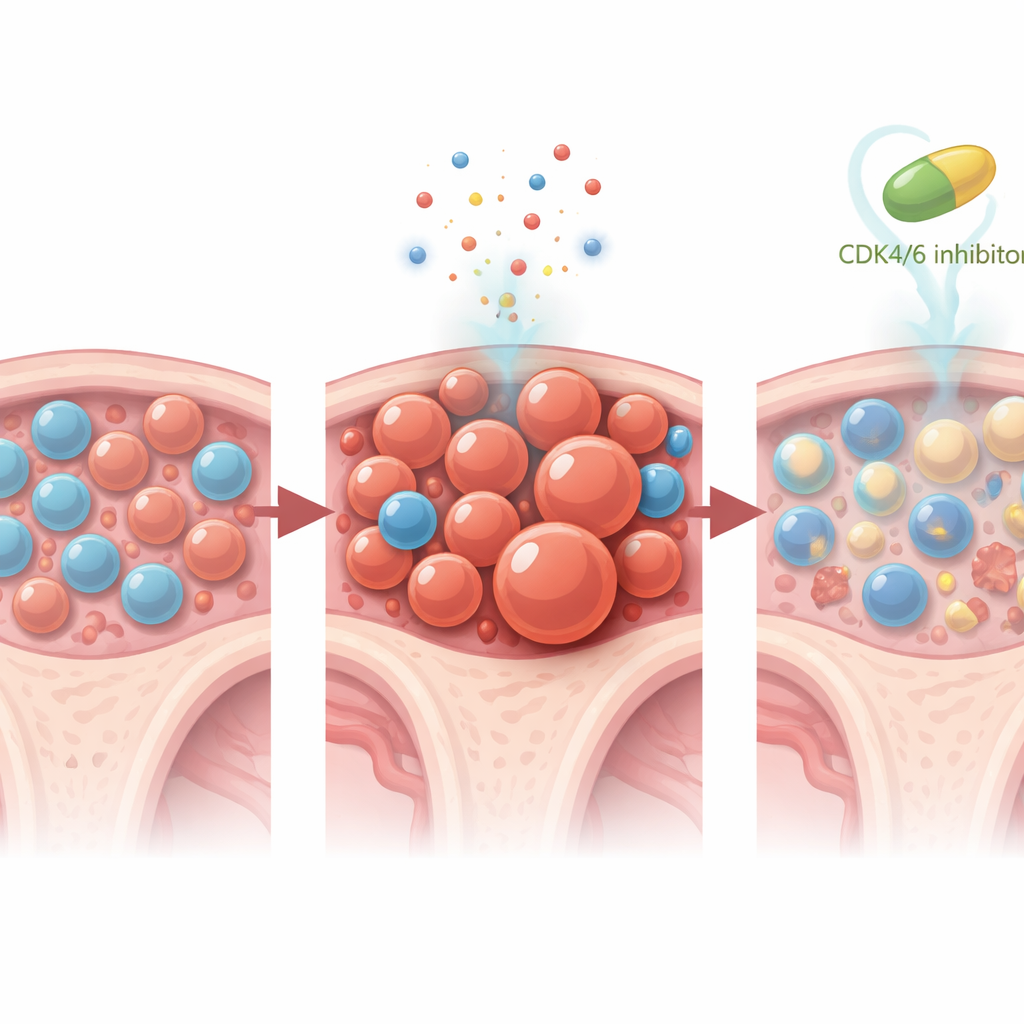
持久影响与未来方向
一项引人注目的小鼠实验表明,即使短期使用 CDK4/6 抑制也能产生持久效果:在化疗前后给药两周的三拉西利阻止了 Trp53 突变克隆的扩张,至少在所有治疗停止后六周内仍然有效。重要的是,血象和整体骨髓健康保持在可接受范围内,表明该保护策略并非以引入另一种毒性为代价。尽管在这些试验随访期间没有患者发展为血癌,但极小的 TP53 突变克隆的存在及其生长放缓支持了这样一种观点:这是通向治疗相关白血病的早期、可干预的一步。
这对癌症患者可能意味着什么
对于已经携带高风险血细胞克隆的患者来说,长期的担忧是,为控制实体瘤所需的化疗可能同时为未来往往难以治疗的白血病埋下种子。这项工作提供了一个概念验证:精心时机安排的 CDK4/6 抑制剂可以通过在化疗期间短暂保护骨髓,削弱那些危险克隆的生长优势。虽然需要更长期、更大规模的临床研究来证明该策略确实能降低治疗相关血癌的发生率,但它指向了一个前景:我们既能积极治疗原发癌症,同时也能保护造血系统免受长期的基因损害。
引用: Chan, I.C.C., Zhang, P., Pan, X. et al. CDK4/6 inhibition mitigates chemotherapy-induced expansion of TP53-mutant clonal hematopoiesis. Nat Genet 58, 582–592 (2026). https://doi.org/10.1038/s41588-026-02526-w
关键词: 克隆性造血, TP53 突变, 化疗副作用, CDK4/6 抑制剂, 治疗相关白血病