Clear Sky Science · zh
全基因组关联分析显示自身免疫性甲状腺功能减退症的自身免疫与甲状腺特异性影响以及与癌症风险的反向关系
这对日常健康为何重要
许多人经常感到疲倦、怕冷或思维迟钝,却没有意识到甲状腺可能是罪魁祸首。自身免疫性甲状腺功能减退是指机体自身防御系统逐渐攻击甲状腺,影响超过二十分之一的人群。本研究使用数十万志愿者的遗传数据,探讨两个重要问题:哪些遗传变异会增加这种病症的发生概率?这些相同的变异又如何与癌症发生风险相关?结果揭示了一个意想不到的取舍:免疫系统有时损害甲状腺,但同时也能在一定程度上保护机体免受肿瘤侵袭。
全基因组范围的观察
研究者将来自两个大型群体项目(芬兰的 FinnGen 和英国的 UK Biobank)的健康记录与遗传信息相结合。他们聚焦于需要长期甲状腺激素替代治疗的人群,并谨慎排除因手术、癌症或其他非自身免疫原因导致的甲状腺问题。这样筛选得到超过81,000例自身免疫性甲状腺功能减退病例和超过700,000名对照,使其成为迄今为止该病最大的研究。对全基因组数百万个DNA标记进行扫描后,研究发现了418个独立的遗传信号(位于主要免疫基因簇之外),分布在至少280个基因组区域。许多信号涉及罕见或低频的蛋白结构改变,提供了指向潜在生物学机制的直接线索。
将广泛免疫效应与甲状腺特异性效应区分开来
自身免疫性甲状腺功能减退位于一般自身免疫与甲状腺独特生物学的交汇处。为将这些成分分离,研究团队将结果与其他自身免疫疾病的遗传研究以及血液中促甲状腺激素(检测甲状腺功能减退的关键临床指标)水平进行了比较。研究使用贝叶斯分类方法,将遗传信号分为与广泛自身免疫疾病共有的信号和更特异于甲状腺激素调节的信号。估计约38%的信号通过影响多种自身免疫病的通用免疫通路发挥作用,而约20%的信号主要通过甲状腺功能本身发挥作用。与甲状腺相关的变体倾向于影响激素水平和在甲状腺组织中活跃的基因,而通用免疫变体在T细胞——协调免疫反应的白细胞中更为活跃。
聚焦一个关键的免疫开关
一个特别引人注目的发现涉及基因 ZAP70 中的一个罕见DNA变异,该基因编码T细胞内的关键信号传导蛋白。该蛋白的严重缺陷已知会导致深度免疫缺陷,但这里鉴定的变异仅导致部分功能丧失。在工程化T细胞的实验中显示,这种改变的ZAP70削弱了但并未完全阻断在识别目标后通常发生的信号级联。携带该变异的细胞较难开启激活标志物和下游信号步骤。该减弱的反应似乎扰乱了通常用于清除自反应性T细胞的微妙平衡,从而使携带者更易患自身免疫性疾病,同时也略微增加某些免疫缺陷的风险。
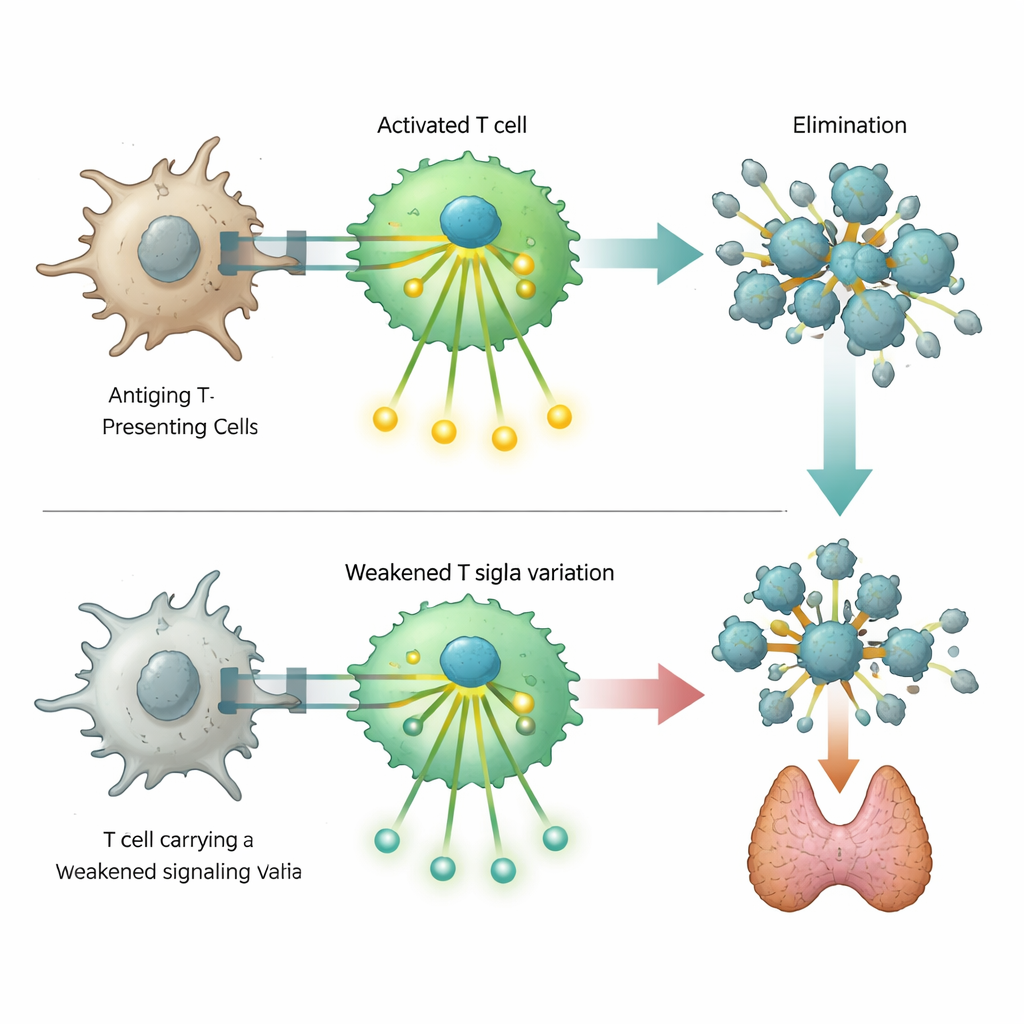
与癌症保护的意外联系
由于驱动自身免疫的相同免疫通路也可能攻击肿瘤,作者接着探问自身免疫性甲状腺功能减退的遗传学如何与癌症风险相关。他们计算了一个多基因风险评分,汇总每个人遗传上倾向于甲状腺功能减退的程度,并在芬兰数据中测试该评分与多种疾病的关联。正如预期,较高的评分与多种自身免疫疾病的风险升高相关。但更令人惊讶的是,若干癌症的风险呈一致降低的模式,尤其是基底细胞癌和其他皮肤癌,还有乳腺癌、前列腺癌以及整体的“所有癌症”分组。当团队直接检查癌症的全基因组扫描时,约10%的与甲状腺功能减退相关位点也影响皮肤癌,且通常相同的遗传变体一方面增加甲状腺自身免疫性,另一方面降低皮肤癌风险。这些共有变体集中在与免疫相关的基因中,包括免疫检查点免疫疗法的已知药物靶点。
对患者与医学实践的意义
从非专业的角度看,这项工作表明有些人生来免疫系统“偏热”一些,使他们更容易发生对甲状腺的缓慢、常常无声的损害,但同时更善于识别并消灭新生肿瘤。研究解析了哪些遗传改变通过普遍的免疫过度活跃发挥作用,哪些特异性影响甲状腺激素的产生,从而解释了像桥本氏病和格雷夫斯病这样的疾病为何可以共享某些风险基因却对甲状腺功能产生相反影响。研究也有助于解释为何在接受促免疫的抗癌药物治疗时出现甲状腺问题的患者通常对这些治疗反应更好。总体而言,研究结果表明免疫检查点和信号传导基因的常见自然变异共同塑造了自身免疫性甲状腺疾病与终生癌症风险,提供了预防和更个体化使用免疫疗法的新线索。
引用: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
关键词: 自身免疫性甲状腺功能减退, 甲状腺疾病, 遗传风险, 免疫系统, 癌症保护