Clear Sky Science · zh
HUNT 研究识别出可重复与人类肠道微生物组成相关的宿主遗传因子
为什么你的基因和肠道细菌很重要
我们每个人肠道中携带着数万亿微生物,帮助消化食物、训练免疫系统,甚至可能影响疾病风险。本研究提出了一个看似简单的问题:这套内部生态系统有多少是写在我们的 DNA 里的?通过扫描数万人的基因组并将其与详尽的肠道微生物组成进行比较,研究者展示了特定人类基因会持续性地将肠道微生物推向某些方向——而这些变化又与乳糜泻、痔疮和心血管相关问题等疾病以及体重有关联。
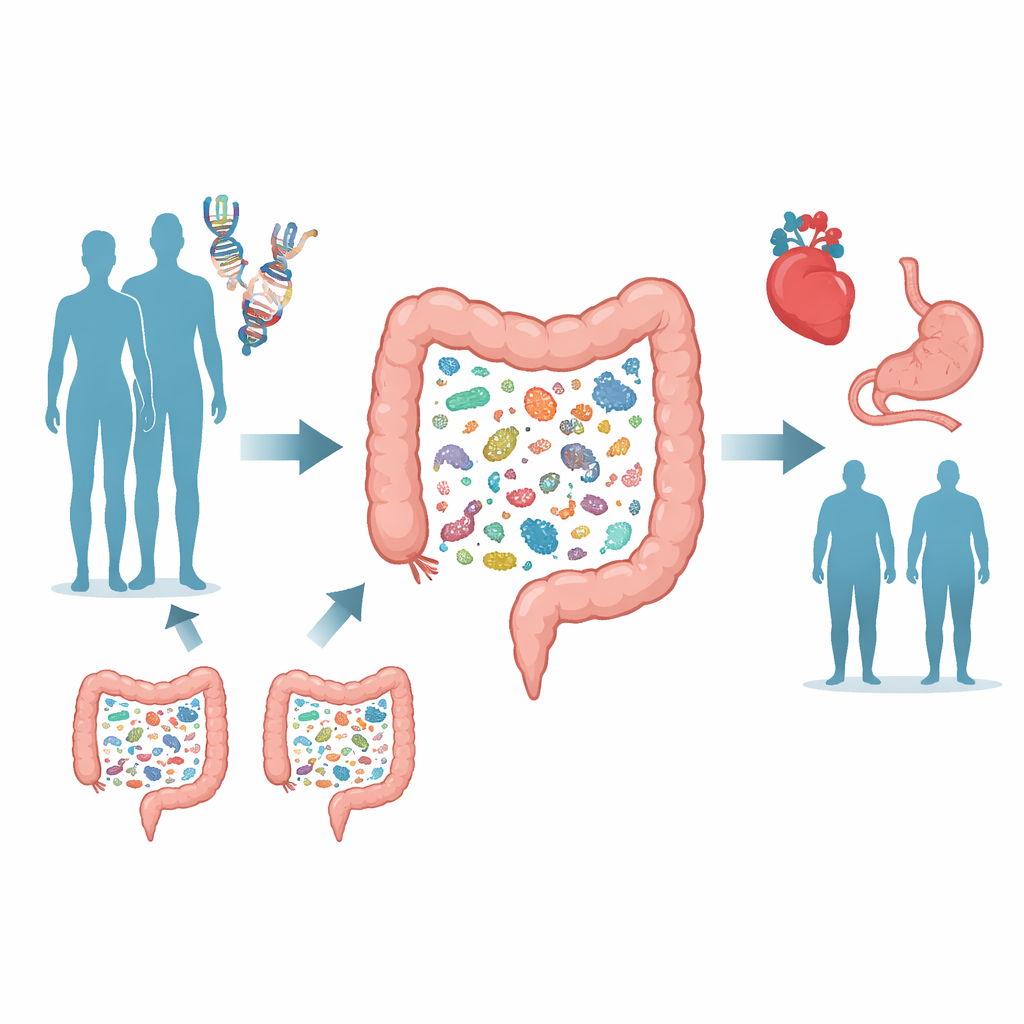
在人群中寻找模式
为追踪基因—微生物的联系,团队利用挪威特伦德拉格健康研究(Trøndelag Health Study),该研究中超过 1.2 万名成年人同时提供了用于 DNA 分析的血样和用于微生物谱分析的粪便样本。与早期采用较为粗略细菌指纹的方法不同,本研究依赖深度宏基因组测序,读取每个样本中大量 DNA,能够区分数百种不同细菌物种及其代谢功能。随后科学家们进行了全基因组关联研究,扫描近 800 万个人人类遗传变异,观察哪些变异与 546 种常见肠道物种的相对丰度差异以及整体微生物多样性指标相一致。
塑造肠道的六个遗传热点
分析显示出令人意外的强烈遗传印迹。研究中发现了 12 个稳健关联,连接了人类 DNA 变异与特定细菌物种,这些关联集中在基因组的六个区域。其中两个区域——位于参与乳糖消化的 LCT 基因附近和 ABO 血型基因附近——此前已有研究提示相关,但另外四个区域(靠近 HLA-DQB1、MUC12、SLC37A2 和 FUT2)则是新发现或新确认。例如,携带持续表达乳糖酶(lactase-persistent)版本 LCT 的人倾向于携带更少的 Bifidobacterium adolescentis,这种细菌利用未完全分解乳糖在肠道中残留的乳糖为食。FUT2 区域影响血型相关糖类是否在肠道黏膜上展示,该区域与若干似乎以这些带糖表面的细菌相关联。
从微生物到疾病风险
当研究者将这些遗传结果与大型人类疾病数据库叠加时,故事变得更耐人寻味。与较高 Agathobacter 物种水平相关的 HLA-DQB1 区域变异也与较低的自身免疫性疾病风险相关,包括乳糜泻。在挪威队列中,患有乳糜泻的人往往该微生物水平特别低,提示疾病本身可能部分重塑肠道群落。另一个靠近 MUC12 基因的区域既与一种名为 Coprobacillus cateniformis 的细菌丰度相关,也与痔疮风险降低相关。实验室研究显示 MUC12 在结肠上皮细胞中高表达,这提示黏液屏障的细微变化可能影响哪些细菌繁盛,进而影响直肠中细小血管和组织的状况。
微生物功能、心脏健康与体重
除了个别物种外,团队还通过将微生物基因归入功能模块(例如转运系统和调控回路)来检视微生物的功能能力。相同的人类遗传区域——LCT、ABO 和 FUT2——也影响这些微生物功能,表明我们的 DNA 不仅决定肠道里有哪些生物,还决定它们在做什么。例如在 FUT2 位点,与“非分泌者(non‑secretor)”状态相关的变异与一些与潜在有害代谢产物相关的细菌以及较高胆固醇和高血压风险并行出现。最后,利用一种称为孟德尔随机化的方法(将基因变异作为自然实验),研究者提供证据表明更高的体质指数(BMI)在因果上会改变微生物组:遗传上倾向于更高体重的人往往总体微生物多样性更低,并在许多物种上表现出一致的变化。
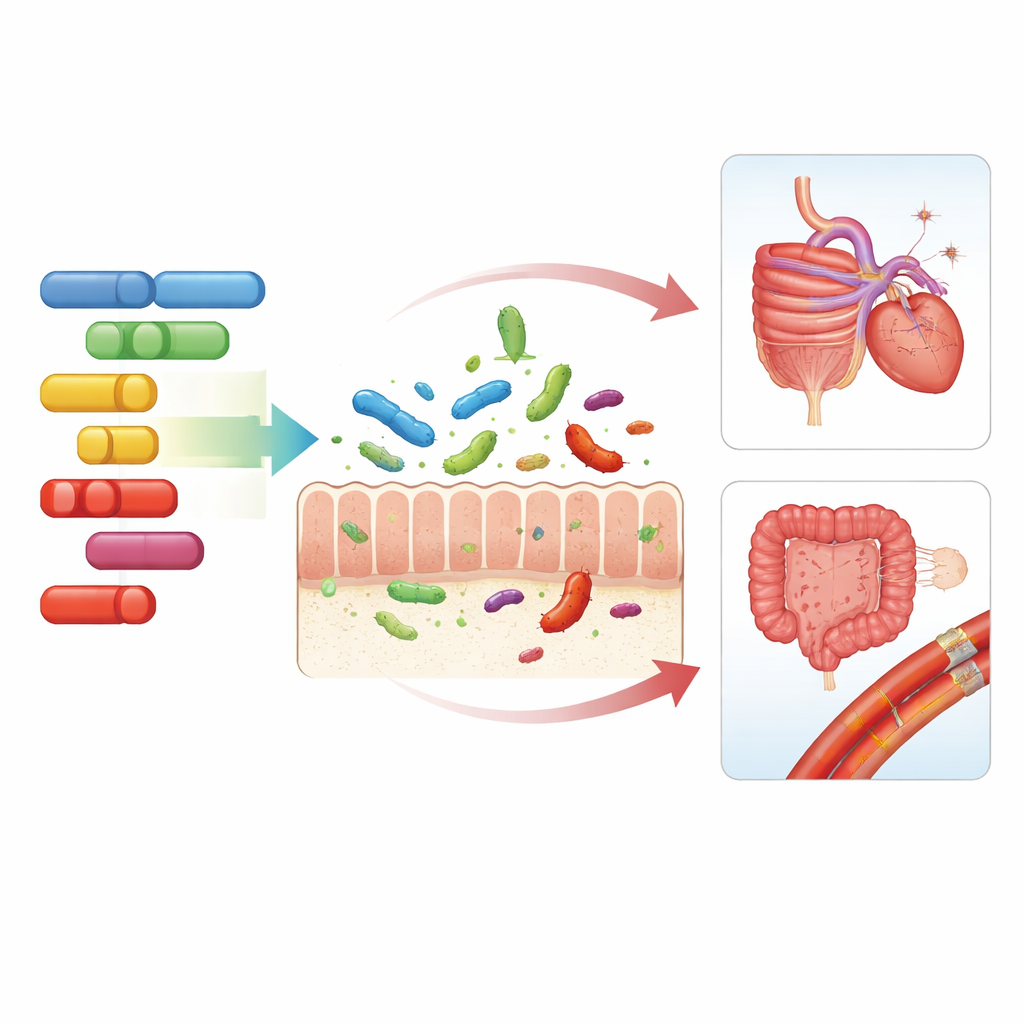
对日常健康意味着什么
综观这些发现,描绘出一幅关于我们基因、肠道微生物与健康之间三方对话的图景。某些人类 DNA 区段会微妙地偏好或抑制特定细菌居民及其微生物活性,进而与消化疾病、心血管问题以及超重带来的影响发生交汇。尽管这些遗传影响只解释了肠道群落巨大变异的一小部分——且尚不能直接转化为临床检测——它们有助于阐明为什么不同人在相同饮食或环境下反应不同,并指向将基因组与微生物组共同纳入考虑的更个性化营养和疾病预防策略。
引用: Moksnes, M.R., Coward, E., Nethander, M. et al. The HUNT study identifies host genetic factors reproducibly associated with human gut microbiota composition. Nat Genet 58, 530–539 (2026). https://doi.org/10.1038/s41588-026-02502-4
关键词: 肠道微生物组, 人类遗传学, 微生物群与疾病, 体重与微生物, 全基因组关联