Clear Sky Science · zh
与肝素硫酸复合的糖RNA调节VEGF-A信号传导
细胞如何微调体内的血管信号
血管并非在任何出现生长信号的地方随意生成——它们必须被精确控制,以在滋养组织的同时不助长肿瘤或导致失明。本文揭示了对一种主要促血管生长信号VEGF-A的意外“刹车”。作者表明,装饰在细胞外侧、与糖和蛋白质协作的小片段RNA可以降低VEGF-A的讯号,这改变了我们对细胞表面语言的认识。
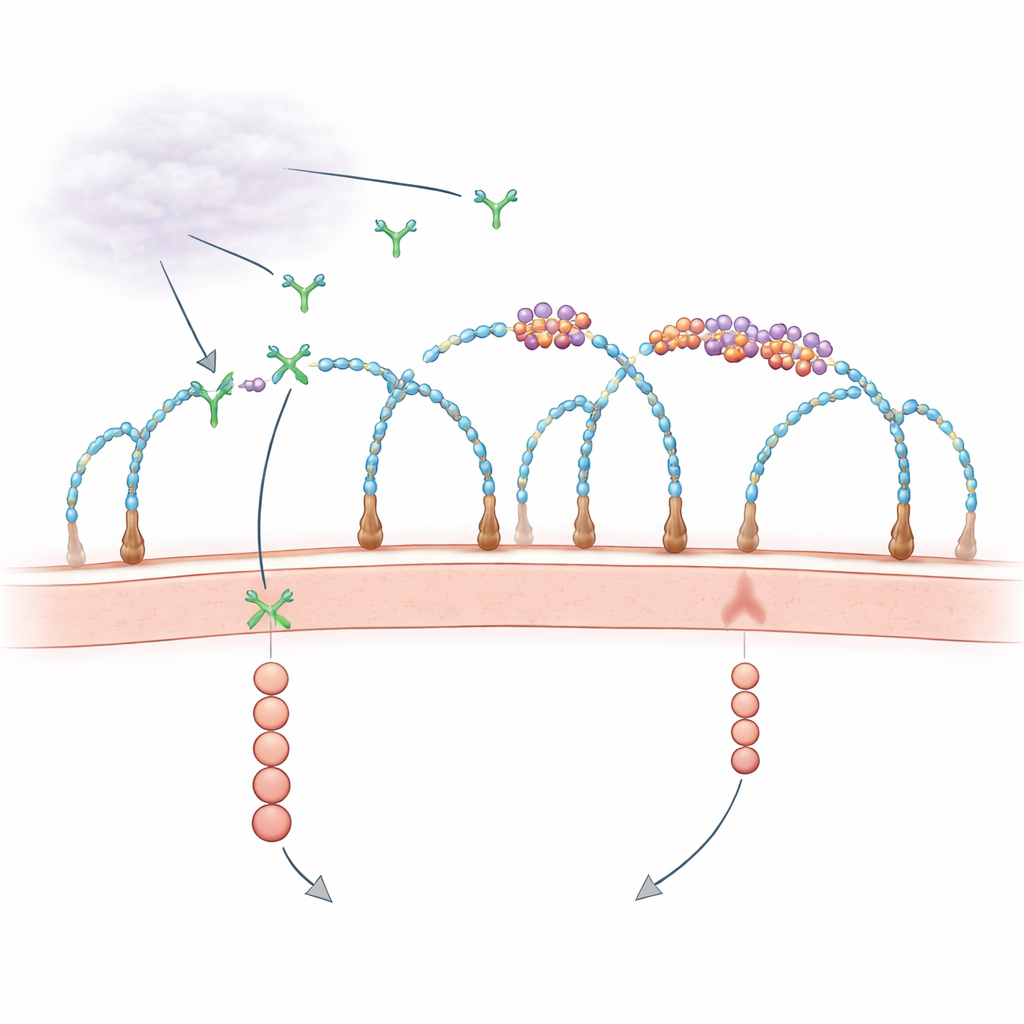
细胞表面RNA的意外角色
几十年来,生物学家已知细胞外层含丰富糖修饰蛋白——肝素硫酸蛋白多糖,能捕获生长因子并将其呈递给受体。与此同时,零散观察提示细胞外的RNA片段可能影响血管生长,但相关分子和机制尚不清楚。近期研究发现一些小RNA通过化学键与复杂糖链结合形成“糖RNA”,并且某些RNA结合蛋白也会出现在细胞表面,与这些RNA聚集在一起。本研究提出了一个明确问题:这些位于膜上的微小RNA–蛋白岛是否真正控制像VEGF-A这样的生长信号如何被接收?
用糖链构建聚集的RNA–蛋白岛
研究者通过全基因组CRISPR敲除筛选与高分辨率显微镜发现,特定的糖链——带有特定硫酸化修饰的肝素硫酸——是组装这些RNA–蛋白簇的必要支架,他们称之为细胞表面核糖核蛋白复合体(csRNPs)。当负责合成或对肝素硫酸进行硫酸化的关键酶被去除时,尽管细胞内的RNA和蛋白仍然存在,细胞表面的糖RNA及其配对蛋白簇却消失了。切除表面肝素硫酸链或化学阻断硫酸化的酶也产生相同效果。这些结果表明,完整且正确硫酸化的肝素硫酸链将csRNPs组织成膜上的纳米尺度岛状结构。
RNA簇作为强效促血管信号的刹车
团队随后转向对VEGF-A有响应的血管内皮细胞进行研究。他们发现这些细胞也展示出由肝素硫酸锚定的csRNP簇。用降解RNA的酶(RNase)处理活细胞可以去除RNA成分而不破坏底层糖链。在这些条件下,VEGF-A最常见的可结合肝素的形式(VEGF-A165)引发下游ERK信号通路的激活显著增强,而缺失肝素结合尾部的短形式(VEGF-A121)则不受影响。去除表面RNA后,更多VEGF-A165分子结合于细胞表面,但受体水平保持不变。在三维微流控装置中,暴露于RNase的内皮细胞在胶原凝胶中生长得更深入并更强烈地形成管状结构,表明破坏表面RNA会释放促血管生成行为。
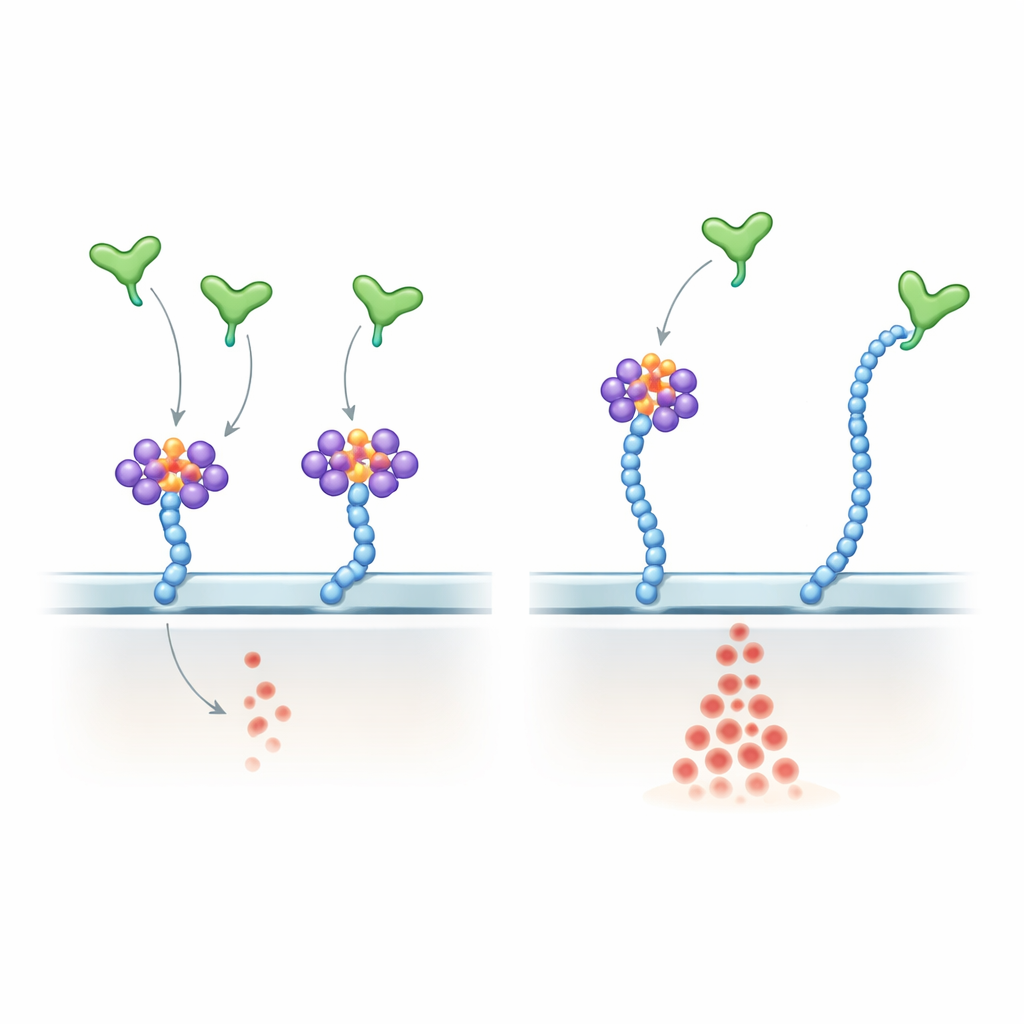
解析VEGF-A如何识别RNA与糖
为探究机制,作者表明VEGF-A165通过其带正电的C端区域直接结合特定的小RNA,包括许多已知的糖RNA——该区域正是结合肝素硫酸的部位。他们设计了一个微妙的VEGF-A165变体,将该尾部中的关键精氨酸残基替换为赖氨酸。该突变体保留了整体正电荷并仍能抓取肝素硫酸链,但对糖RNA的结合能力较差,并且在很大程度上对RNase处理不敏感。在内皮细胞中,该突变体比正常的VEGF-A165诱导更强且更耐RNase的ERK激活,几乎复制了去除细胞表面RNA的效果。在活体小鼠中,将该突变体注入眼内比注入正常蛋白导致更为旺盛的视网膜血管生长。在斑马鱼胚胎中,过表达该Vegfa突变体扰乱了正常的血管模式并增加了内皮细胞数量。
从基本机制到更广泛的影响
最后,作者展示将VEGF-A的肝素结合尾部融合到无关的信号蛋白Wnt3a上可以重新定向Wnt活性:连接正常尾部会减弱Wnt驱动的发展学变化,而连接对RNA不敏感的尾部则增强这些变化。综合这些实验,支持这样一个模型:由特定硫酸化肝素硫酸锚定的csRNP簇结合VEGF-A及相关因子以缓和其活性。当RNA成分被移除或生长因子失去感知RNA的能力时,信号强度倾向增强,并在多种物种中改变血管发育。
此发现对健康与未来疗法的意义
对非专业读者而言,关键结论是细胞不仅使用蛋白质和糖,还利用展示在表面的短RNA来微调像VEGF-A这样强大的生长信号。这些糖锚定的RNA–蛋白簇充当血管形成的可调节刹车,帮助确保新血管在适当的时间和地点萌发。破坏这种平衡——通过降解表面RNA或改变生长因子对RNA的结合特性——可能会夸大或误导血管生长。理解这一新揭示的调控层或可开辟途径,通过靶向表面RNA、其糖支架或生长因子的RNA感知区域,更精确地调节癌症、眼病、伤口愈合与再生医学中的血管生成。
引用: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
关键词: 血管生成, 血管内皮生长因子, 肝素硫酸, 细胞表面RNA, 糖RNA