Clear Sky Science · zh
在人体干细胞自闭症模型中观察到的发育趋同与背离
这项研究对家庭与社会的重要性
自闭症谱系障碍以其复杂性著称:数以百计的不同基因与风险增加有关,但许多自闭症人士在交流、社交与行为方面表现出相似的挑战。本研究提出了一个看似简单但影响深远的问题:当不同的基因改变都增加自闭症的概率时,它们最终是否以相似的方式干扰正在发育的人脑?研究人员使用由患者自身细胞构建的微小体外人类大脑皮质模型,追踪早期基因活性失调如何汇入共同通路,从而改变脑细胞的产生、成熟与连接方式。
在实验室中培养微型人类脑组织
为了解答这个问题,研究团队收集了55名个体的皮肤或血液细胞:其中一些人携带与自闭症高度相关的已知罕见突变,另一些为无已知主要突变的自闭症患者,还有对照组无影响者。将这些细胞重编程为诱导多能干细胞(iPSC),这种细胞几乎能分化为任何细胞类型。随后科学家引导其形成三维“皮质类器官”——模拟人类大脑皮质早期发育的微小组织团块。在超过100天的培养过程中,这些类器官从以干细胞样前体为主发展到富含幼年神经元的网络。在这一时间线上四个节点(第25、50、75和100天),团队测量了数百个类器官中哪些基因被开启或关闭,绘制出早期脑发育期间分子变化的详尽影像。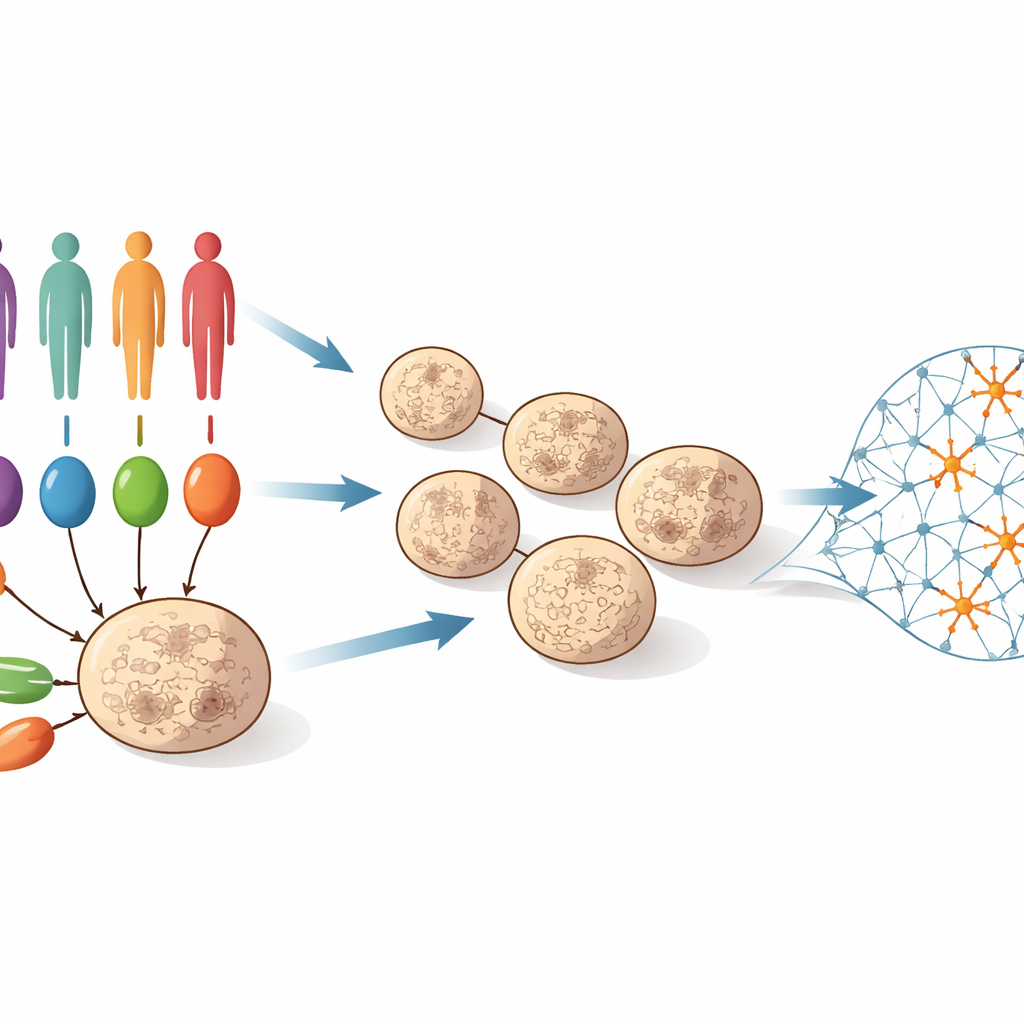
多条遗传路径、共享的早期偏差
尽管与自闭症相关的突变各不相同——包括大型缺失或重复的DNA片段以及特定基因变异——携带相同突变的类器官表现出高度可重复的基因活动模式。在发育早期,尤其在第25天左右,每种突变产生其独特的强烈特征:与对照相比,有数百到上千个基因出现调控异常。然而即便在这一早期阶段,若干突变也改变了彼此重叠的基因集,这些基因参与细胞内DNA的包装与读取。这些共享变化影响了已知的高风险自闭症基因和其他神经发育障碍相关基因,表明不同突变在脑形成的非常早期就开始扰动类似的细胞机制。
随着脑模型成熟出现的趋同
随着类器官向更成熟的神经元发展(到第75天和100天),情况发生了变化。突变特异的差异变得不那么显著,而相似性增强。在几乎所有研究的不同遗传形式的自闭症中,研究人员观察到对突触电信号相关基因的活性降低——突触是神经元之间的通讯点——同时细胞生长和蛋白质合成相关基因的活性上升。不同细胞类型的比例与成熟阶段出现细微变化,指向神经元产生与成熟时序的改变,而非某类细胞的大规模丧失。在最晚的时间点,数千个基因在多种罕见突变间表现出共同的失调模式,尽管这些突变本身影响的是不同的原始基因。
连接众多自闭症基因的中央调控枢纽
进一步挖掘时,研究团队使用网络分析将倾向于一起开关的基因分组为“模块”。其中一个模块,称为M5,格外突出。该模块的基因在发育早期最为活跃,富含自闭症风险基因,尤其是那些控制其他基因如何被开启或关闭以及DNA如何被包装的基因。在来自若干自闭症突变组的类器官中,这一模块持续地被下调。研究人员表明,M5中许多蛋白质存在物理相互作用,形成一个调控枢纽。利用CRISPR为基础的工具在人体神经前体细胞中选择性地抑制了26个M5调控因子后,他们证实该枢纽直接控制着大量下游基因,包括许多额外的自闭症和神经发育风险基因,并且其扰动会改变参与神经元形成和突触功能的通路。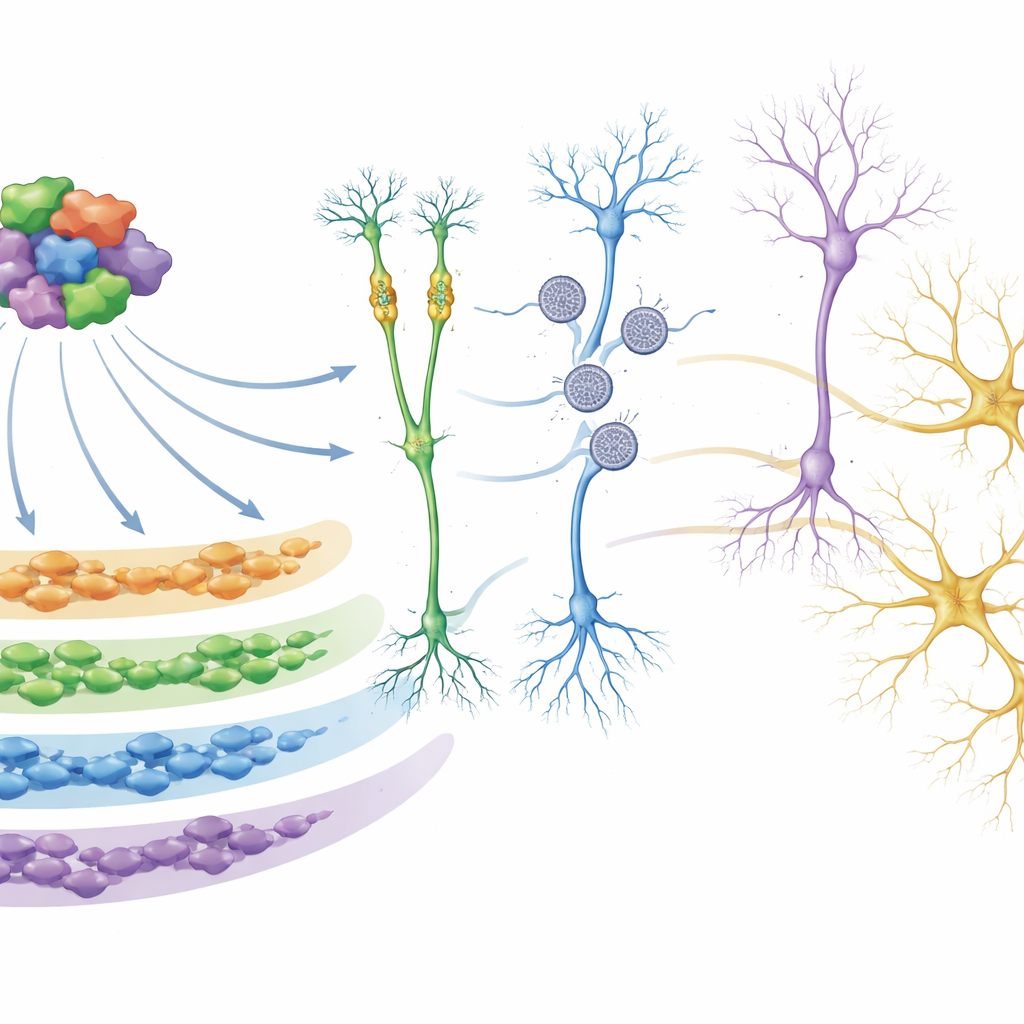
这对理解自闭症意味着什么
这项研究提出了一个统一的图景:罕见但影响力强的自闭症相关突变最初扰动基因组的不同部分,但其效应会通过一个共享的早期控制网络向前传导,该网络管理皮质神经元如何被生成与连线。随着时间推移,这些波及效应在共同的结果上趋同——神经元成熟延迟或改变以及突触程序被扰乱——即便最初的遗传原因不同。对家庭来说,这意味着在DNA层面上截然不同的诊断仍可能在发育中的大脑中影响重叠的生物学通路。对研究人员与临床医生而言,被识别的调控网络提供了一组聚焦的分子靶点,供未来旨在恢复更典型大脑发育模式的疗法在多种与自闭症相关的遗传状况中使用。
引用: Gordon, A., Yoon, SJ., Bicks, L.K. et al. Developmental convergence and divergence in human stem cell models of autism. Nature 651, 707–719 (2026). https://doi.org/10.1038/s41586-025-10047-5
关键词: 自闭症谱系障碍, 大脑类器官, 干细胞模型, 基因调控, 神经发育