Clear Sky Science · zh
个性化 mRNA 疫苗在辅助治疗三阴性乳腺癌中激发持久的 T 细胞免疫
乳腺癌治疗后的新希望
对于许多患有一种称为三阴性乳腺癌的侵袭性乳腺癌的女性来说,化疗和手术结束并不意味着恐惧消失。这类癌症有较高的复发和转移风险,往往在数年内发生。这里描述的研究检验了一种高度个性化的疫苗——基于每位患者自身肿瘤的突变构建——以评估它是否能训练免疫系统在多年内守护并降低标准治疗结束后复发的可能性。
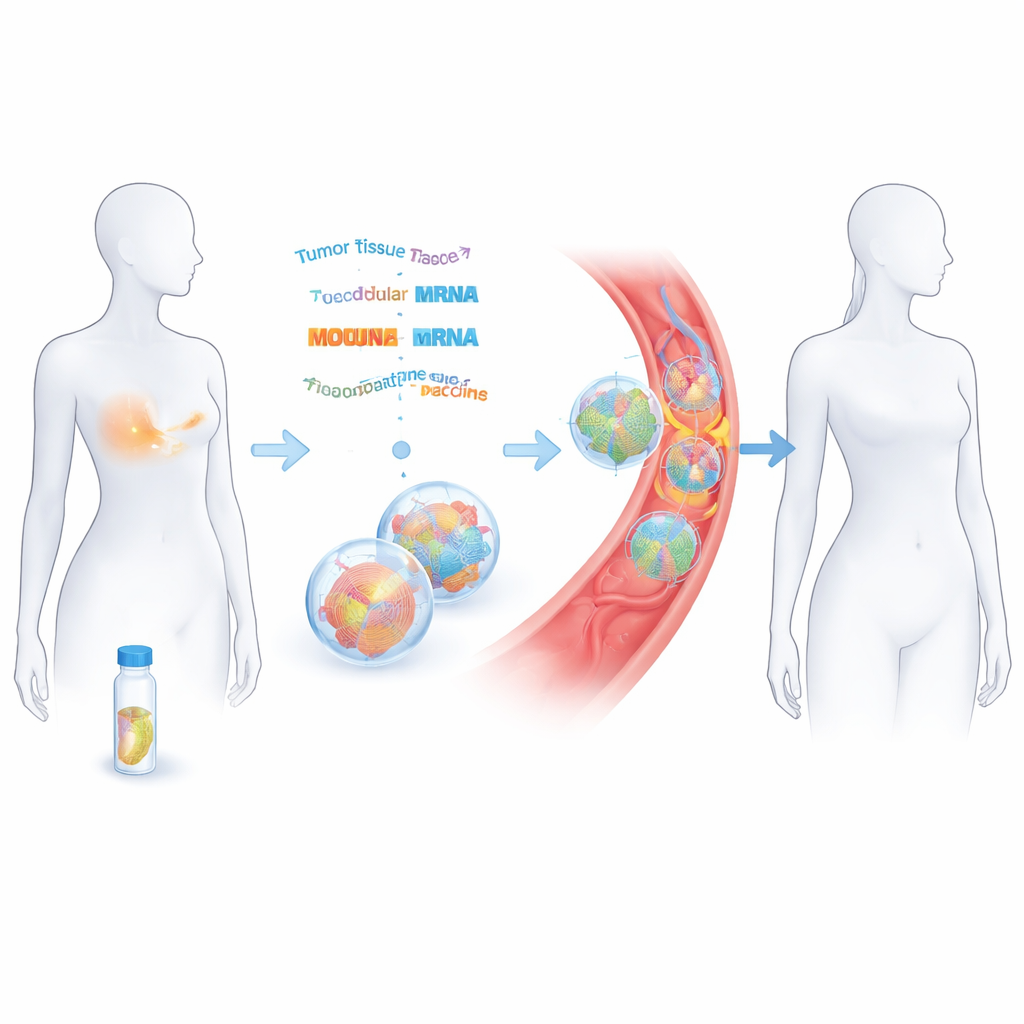
将切除的肿瘤变成定制疫苗
研究人员招募了 14 名已接受手术和意图治愈性化疗的早期三阴性乳腺癌女性。从切除的肿瘤组织中读取 DNA 和 RNA,记录肿瘤特有的突变。借助计算工具,他们预测哪些变异可能被免疫细胞识别为外来物。最多挑选 20 个这样的“新抗原”并将其拼接编码到两条信使 RNA(mRNA)链中,原理类似于新冠疫苗但针对每位患者量身定制。这些 mRNA 链被封装在微小脂质囊中,通过静脉注射在大约两个月内分八次给药。
疫苗如何唤醒免疫防御者
进入体内后,mRNA 指示称为树突状细胞的免疫哨兵短暂合成新抗原蛋白并在其表面展示其片段。这就像给 T 细胞张贴通缉令,T 细胞是免疫系统主要的杀癌力量。研究团队在接种前及随后多个时间点采血,以检测是否出现了新抗原特异性的 T 细胞以及其强度。使用灵敏的体外检测,他们发现每位患者都对至少一种所选突变产生了新出现或增强的 T 细胞反应,大多数患者对多种突变有应答。在许多情况下,循环 T 细胞中识别肿瘤特异性靶点的比例较大——这一水平通常仅在强效细胞疗法中见到。
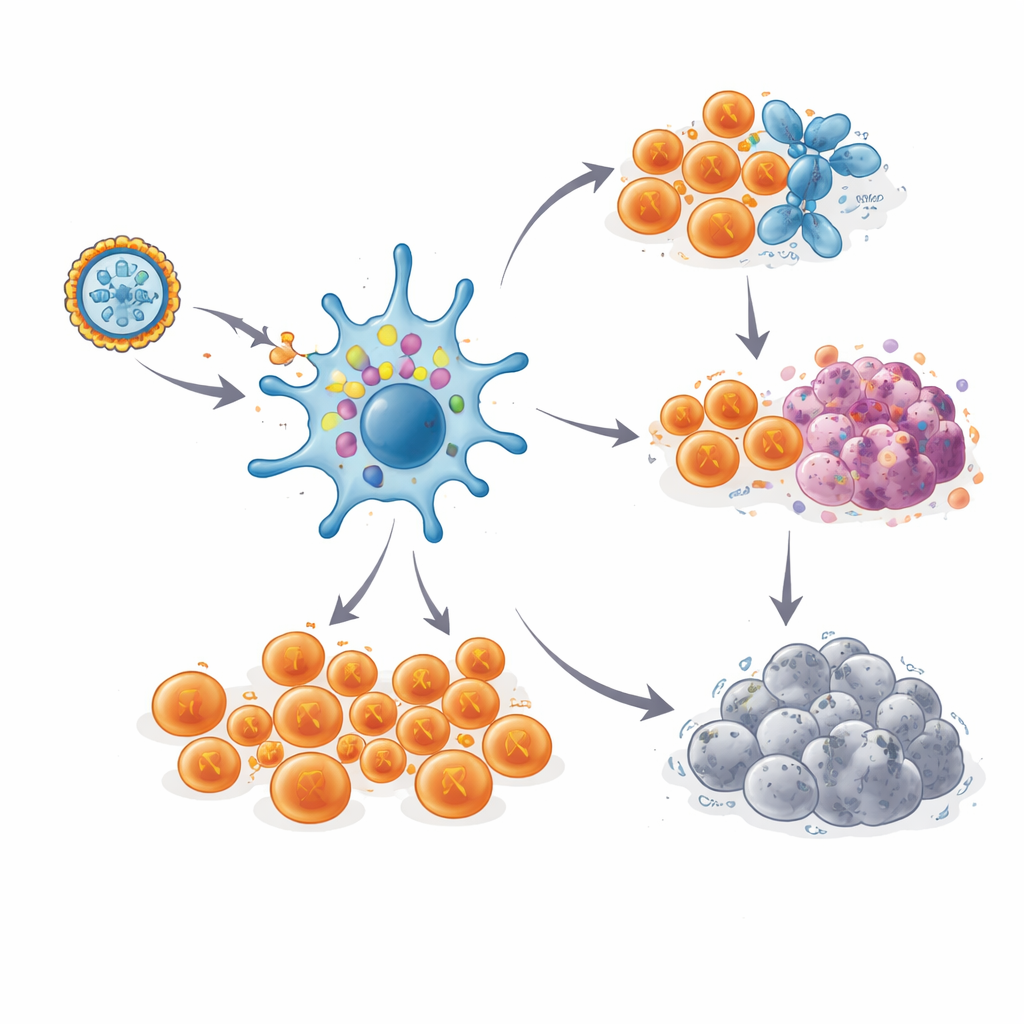
持久的免疫记忆
重要的是,这些 T 细胞反应并未迅速消失。大多数患者的强反应在接种期间达到峰值,随后略有下降,但在一至三年半内仍维持在较高水平,即便没有加强针。通过追踪单个 T 细胞克隆的独特受体“条形码”,科学家能够在一名长期无癌患者中追踪到特定的新抗原反应性细胞长达六年。详尽的单细胞分析显示这些细胞有两种主要归宿:许多细胞成为高度武装的杀伤性 T 细胞,准备摧毁携带相应新抗原的任何细胞;另一些则发育成更为罕见的、具有自我更新标志的干样记忆库,提示如果癌细胞重新出现,这一储备能够再生新一波战斗细胞。
患者的结局如何
从第一剂疫苗开始随访中位时间略超过五年后,14 名女性中有 11 人未出现癌症复发;其中一人在缓解期因与癌症无关的原因去世。三名女性发生复发,她们的病例提供了个性化疫苗有时失败的线索。一名患者仅产生微弱的 T 细胞反应,后来接受了另一种免疫疗法(抗 PD‑1 抗体)并获益,但最终仍因广泛转移而去世。第二名患者有遗传风险并在双侧乳房均有肿瘤;疫苗仅基于一侧肿瘤设计,后续证据显示复发来自遗传上不同、未被疫苗覆盖的另一侧肿瘤。第三名患者产生了强烈的疫苗诱导 T 细胞并侵入复发肿瘤,但癌细胞大部分丧失了在表面展示新抗原所需的关键分子,从而有效地对免疫攻击隐蔽起来。
这项工作对未来的重要性
这是一项早期临床研究,规模小且无对照组,因此不能证明单靠疫苗就能防止复发。尽管如此,研究表明从患者自身肿瘤构建复杂的个性化 mRNA 疫苗在常规医院环境中是可行的,通常耐受性良好,并能诱发针对多种癌症特异性靶点的强大且持久的 T 细胞军团。研究结果还突出了肿瘤可能采取的逃逸途径,例如丢失抗原展示机制或来自未被覆盖的病灶,这提示需要与其他免疫疗法联合或进行更广泛的肿瘤测序。对于面临三阴性乳腺癌的患者来说,这项工作表明,术后给予的定制疫苗未来或能通过将自身免疫系统转变为持久且高度特异的防线,帮助阻止疾病复发。
引用: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
关键词: 三阴性乳腺癌, mRNA 癌症疫苗, 新抗原免疫疗法, T 细胞免疫, 肿瘤复发