Clear Sky Science · zh
衰老促进小胶质细胞积累降解缓慢的突触蛋白
为何我们大脑的蛋白质清理随年龄增长至关重要
我们大多数人希望随着年龄增长仍然保持头脑敏锐,但年龄是阿尔茨海默病和其它痴呆症的最大风险因素。这项研究提出了一个看似简单的问题:随着年龄增长,大脑细胞内部日常的“家务”——蛋白质的维护——发生了什么变化?研究者在小鼠中构建了新的分子工具以追踪新合成的神经元蛋白质随时间的命运,描绘了蛋白质如何更新、如何聚集成凝块,以及大脑的免疫细胞小胶质细胞如何帮助清理这些垃圾。研究结果显示,蛋白质清理总体变慢,且集中发生在突触——即神经元交流的连接处——这或能部分解释与年龄相关的记忆衰退。
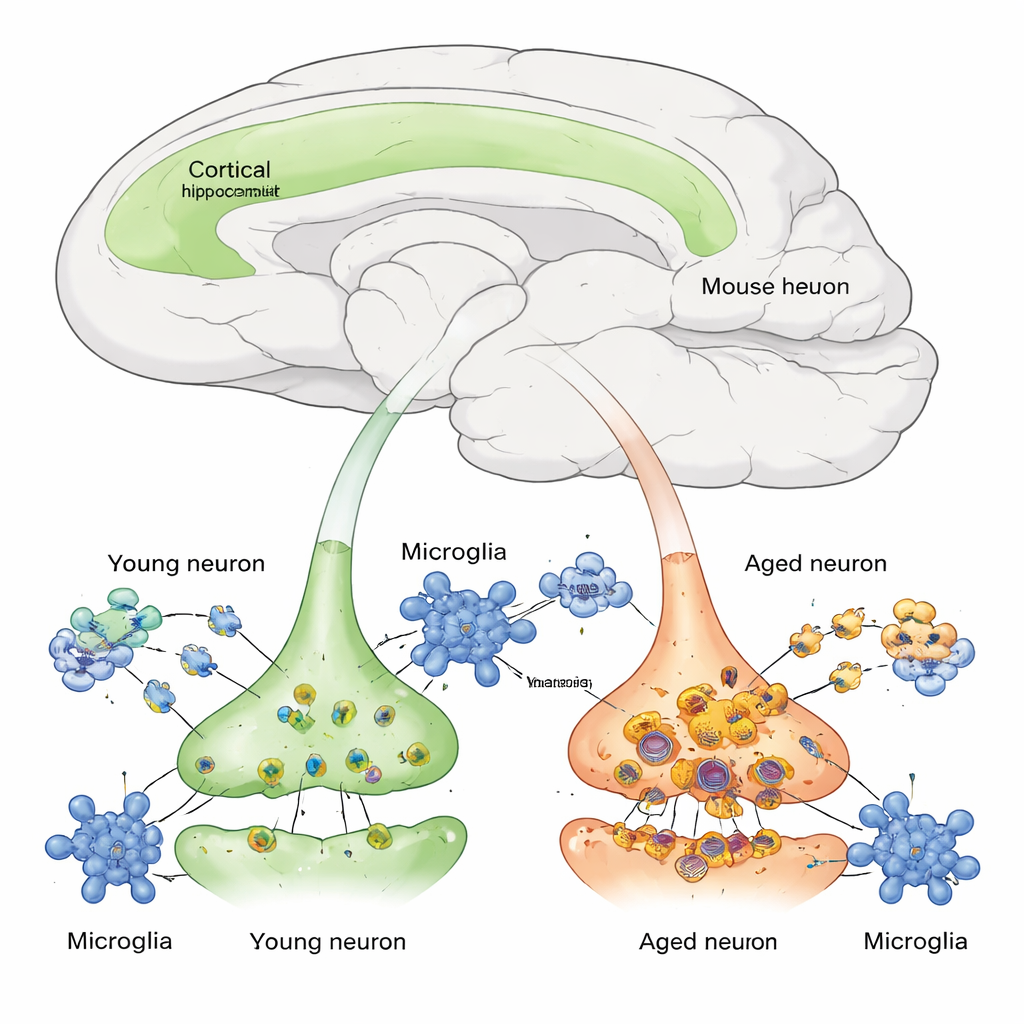
在活体脑细胞中追踪新蛋白
细胞中的蛋白质不断合成与降解,这一平衡称为蛋白稳态。此前,很难在活体哺乳动物脑内对特定细胞类型测量这一过程。作者工程化小鼠,引入一种名为 BONCAT 的遗传“标记”系统,使得只有某些神经元——受 Camk2a 启动子驱动的神经元,主要为皮层和海马的兴奋性神经元——在新合成的蛋白中掺入一种特殊且可点击的氨基酸。在给药短期标记后,研究团队能够通过质谱拉下并鉴定仅来自新合成神经元蛋白的分子,并随后观察这些蛋白在停止标记后的“消退”过程,即随降解而减少的变化。
衰老如何减慢蛋白质更替
研究者使用病毒载体版本的标记工具,对年轻(4 个月)、中年(12 个月)和老年(24 个月)小鼠的神经元进行了标记。随后在多个脑区——感觉皮层与视觉皮层、海马和下丘脑——在为期两周的“追踪”期内跟踪数千种蛋白。在对这些衰减曲线建模后,他们估算了每种蛋白的半衰期,即被清除一半所需的时间。总体来看,神经元蛋白的半衰期从年轻到老年大约翻倍,且大部分减速在中年之后出现。该效应在不同脑区间有所差异,且某些蛋白集合以紧密协调的方式共同降解,表明整个通路——例如控制突触信号传导的通路——具有相似的、与年龄相关的动力学特征。
蛋白聚集与脆弱的突触
降解速度变慢会提高蛋白质错误折叠并粘连在一起的风险。团队从老年小鼠脑中分离出去污剂不溶性的聚集物,并利用他们的神经元标签定义了包含 1,726 种神经元蛋白的“聚集蛋白组”。几乎一半在老化中降解减慢的蛋白也出现在这些聚集体中,许多蛋白此前的遗传学研究已将其与神经发育或神经退行性疾病联系起来。突触蛋白尤为突出:突触前与突触后机制的组分、细胞连接蛋白以及位于突触处的线粒体元件在降解缓慢和聚集的蛋白中高度富集。显微镜验证显示,诸如 RTN3 和 SRSF3 等特定蛋白在老年小鼠海马中形成类似聚集体的点状结构,但在年轻小鼠中并不明显。这种以突触为中心的蛋白稳态失衡,与长期以来的证据一致:突触丧失与认知衰退密切相关。
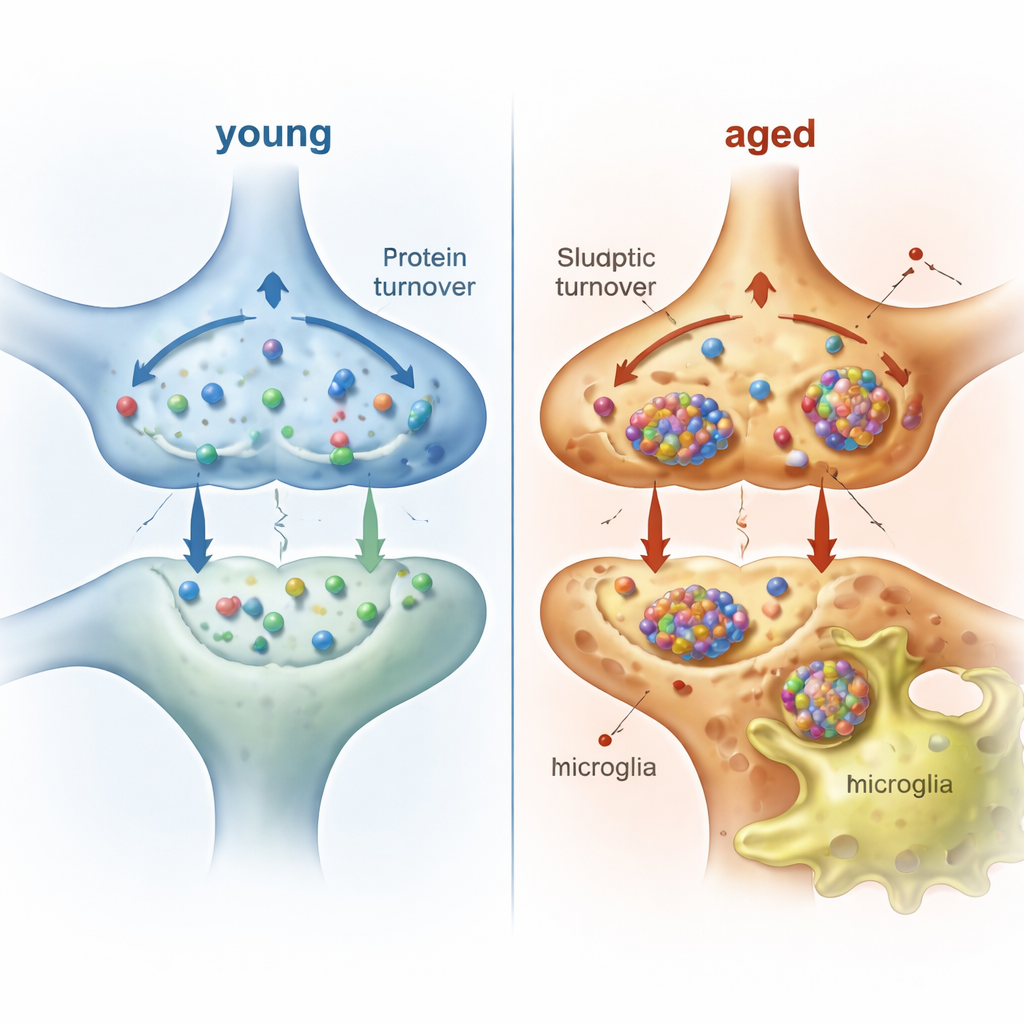
作为大脑清道夫的小胶质细胞
神经元并非独自承担这一负担。小胶质细胞作为大脑的常驻免疫细胞,会不断巡视并修剪突触。为了解在活体动物中小胶质细胞实际摄取了哪些来自神经元的物质,作者在年轻和老年小鼠中对神经元蛋白进行了为期一周的标记,然后分离纯化数十万个小胶质细胞,并拉出其中任何被标记的蛋白。他们在小胶质细胞内检测到数百种神经元蛋白,并以突触、膜和线粒体成分为主。许多这些蛋白携带信号序列或已知为外泌体货物,提示分泌可能是转移的一条途径,而其它则与小胶质细胞吞噬突触成分一致。在老年小鼠中,小胶质细胞内含有更多种类和更大量的神经元来源蛋白,但突触前与突触后成分的比例仍大致相当。
当清理失效时,大脑为此付出代价
通过叠合三组数据集——随年龄降解变慢的蛋白、出现在神经元聚集体中的蛋白、以及在老年大脑中在小胶质细胞内富集的蛋白——研究识别出 166 种位于这些过程交叉点的蛋白。超过一半在老年小胶质细胞中富集的神经元来源蛋白表现出某种与年龄相关的蛋白稳态问题。许多这些蛋白由先前被标记为阿尔茨海默氏病、帕金森氏病及其它脑部疾病风险因子的基因编码。综合来看,结果勾画出一个级联过程:随年龄增长,神经元蛋白周转变慢,尤其在突触处;脆弱的蛋白更可能错误折叠并聚集;小胶质细胞越来越多地清除这些受损成分,可能通过吞噬受压的突触来实现。从短期来看,这或许能保护神经元,但数十年累积下来可能促成突触丧失与认知受损。因此,理解并最终恢复健康的神经元蛋白稳态,可能是维持晚年大脑韧性的关键策略。
引用: Guldner, I.H., Wagner, V.P., Moran-Losada, P. et al. Ageing promotes microglial accumulation of slow-degrading synaptic proteins. Nature 650, 930–941 (2026). https://doi.org/10.1038/s41586-025-09987-9
关键词: 大脑衰老, 蛋白质更新, 突触, 小胶质细胞, 神经退行性