Clear Sky Science · zh
依赖多胺的代谢屏蔽调控可变剪接
微小分子如何帮助细胞“读”基因
在每个细胞内部,相同的 DNA 剧本可以有多种读取方式,使得有限数量的基因能够产生成千上万种蛋白质。这种灵活性依赖于一种称为可变剪接的过程,它在 RNA 信息被翻译成蛋白质之前对其进行编辑。本文揭示了一类带正电的小分子——多胺,悄然引导这一编辑步骤,充当一种保护性屏蔽,帮助细胞决定产生哪种 RNA 变体。由于可变剪接在癌症、大脑功能和干细胞中至关重要,发现这一隐藏的调控层对健康与疾病具有广泛影响。
存在于每个细胞中的带电小帮手
多胺是体积小、柔性的分子,带有多个正电荷。细胞由基本营养物质合成它们,长期以来人们已知它们是促进生长和存活的助力,尤其在像肿瘤这样快速分裂的细胞中。作者探问多胺是否不仅仅作为“燃料”,也充当信号。通过在前列腺癌细胞和小鼠中部分抑制多胺合成,他们随时间测量了蛋白质和 RNA 的变化。他们发现,在总体多胺水平显著下降之前,很早就出现了一波明显的蛋白质磷酸化变化——这是开启或关闭蛋白质开关的化学标记——尤其集中在细胞 RNA 编辑机器,即剪接体的组分上。
重布细胞的 RNA 编辑器
针对 RNA 的变化,团队使用深度测序跟踪在抑制多胺合成时的可变剪接。数百个 RNA 片段在癌细胞系、正常细胞类型和小鼠组织中出现不同的跳跃或包含模式。这些变化并非仅仅是细胞分裂变慢或另一种已知的多胺依赖过程(称为假赖氨酸化)的副作用。相反,当研究者向细胞补充外源多胺时,许多剪接改变会迅速恢复到接近正常。用药物和遗传工具降低多胺都产生了相似的剪接模式,且用药物组合进一步降低多胺使这些改变更为显著,证实了该效应与多胺可得性紧密相关。
一个隐藏的靶点:SF3 剪接模块
为确定多胺在剪接机器中作用的位置,作者将降低多胺引起的剪接特征与通过单独沉默 300 多个已知剪接因子生成的大型参考图谱进行比对。最接近的匹配指向剪接体的一个特定部分——SF3 亚复合体,它有助于识别 RNA 中的关键信号。对公开的蛋白–RNA 结合数据进行的计算分析支持这一联系:那些因多胺缺失而剪接发生改变的 RNA 特别倾向于被 SF3 蛋白结合。当团队通过遗传手段或药物部分失活 SF3 组件时,多胺耗竭引起的剪接效应在很大程度上被抵消,表明完整的 SF3 活性是这一新型调控通路所必需的。 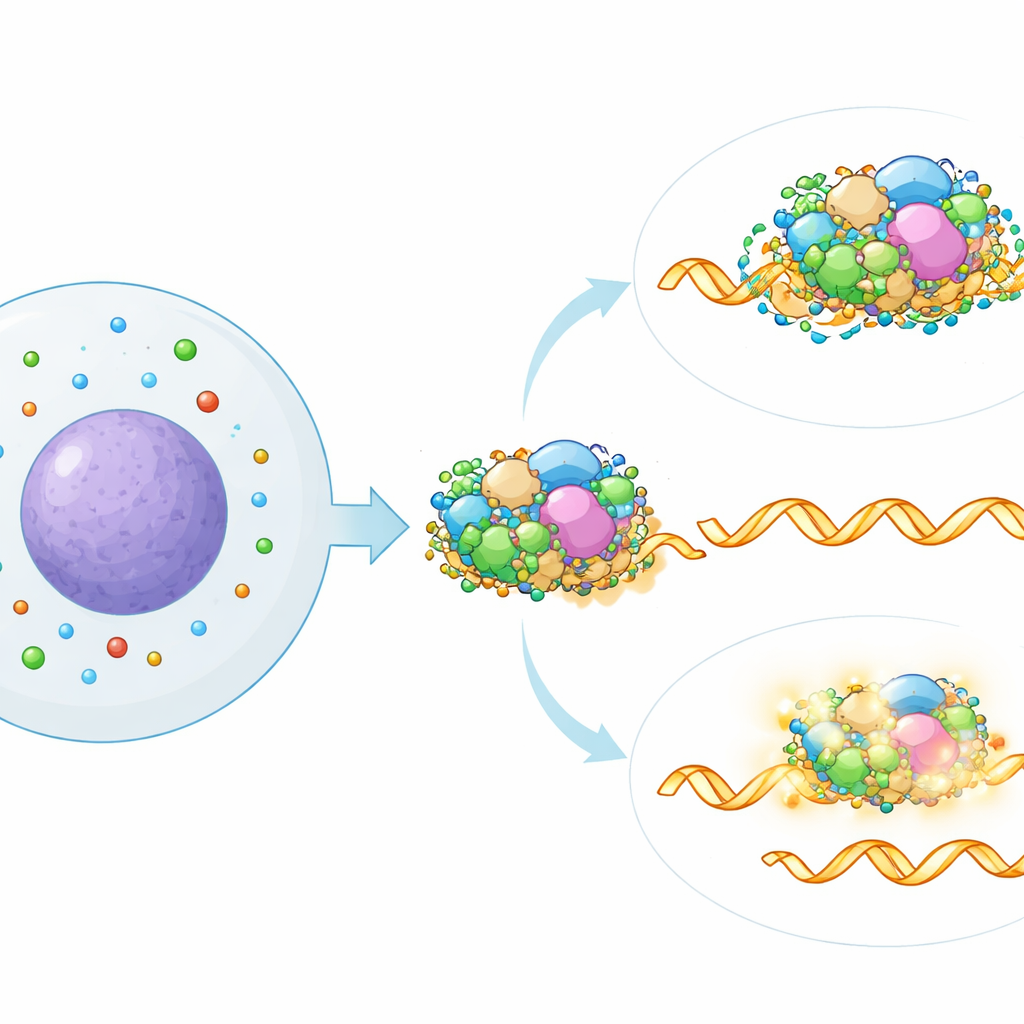
代谢屏蔽:多胺如何阻止蛋白质标记
深入研究时,研究者注意到 SF3 蛋白上受影响最严重的磷酸化位点聚集在含有大量带负电氨基酸的短序列上。分子建模和核磁共振实验证明,多胺嵌入这些酸性斑块,与之形成多重静电接触,并部分覆盖邻近的丝氨酸残基(通常是磷酸基团附着的位置)。这种物理上的“拥抱”降低了这些位点被蛋白激酶——附加磷酸基团的酶——接近的可及性。在体外实验中,加入多胺直接阻止了一种叫 CK1 的激酶对 SF3 蛋白的磷酸化。在细胞中,抑制 CK1 及其近亲 CK2 减弱了多胺缺失引起的剪接变化;而特意构建的小鼠其 SF3A3 蛋白缺失三个关键磷酸化位点后,对多胺依赖的剪接变化基本呈不敏感。 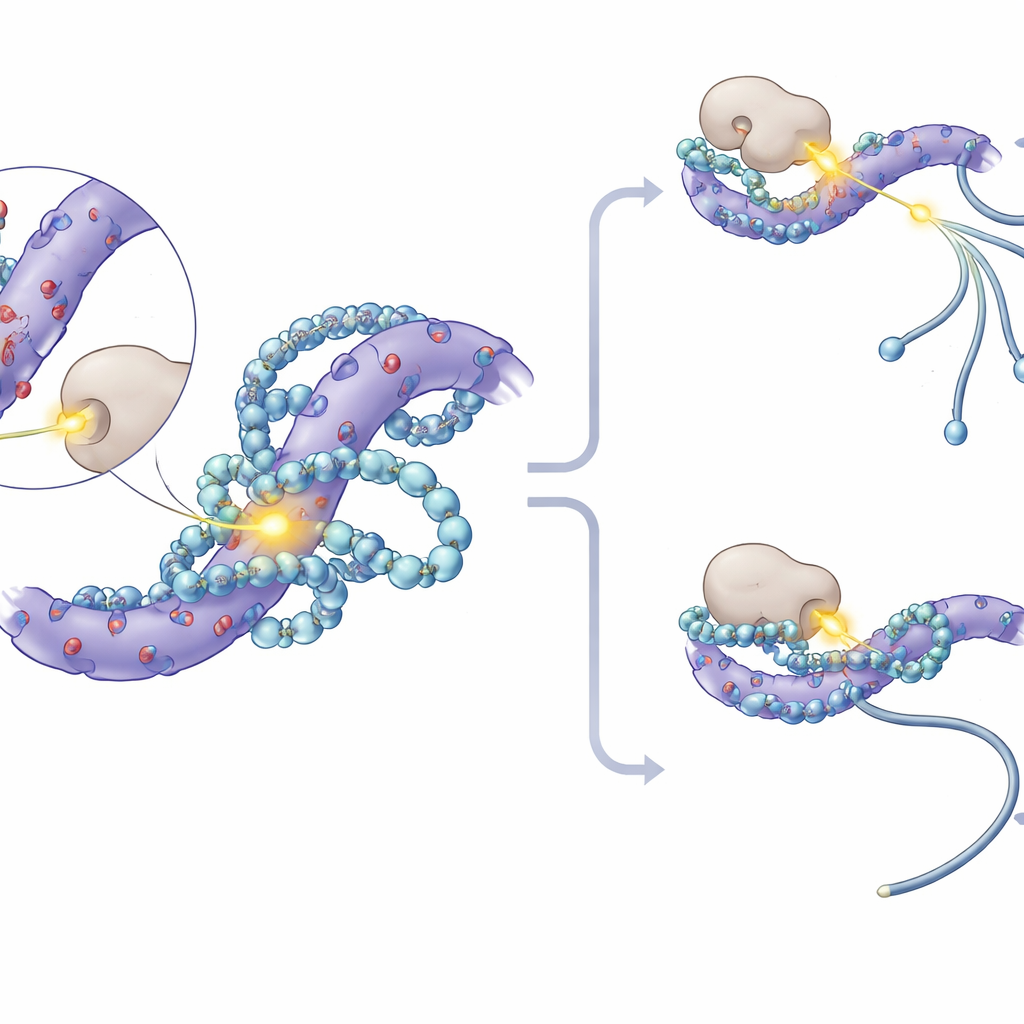
将功能拆分的设计分子
该研究还介绍了一种类多胺药物 BENSpm,它带有更强的正电荷,同时抑制细胞自身的多胺合成。BENSpm 紧密结合 SF3 的酸性斑块并阻断激酶作用,就像天然多胺一样,但在真实多胺短缺时它并不能恢复细胞生长。这使作者能够将经典的多胺功能(支持生长和代谢)与新定义的屏蔽作用区分开来。在小鼠胚胎干细胞中,耗竭多胺促使细胞失去“干性”标志 Nanog 并改变其剪接景观。尽管正常多胺合成持续被抑制,BENSpm 仍能恢复剪接谱和 Nanog 的表达,表明代谢屏蔽是维持干细胞身份的关键要求。
这一发现为何重要
通俗地说,这项工作表明多胺像一双微小的保护手套包裹在关键剪接蛋白的敏感部位上。当手套戴着时,激酶不易抓取并标记这些位点,细胞的 RNA 编辑维持正轨;当多胺低时,手套脱落,磷酸化激增,剪接模式发生转变,这对癌细胞和干细胞均有影响。通过定义这一“代谢屏蔽”机制并提供一个可选择性模拟它的工具分子,该研究为在不改变 DNA 的情况下调节基因读取打开了新途径,可能启发未来针对癌症和再生医学中剪接的治疗策略。
引用: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
关键词: 多胺, 可变剪接, RNA 处理, 代谢信号, 干细胞调控