Clear Sky Science · zh
配体特异性激活轨迹决定细胞中 GPCR 的信号传导
同一受体如何表现得像多个开关
如今许多药物作用于一大类细胞表面蛋白——G 蛋白偶联受体(GPCR)。这些受体影响心率、情绪、呼吸及无数其他生理功能。几十年来人们把它们视为简单的开–关开关:药物结合,开关翻转,细胞内产生信号。本文表明现实要丰富得多。作者在受体上直接内置了一种新型荧光“侦察器”,在活细胞中观察不同药物如何将同一受体沿着不同的激活路径推送——就像在城市中选择不同路线——以产生不同的信号模式。理解这些隐藏的路径有助于设计在带来期望疗效同时避免副作用的药物。
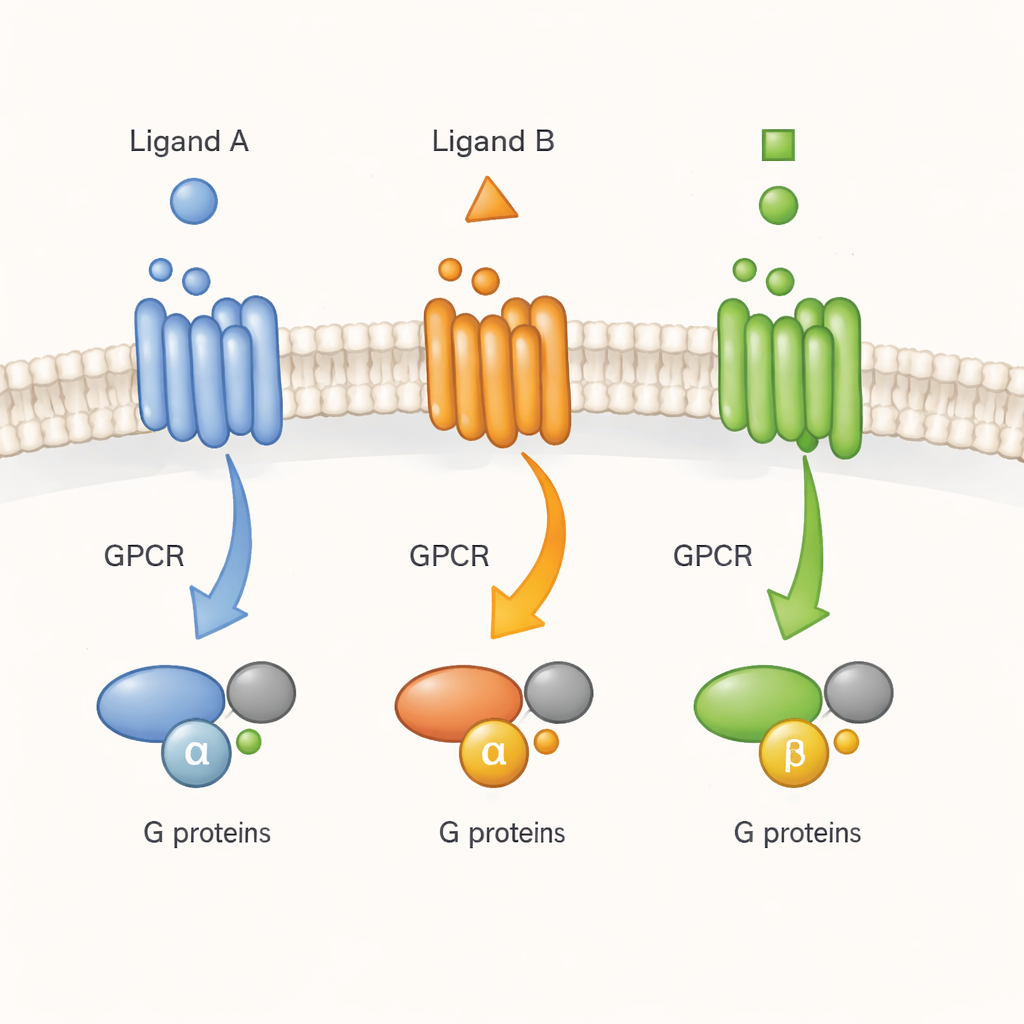
实时观察细胞的“门铃”
GPCR 常被比作分子门铃:信号分子(配体)从外部按铃,受体将信息传给内部的 G 蛋白。此前在去垢剂中对纯化受体的研究表明,GPCR 并非简单地在一种失活形态和一种活化形态之间切换。相反,它们会采样多种构象,药物可以以不同程度稳定这些构象。但尚不清楚在拥挤、动态的活细胞环境中是否存在相同的复杂性。在此研究中,作者聚焦于一个代表性受体——M2 毒蕈碱型乙酰胆碱受体(M2 受体),它是心脏和神经活动的重要调节因子,探讨不同配体是否将其驱动至对实际细胞信号传导具有意义的不同激活构象。
在受体表面构建微小的光学报告器
为了在不干扰受体正常功能的情况下追踪其运动,研究团队使用了遗传密码扩展技术,该技术可在受体外表的选定位置插入一种特殊设计的氨基酸。这个化学“锚点”可以在活细胞中与小型荧光染料点击连接。通过扫描 72 个位置并仅保留那些仍表现为正常受体的位点,他们构建了一组七个 M2 受体变体,每个变体在不同的外环位点携带一个荧光染料。当施加天然信使乙酰胆碱时,这些位点的染料亮度以特征性的方式上升或下降,展示了受体外表各部分在信号启动时如何移动。关键是,这些标记受体仍能激活 G 蛋白并进行正常内吞,表明这些报告器是忠实的,而非破坏性的。
药物留下独特的“构象指纹”
研究者随后比较了几种均能激活 M2 受体但强度不同的药物:体内自身的乙酰胆碱、一种超强合成激动剂 iperoxo,以及两种较弱的部分激动剂阿雷可林(arecoline)和毛果芸香碱(pilocarpine)。每种药物在七个报告位点上都产生了独特的荧光变化模式——一种构象指纹。在大多数位点上,位移大小与药物激活受体的强度相对应。然而在两个位点上,关系呈倒置:较弱的药物产生了最大的变化,而最强的药物几乎没有引起变化。这种行为无法用单一活性状态解释。相反,它表明同一受体在活细胞中可以采纳几种不同的活性构象,某些构象被强效药物偏好,另一些则被弱效药物偏好。
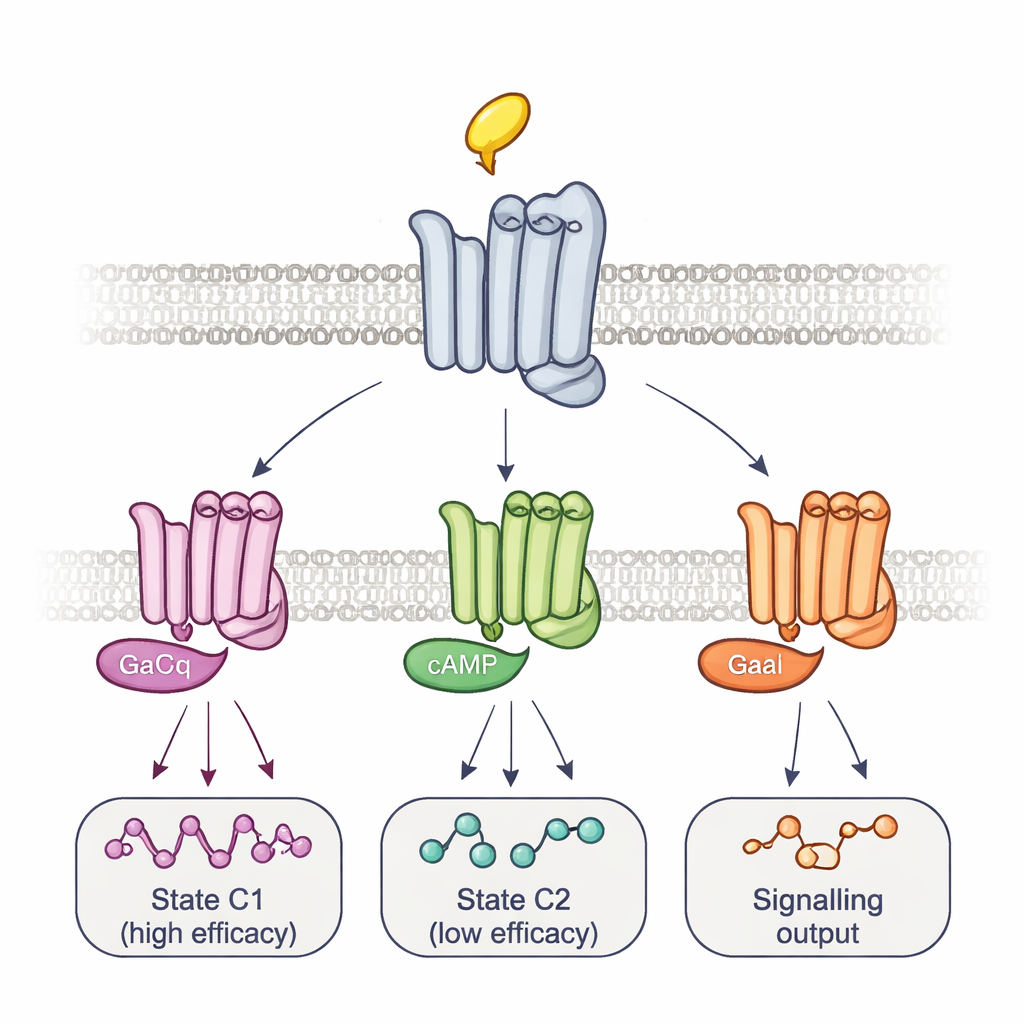
多种复合体与时序化的信号路径
为将这些构象与实际信号相连,团队改变了 G 蛋白本身。过表达一种可与受体形成非常紧密、寿命较长复合体的突变 G 蛋白,选择性地抹去了某些报告位点的信号,同时增强了其他位点的信号。该模式连同荧光变化的时序显示了至少两种主要的受体–G 蛋白复合体:一种形成迅速、效能高的复合体,另一种形成较慢、效能低的复合体。不同药物改变了这些复合体之间的平衡,甚至通过不同的中间步骤到达目标,描绘出药物特异的激活轨迹。使用另一种监测 14 种 G 蛋白亚型面板的生物发光测定,作者表明这些平衡不仅决定药物总体激活信号的强弱,也决定被激活的具体 G 蛋白类型。例如,阿雷可林优先激活某些 Go 蛋白,而毛果芸香碱则强烈偏向低效能复合体。
这对更好药物设计的意义
对非专业读者而言,关键信息是:单一受体并非仅仅是一个开关,而是一簇相关的开关,每个开关可通过不同路径到达,并各自连接到略有不同的下游效应。该研究在完整细胞中直接揭示了那些路径和状态,而不是在简化的试管体系中。通过绘制特定药物如何偏向受体进入特定复合体和 G 蛋白伙伴的图谱,研究者得到了设计“更聪明”药物的蓝图——能够将受体引导至产生有益信号而避开与副作用相关状态的化合物。本文开发的荧光生物传感策略应可推广到许多其他受体,为观察活细胞中药物作用的实时编舞打开了一扇窗。
引用: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
关键词: GPCR 信号传导, 配体效能, G 蛋白, 构象生物传感器, 药物发现