Clear Sky Science · zh
双向 CRISPR 筛选解析依赖 GLIS3 的纤维化细胞回路
愈合何时变成有害瘢痕
我们的肠道本应在每次擦伤和刺激后自行修复。但在克罗恩病和溃疡性结肠炎等慢性疾病中,这一修复过程可能失控,导致厚而僵硬的瘢痕组织使肠腔狭窄,甚至需要手术治疗。本研究揭示了肠道中免疫细胞与结构细胞之间一段隐藏的对话,这段对话驱动了瘢痕形成,并定位到一个主控开关——名为 GLIS3 的基因,为打破这一循环提供了潜在新途径。
受炎症侵袭肠道中的隐秘网络
为理解为何部分患者会发展为顽固性炎症与纤维化,研究者构建了人类肠道的细胞“图谱”。他们将单细胞 RNA 测序(读取单个细胞内活跃基因)与空间谱系定位(映射这些细胞在真实组织切片中的位置)结合起来。使用来自克罗恩病、溃疡性结肠炎患者及对照者的样本,他们在肠壁中描绘了超过四百万个细胞。在这片人群中,一个成纤维细胞亚群格外引人注目:炎症相关成纤维细胞(IAF)。这些细胞在活动性和慢性结肠炎区域集中,携带与对常规抗 TNF 治疗耐药相关的基因特征,表明它们在难治性疾病中扮演核心角色。 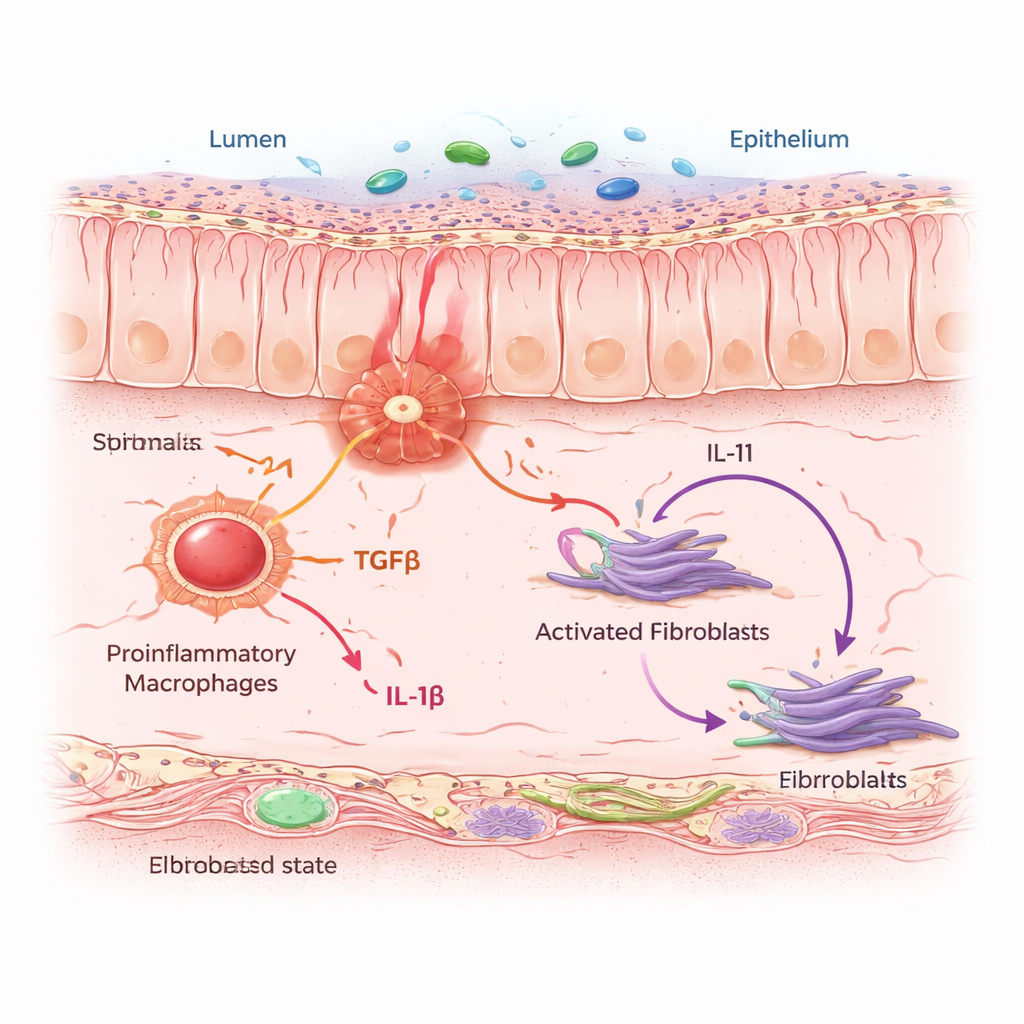
巨噬细胞低语,成纤维细胞造瘢痕
IAF 并非孤军奋战。它们聚集在与促炎巨噬细胞密集的“邻里”中——这些免疫细胞感知危险并释放警报信号。通过计算模型和细胞共培养实验,团队展示出当巨噬细胞被驱动到炎症状态时,会分泌两种关键的信使蛋白:TGFβ 和 IL-1β。邻近的成纤维细胞通过特定受体感知这些信号。当两种信号同时到达时,成纤维细胞会转换为 IAF 状态,并开始产生 IL-11(一种已被怀疑促进纤维化的细胞因子),以及胶原和其他使肠壁增厚、变僵的基质蛋白。在接受慢性结肠炎处理的小鼠中,阻断 IL-11 或选择性在成纤维细胞中删除 IL-11 可减少胶原堆积,而不会阻止初始炎症,显示 IL-11 是瘢痕阶段的关键驱动因子。
GLIS3:纤维化成纤维细胞中的主控开关
为将相关性推向机制性理解,作者使用了强大的全基因组 CRISPR 工具。他们改造了人类成纤维细胞,使 IL-11 产生可通过荧光标签监测,然后并行进行了基因敲除和基因激活筛选。通过对在 TGFβ 和 IL-1β 刺激后产生异常高或低 IL-11 的细胞进行分选,他们鉴定出控制该反应的基因。在众多信号组分中,一个转录因子——GLIS3——脱颖而出成为重要调控因子。当 GLIS3 被禁用时,成纤维细胞产生的 IL-11 大幅减少;当其被增强时,IL-11 激增。额外实验显示,GLIS3 会在巨噬细胞信号作用下进入成纤维细胞细胞核,直接结合 IL11 基因及其他基因附近的 DNA,并激活一整套炎症和纤维化基因程序,包括胶原及吸引更多免疫细胞的因子。 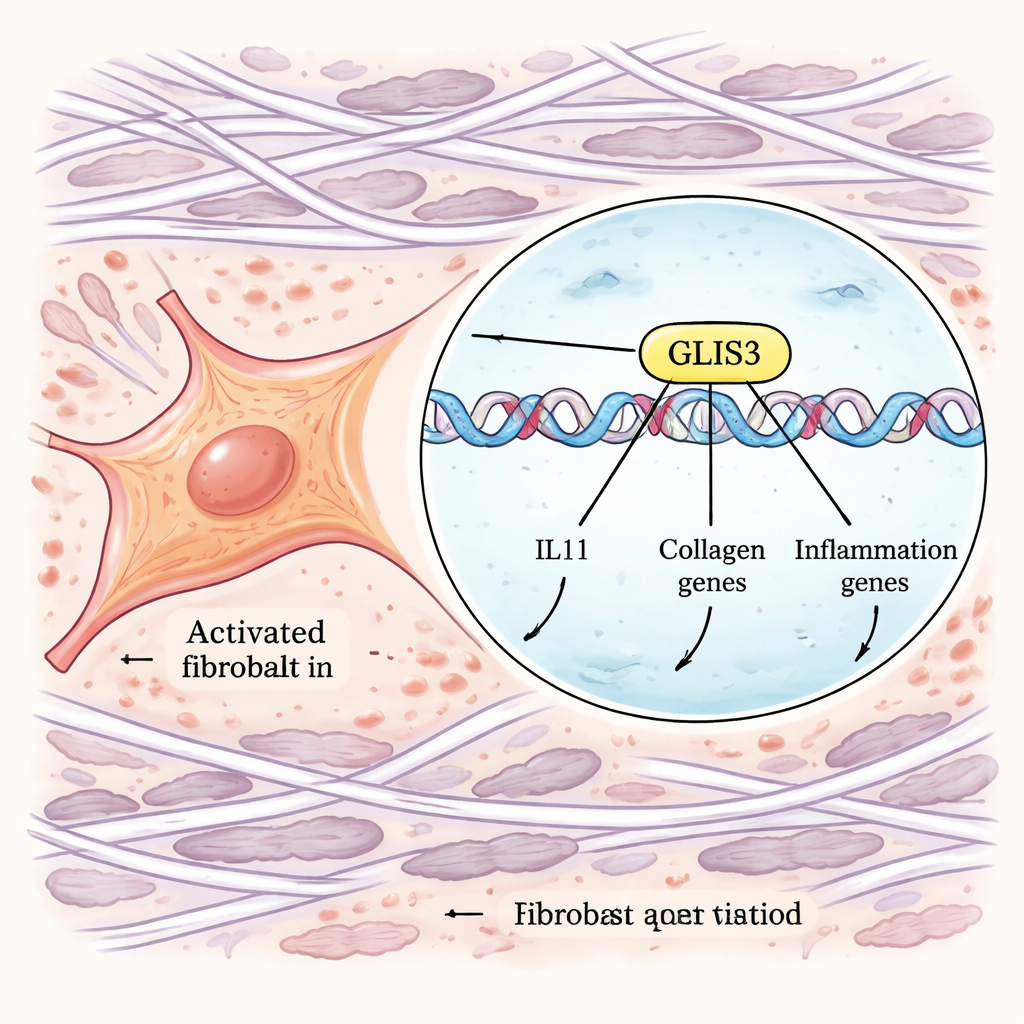
从小鼠模型到患者严重度
团队接着探问这一由 GLIS3 驱动的程序在生物体内是否重要。在小鼠中,他们构建了仅能在成纤维细胞中移除 GLIS3 的品系。当这些动物接受慢性结肠炎刺激时,表现出更少的肠道瘢痕,胶原和纤维化基因表达水平降低,并且与正常小鼠相比炎症程度也有所减轻。空间映射确认 GLIS3 缺失的小鼠具有更少产生 IL-11 的成纤维细胞,以及更少邻近被激活的巨噬细胞和中性粒细胞,表明破坏 GLIS3 会削弱整个炎症—纤维化回路。转向一大批儿科溃疡性结肠炎队列,作者提炼出由 50 个基因组成的 GLIS3“特征”并发现,其在结肠活检中的活性与疾病严重度及 IAF 与激活巨噬细胞的丰度紧密相关,直接将该通路与患者结局联系起来。
打破炎症与瘢痕的循环
对非专业读者来说,结论是这项工作揭示了一个自我强化的回路:促炎巨噬细胞促使成纤维细胞转变为形成瘢痕的 IAF;这些 IAF 在 GLIS3 的控制下大量分泌 IL-11、胶原和其他重塑组织并吸引更多炎性细胞的因子。广泛抑制免疫系统的常规药物可能无法完全打断这一回路,这也部分解释了为何许多患者最终对现有疗法失效。通过将 GLIS3 和产生 IL-11 的成纤维细胞状态识别为炎症—纤维化回路中的关键节点,这项研究为更有针对性的策略指明了方向——瞄准成纤维细胞而不仅仅是免疫细胞——未来或可预防或逆转炎性肠病乃至其他慢性炎性疾病中的瘢痕形成。
引用: Pokatayev, V., Jaiswal, A., Shih, A.R. et al. Bidirectional CRISPR screens decode a GLIS3-dependent fibrotic cell circuit. Nature 650, 997–1006 (2026). https://doi.org/10.1038/s41586-025-09907-x
关键词: 炎性肠病, 肠道纤维化, 成纤维细胞, 巨噬细胞, GLIS3